В связи с ухудшением состояния окружающей среды, увеличением объемов вредных веществ, выбрасываемых промышленными предприятиями, повышается процент населения, страдающих различными заболеваниями, в том числе онкологическими, заболеваниями нервной системы и д.р. В связи с этим, актуальным является поиск новых путей синтеза прекурсоров лекарственных препаратов на основе гетероциклических систем изохинолина, которые служат структурными компонентами большого числа алкалоидов. Именно это стимулирует интерес к этому классу соединений, среди которых найдены и с успехом применяются многие лекарственные средства (транквилизаторы, антидепрессанты и д.р.). Работы по установлению структуры, синтез природных аналогов, поиск новых биологически активных соединений на основе изохинолина оказали существенное влияние на развитие химии гетероциклических соединений и органической химии в целом.
Подавляющее большинство изохинолинов, и поликонденсированных гетероциклов на их основе получены в результате использования давно открытых и хорошо изученных реакций – Померанца-Фрича, Бишлера-Напиральского, Пикте - Шпенглера и некоторых других. Каждому из этих методов присущи определённые недостатки: невысокие выходы (Померанц-Фрич), необходимость дегидрирования промежуточных дигидроизохинолинов (Бишлер-Напиральский) и т.д.
В последнее время одним из перспективных путей получения таких соединений является реакция кислотно-катализируемой циклизации арилзамещенных аминогетероциклов с карбонильными соединениями. Этот метод позволяет с помощью доступных реагентов, в приемлемых условиях и с высокими выходами получить конденсированные гетероциклические системы с ядром изохинолина.
Пиразоло[4,5-с]изохинолины являются интересными и перспективными соединениями, но в литературе методы их получения представлены мало. На основе метода, разработанного в отделе химии биологически активных соединений ИнФОУ, была апробирована методика получения пиразоло[4,5-с] изохинолинов, заключающаяся в циклизации аминопиразолов. Особенность данного метода заключается в том, что полученные соединения не требуют дальнейшей ароматизации.
Была поставлена задача, получить новые гетероциклические системы, обладающие перспективными свойствами, а также разработать удобные препаративные методики получения известных труднодоступных производных изохинолина.
В ходе проводимой работы нами были синтезированы следующие соединения:
![1-(3,5-дихлорпиридил)-3-(метил)-7,8-(диметокси)-11-(4-хлорфенил) – пиразоло[4,5-с] изохинолин](aminoazin.gif)
1-(3,5-дихлорпиридил)-3-(метил)-7,8-(диметокси)-11-(4-хлорфенил) – пиразоло[4,5-с] изохинолин
![1-(2-бензтиазолил)-3-(метил)-7,8-(диметокси)-11-(4-хлорфенил)–пиразоло[4,5-с] изохинолин](aminoazin1.gif)
1-(2-бензтиазолил)-3-(метил)-7,8-(диметокси)-11-(4-хлорфенил)–пиразоло[4,5-с] изохинолин.
Для получения 1-(3,5-дихлорпиридил)-3-(метил)-7,8-(диметокси)-11-(4-хлорфенил)- пиразоло [4,5-с] изохинолина, на первой стадии кетонитрил (1) вводится в реакционный сосуд с веществом (2), при их взаимодействии образуется вещество (3). Действием парахлорбензальдегида на аминопиразол (3) получают соответствующий изохинолин.
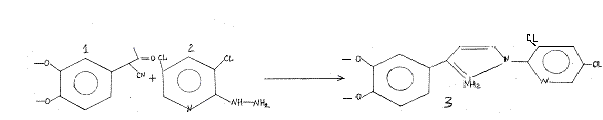
Реакция проводится в среде растворителя - изопропилового спирта с добавлением муравьиной кислоты. Исходные вещества помещаются в колбу с обратным холодильником, где кипят в течение 12-ти часов, продукт выпадает в виде кристаллов. После этого проводят нейтрализацию путем добавления аммиака в реакционную смесь, готовый продукт отфильтровывается. Выход составляет примерно 45%.
При синтезе 1-(2-бензтиазолил)-3-(метил)-7,8-(диметокси)-11-(4-хлорфенил) - пиразоло[4,5-с] изохинолина проводится реакция взаимодействия кетонитрила (1) с веществом (4), в результате образуется вещество (5).
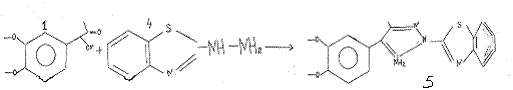
Следующей стадией является реакция взаимодействия парахлорбензальдегида и аминопиразола (5) с образованием изохинолина. Она проводится аналогично вышеописанной методике, выход - 63%.
Таком образом, в результате проведенной работы была апробирована новая методика получения пиразоло[4,5-с] изохинолинов, дающая приемлемые выходы, не требующая использования дополнительной ароматизации продуктов и дающая возможность получения соответствующих соединений на основе доступных реагентов.