
Факультет: Екології та хімічної технології
Спеціальність: Хімічна технологія високомолекулярних сполук
Метою роботи є складання та виконання методики дослідження процесів плавлення та кристалізації органічних речовин, що мають температуру плавлення меншу ніж 100оС.
В роботі розглянуті органічні речовини: тринітротолуол, нафталін, гипосульфіт, парафін та петролатум; фізико–хімічні основи процесів плавлення та кристалізації; методика дослідження, що складається з вивчення виготовлення розплавів в плавителях (в заводських умовах) та приготування їх лабораторних умовах; вивчення таких методів кристалізації, як лускування тротилу та кристалізація розплаву в формах (вироби ДПУ–830ТЛ), відпрацювання методики кристалізації в формах розплавів парафіну та петролатума.
Практичною цінністю цієї роботи є розробка методіки вивчення фізико-хімічних властивостей процесів кристалізації та плавлення високомолекулярних речовин в університетській лабораторії. Робота з речовинами, що вивчають, є небезпечною, тому потребує спеціальних умов, які зараз надає Донецький казений завод хімчних виробів, що складає певні труднощи для студентів та викладачей. Вихідом з цієї ситуації є вибір речовин, східних за властивостями з тринітротолуолом, а також розробка обладнання для проведення експериментів.
1 ВИБІР ОРГАНІЧНОЇ РЕЧОВИНИ,ЩО МАЄ ТЕМПЕРАТУРУ ПЛАВЛЕННЯ ДО 100oС
1.1 Тринітротолуол
Тротил – це кристалічна речовина блідно-жовтого кольору, відноситься до бризантних вибухових речовин.
Тротил – пожежно-небезпечний, фізично і хімічно стійкий. При нагріванні в плині 100 годин при 1500 oС він не змінює властивість, температура розпаду складає 1600oС.
Так як тротил має негативний кисневий баланс, він має при вибуху велику кількість утворювання оксиду вуглецю. Він токсичний, викликає тротилову інтоксикацію організму, подразнення шкіри і хворобу очей.
Утилізований дроблений тротил являє собою шматки поледіспорсного складу, нерегламентованої форми з включеннями лаку, емалей, грунтівок. Має колір від світло-жовтого до коричневого. Шматки розміром: не більше 60мм; не більше 10мм. Пресовані шашки мають колір від світло-жовтого до коричневого та діаметр до 45мм та висоту до 60мм.
Утилізований лускуйований тротил нерегламентованої форми полідисперсного складу. Колір мають від світло-жовтого до коричневого, а також має домішки лаку, емалей та грунтівок.
Утилізований гранульований тротил має гранули нерегламентованої форми від світло-жовтого до темно-коричневого кольору з домішками лаку, емалей, грунтівок. Розмір гранул:
- прохід гранул крізь сито з сіткою №5 по ГОСТ 3826 – не менше 50%;
- залишок гранул та їх зрощення на ситі з сіткою №10 – не більше 3%;
- з сіткою №14 – їх відсутність.
1.2 Нафталін
Нафталін-С10Н8 тверда кристалічна речовина з характерним запахом, що в воді не розчиняється, але добре – у органічних речовинах: бензолі, ефірі. Перегоняється з водяним паром.
Н. (від грецьк. naphtha – нафта), ароматичний вуглеводень; температура плавлення 80,3оС, температура кипіння 218оС; летючі, возгоняється при 50оС; щільність 1,15 г/см3 (15 оС).
Н. по хімічним властивостям згоден з бензолом: легко нітрується, сульфується, взаємодіє з галогенами. Відрізняється від бензола тим, що легше вступає в реакції.
В промисловості Н. отримують в основному з каменовугільної смоли (якій його 8-10%), а також виділяють з продуктів піролізу нафти. Останній значно чище каменовугільного.
Гідрування Н. дає тетралін та декалін, окислення-фталевий ангідрид.
Н. має важливе значення як вихідна речовина для отримання більшої кількості органічних полу продуктів (головним чином фталевого ангідриду) та фарбників ( на основі нафтолів, нафтиламінів та їх сульфокислот).
Найближчі гомологи Н. – метилнафталіни – також є в каменовугільній смолі та мають сходні з Н. властивості. Їх використовують, наприклад, для синтезу так званих регуляторів росту рослин; поліметілнафталіни – інсектициди; солі сульфокислот вислих гомологів Н. використовуються в якості емульгаторів.
1.3 Гипосульфіт
Натрію гипосульфіт (натрію тіосульфат) – безкольорові прозорі кристали без запаху з моноклінною решіткою; температура плавлення 48,5 оС (з розл.); 1,715 г/см3; солоновато-гірьки на смак. Отримані ді- та гемі гідрати, які плавяться інкогруентно відповідно при 65,5 та 74оС, а також метастабільні тетра- та гексагідрати.
Дуже легко розчиняється в воді (1:1), практично не розчиняється у спирті. При температурі близько + 50оС. Гіпосульфіт плавиться в кристалізаційній воді. Водяний розчин (30%, рН 7,8 – 8,4) стерилізують при температурі + 100оС протягом 30 хв (на 1л розчину додають 20г натрію гідрокарбоната). Гіпосульфіт натрію оказує проти токсичну, протизапалювальну та десенсибілізирующу дію.
Як протитоксичний засіб натрію гіпосульфіт використовують при отруєні сполуками мишяка, ртуті, свинця (утворюються неотруйні сульфіти), сінільної кислоти та її солями (утворюються менш отруйні роданисті сполуки), солями йоду, брому.
Гипосульфіт – відновник; сильні окисники з хлором хлору та слабкі з йодом в нейтральних розчинах. Гипосульфіт для видалення хлору при відбілюванні тканин, як закріпитель в фотографії, реактив в йодометрії.
1.4 Парафін
Парафін – високоподібна речовина, суміш межевих вуглевонів (алканів) складу від С18Н38 до С35Н72. Температура плавлення 40-65оС, щильність 0,880-0,915 г/см3 (15оС). Отримують головним чином з нафти. П Застосовують для готування парафінистого паперу, просочення деревини в сірниковому й олівцевому виробництвах, також як ізоляційний матеріал, хімічна сировина й т.д. У медицині використовується для парафінолікування. Парафіни являють собою суміш твердих вуглеводнів метанового ряду переважно нормальної будови з 18-35 атомами вуглецю в молекулі й температурою плавлення 45-65oС. У парафинах звичайно втримується деяка кількість ізопарафиновых вуглеводнів, а також вуглеводнів з ароматичним або нафтеновим ядром у молекулі.
Парафін – речовина білого кольору кристалічної будови з молекулярною масою 300—450, у розплавленому стані має малу в'язкість. Величина й форма кристалів парафіну залежать від умов його виділення: з нафти парафін виділяється у вигляді дрібних тонких кристалів, а з нафтових дистилятів і дистиллятных рафинатов селективного очищення – у вигляді великих кристалів. При швидкому охолодженні виділювані кристали дрібніше, ніж при повільному. Парафіни інертні до більшості хімічних реагентів. Вони окисляються азотною кислотою, киснем повітря (при 140oC) і деякими іншими окислювачами з утворенням різних жирних кислот, аналогічних жирним кислотам, що втримуються в жирах рослинного й тваринного походження. Синтетичні жирні кислоти, одержані окислюванням парафіну, застосовують замість жирів рослинного й тваринного походження в парфумерній промисловості, при виробництві змащень, мийних засобів і інших продуктів. Парафіны можуть бути виділені також з інших продуктів, напр., з озокерита. Залежно від фракційної сполуки, температури плавлення й кристалічної структури парафины розділяють на рідкі (температура tпл ? 27 oC), тверді (tпл=28-70oC) і мікрокристалічні (tпл > 60—80oC) — церезіни. При однаковій температурі топ. церезини відрізняються від парафинів більшою молекулярною масою, густотою й в'язкістю. Церезини енергійно реагують із димною сірчаною кислотою, із соляною кислотою, у той час як парафіни реагують із ними слабко. При перегонці нафти церезини концентруються в осаді, а парафін переганяється з дистилятом. Церезини, які концентруються в залишку після перегонки мазуту, представляють собою суміш циклоалканов і в меншій кількості твердих аренів і алканів. Ізоалканів у церезині порівняно мало. По ступені очищення парафіни розділяють на гачи (петролатумы),які містять до 30% (мас.) масел; неочищені парафіни (церезини) зі змістом масел до 6% (мас.); очищені й высокоочищенні парафини (церезини). Залежно від глибини очищення вони мають білий колір (високоочищенні й очищені марки) або злегка жовтуватий і від ясно-жовтого до ясно-коричневого (неочищені парафины). Для парафіну характерна пластинчаста або стрічкова структура кристалів. Очищений парафін має щільність 881—905 кг/м3. Церезины являють собою суміш вуглеводнів з кількістю вуглецевих атомів у молекулі від 36 до 55 (від З36 до З55). Їх витягають із природної сировини (природного озокерита також залишків высокопарафинистых сортів нафти, одержуваних при її переработкке) і роблять синтетично з окислу вуглецю й водню. На відміну від парафинів, церезини мають мелкокристаллическое будова. Температура плавлення 65—88oC, молекулярна маса 500—700. Парафины широко використовують в електротехнічної, харчовий (парафины глибокого очищення; tплавл = 50—54oC; зміст масел 0,5—2,3% по масі), парфумерній і іншій галузях. На основі церезину виготовляють різні композиції в промисловості побутової хімії, вазеліни; вони використовуються також як загустители у виробництві пластичних змащень, ізоляційних матеріалів в электро- і радіотехніку й воскових сумішах.
Неочищені тверді парафіны роблять методами: 1) знемаслювання гачей і петролатумів — побічних продуктів виробництва (депарафинизации) масел із застосуванням розчинників (суміші кетона, бензолу й толуолу, дихлоретан), одержуючи при цьому неочищені парафины (з гача) і церезини (з петролатума); 2) виділення й знемаслювання парафіну з дистилятів высокопарафинистых нефтей сумішшю кетона, бензола і толуола; 3) кристалізації твердих парафинов без застосування розчинників (шляхом охолодження в кристалізаторах і фильтропресування). Неочищені парафины після цього облагороджують з використанням кислотно-лужного, адсорбційного (контактного або перколяційного) або гидрогенизаційного доочищення (для видалення нестабільних речовин, які офарблюють і мають захід). Рідкі парафины виділяють із дизельних фракцій депарафінізацією з використанням виборчих розчинників (суміш ацетону, бензолу й толуолу), концертної депарафінізації (у виробництві низькозастигающого дизельного палива) і адсорбції на молекулярних ситах (виділення рідких парафинів З 10- за допомогою пористого синтетичного цеоліту).
Аналізуючи властивості перерахованих речовин, обираємо для проведення методики дослідження процесів плавлення та кристалізації такі речовини, як парафін та петролатум. Вибір обґрунтовується їх найменшою небезпечністю та невеликою температурою плавлення [4].
2 ФІЗИКО–ХІМІЧНІ ОСНОВИ ПЛАВЛЕННЯ ТА КРИСТАЛІЗАЦІЇ
2.1 Фізико-хімічні основи процесу плавлення
Метод виготовлення детонаторів заливкою характеризується наповнюванням рідкою масою із ВР у оболонку детонатора яка затверджує і відтворює монолітний розривний заряд, який володіє високою щільністю та механічною міцністю. Таким чином фізико-хімічним процесом являє собою процес плавлення тротилу, і процес його кристалізації.
Під плавленням зрозуміють процес переходу речовини із кристалічного стану в рідке. Якщо тверду кристалічну речовину нагрівати, то по досягненні визначеної температури, його температура залишається постійною, а речовина починає переходити із твердого в рідке. Це явище і носить назву плавлення.
Теплота, витрачається на перехід речовини із кристалічного стану в рідке (при температурі плавлення), називається схованою теплотою плавлення.
Теплота, що поглинається речовиною у процесі плавлення, при охолоджуванні виділяється в навколишнє середовища у тої ж кількості при зворотному процесі, називається кристалізацією.
У твердої кристалічної вибухової речовини молекули розташовуються в вузлах просторової решітки. Молекули вибухової речовини у кристалічної решітки утримуються силами Ван-дер-Ваальсу, які, крім того, певним чином орієнтують молекули органічної вибухової речовини відносно один одного. При нагріванні збільшується амплітуда теплового коливання молекул навколо їх положення рівноваги в решітки. Нагрівання приводить до збільшення середніх розмірів між молекулами і до розширення кристалу, але не змінює відносно розташування молекул в кристалі.
Теплове коливання молекул в кристалі поодчиняється закону Максвелла про розташування швидкостей молекул. З цього закону випливає, що навіть при низьких температурах я відносно не великої середньої кінетичної енергії молекул в кристалічної решітки завжди є деяка кількість молекул, які у наслідок взаємодії з сусідніми молекулами мають як завгодно більшу кінетичну енергію. Молекула , яка отримала на деяку мить енергію більш ніж необхідну для того, щоб вирватися з попереднього стану, в якому її утримають сили Ван-дер-Ваальса, залишає цей стан й займає інший, передаючи зайву енергію іншій молекулі. У новому стані молекула буде коливатися навколо свого стану рівноваги до того часу, доки знову не отримає надлишкову енергію, яка достатня для переходу до нового стану. Така схема так називаємо внутрішнього випаровування молекул.
Молекули, що випаровуються, переміщуються по міжвузлям кристалічної решітки. Це приводить до порушення її ідеального порядку: у кристалі, окрім молекул, що займають вузли решітки, опиняються рухомі, діслоцировані молекули і вузли, не заповнені молекулами, своє подібні „отвори”. Кількість діслоцированих молекул й „отворів” зростає з підвищенням температури і досягає максимуму при температурі плавлення.
При температурі плавлення середній запас кінетичної енергії молекул стає на стільки великим, а сили Ван-дер-Ваальсу, в наслідок збільшення відстані між молекулами, на стільки ослабшають, що надання речовині нової кількості теплоти переводить молекули з їх стійкого стану у вузлах кристалічної решітки і до нестійкого, й кристалічна структура руйнується.
Незважаючи на те, що кристал і рідина являє собою якісно різні стани речовини, структура і властивості рідини багато в чому подібні структурі й властивостям твердої речовини. При плавленні кристалічної речовини відбувається порівняльне невелике збільшення об’єму (при плавленні тротилу його об’єм збільшується приблизно на 13%, отже відстань між молекулами збільшується не на стільки, щоб могло відбутися корінна зміна у будові речовини). Теплоємкість при плавленні майже не змінюється або збільшується у незначних розмірах. Таким чином, характер теплового руху молекул речовини під час плавлення суттєво не змінюється. При температурі, що не значно перевищує температуру плавлення, рідина здатна витримувати великі розривні зусилля. Рідина володіє текучістю ( як і тротил), це основна особливість відрізняє її від твердого тіла.
2.2 Фізико–хімічні основи процесу кристалізації
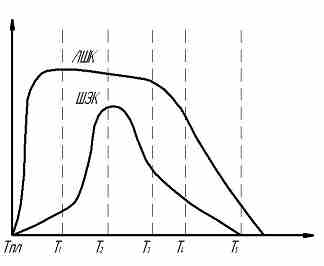
Процес кристалізації вибухових речовин, зокрема тротилу, із розплаву до цього часу вивчена не досить. На основі практичних доглядів можна вважати, що для більшої кількості вибухових речовин, що використовують для заливки, залежність швидкості утворювання центрів кристалізації й лінійної швидкості кристалізації схожа з характером залежності, що відображена на рис.2.1. Крива ШЗЦ досягає максимуму пізніше ніж крива ЛШК, і йде на знижування раніше, ніж крива ЛШК.
Як що такі речовини кристалізувати при повільному охолодженні, щоб Т досягло такого ж значення, при якому ЛШК вже досягла свого максимуму, а ШЗЦ ще має незначну величину (Т1), то виходять крупно кришталеві виливки. Якщо кристалізацію вести при охолодженні, достатнього для того, щоб на протязі всього процесу підтримувати величину Т на рівні, відповідному максимуму ШЗЦ (Т2), то при цьому вийде виливка з дрібнокристалічною структурою.
 |
Рисунок 2.1 – Залежність швидкості створення центрів кристалізації (ШЗЦ) і лілейної швидкості кристалізації (ЛШК) від переохолодження
При ще більш скорішому охолодженні, достатньому для підтримки величини Т на рівні, що відповідає Т3 або Т4 виходять дрібно кришталеві виливки. Якщо охолодженні вести на стільки швидко, щоб кристалізація йшла при температурі Т5, то виливка буде мати аморфну структуру з вкрапленими до неї окремими кристалами. Таким чином, спів подання або близькість положень максимуму обох кривих речовини легко кристалізується, і її важко або не можливо отримати при охолоджуванні розплаву в аморфному стані.
Кристалізація тротилу починається при зрівняло невеликому переохолодженні. При охолодженні розплавленого тротилу в металевому бачку ємкістю 60л при безперервному перемішуванні дерев’яним веслом зміна температури розплаву відбувається приблизно так, як це зображено на кривої залежності температури від часу змішування на рис 1.2. Такий хід охолодженні тротилу можливо пояснити тим, що при температурі до 79,4oС швидкість утворення центрів кристалізації практично дорівнює нулю. Починаючи з 97,4oС, коли T досягає величини приблизно 10С, крива ШЗЦ йде доверху, кристалізація починається і, в наслідок виділення схованої теплоти кристалізації, температура вибухової речовини швидко підвищується до температури затвердження.
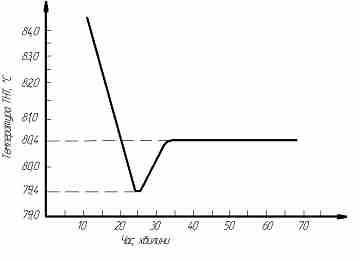 |
Рисунок 2.2 – Крива охолодження тротилу при перемішуванні
При повільному охолоджуванні розплавленого тротилу виходять виливки з крупно кришталевою структурою. Це пояснюється тим, що при малих значеннях Т швидкість створення центрів кристалізації мізерно мала. Тротил у мілко кристалічному стані може бути отримано при дуже швидкому охолодженні, тобто в умовах кристалізації при великих Т.
Якщо холодну металеву пластинку занурити в розплав тротилу, то в результаті швидкого переохолоджування на її поверхні утвориться тонкий шар дрібно кришталевого тротилу. Однак отримати таким шляхом розривні заряди з дрібно кришталевою побудовою неможливо через нездійсненність досить швидкого охолодження розплаву, залитого в камору.
Будівля виливки, отриманої з розплавленого і залитого у холодну оболонку тротилу, при чому виникає велика кількість центрів кристалізації, утворюючих тонкий шар дрібно кришталевого тротилу. Але при подальшому виділенні схованої теплоти кристалізації, мала теплоємкість вже створеної корки твердого тротилу і швидке збільшення температури оболонки приводять до зростання температури розплаву і його Т стає недостатньої для утворення нових центрів кристалізації.
Швидкість росту грані кристалу пропорційна коефіцієнту теплопровідності кристалу у напрямку, перпендикулярно зростаючої грані, а також градієнту температури і назад пропорційно схованої теплоті кристалізації і площини кристалу.
Отже, швидше зростають ті кристали, напрямок максимальної теплопровідності яких співпадає з напрямком від стінки оболонки до геометричної осі обертання розривного заряду. Ці кристали швидко випереджують своїх сусідів, лишають їх можливості подальшого росту і розповсюджуються по розплаву у вигляді стовпиків, що перпендикулярні поверхні охолодження. Таким чином, виходить заряд крупнокришталевої побудови з невеликим, прилягаючий безпосередньо до стінки оболонки, шаром, створеним з дрібних безпорядковоорієнтованих кристалів.
Для отримання дрібнокристалічних розривних зарядів високої щільності і достатньої механічної міцності, розплавлена вибухова речовина до заливки її в камору БП або якийсь виріб насичують такою кількістю центрів кристалізації, якої достатньо для утворення дрібнокристалічної побудови навіть у тому випадку, якщо затвердження її буде проходити без утворення нових центрів кристалізації. Насичення розплаву центрами кристалізації є задачею підготовки вибухової речовини до заливки [2].
3 МЕТОДІКА ДОСЛІДЖЕННЯ
3.1 Виготовлення розплаву
3.1.1Виготовлення розплаву в плавителях
Для плавки тротилу використовуються апарати трьох видів: плавильний казан Михайлова, змієвиковий плавник безперервної дії і конічний плавник.
Плавильний казан Михайлова є мідний лужоний сосуд полусферічної форми 1 із хромонікілевої сталі, постачений паровою сорочкою 2 (рис.3.1).
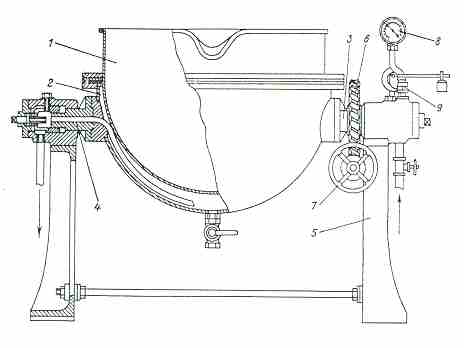 |
Рисунок 3.1 – Плавильний казан Михайлова
У сорочці, яка також має форму полусфери, є дві цапфи 3 і 4. Казан опирається на чавунні стійки 5. На цапфі 4 закріплена шестерня черв’ячної передачі 6, за допомогою якої обертаючи штурвал 7, казан при зливу з нього розплавленого тротилу можна нахиляти під будь-яким кутом. Підведення пари здійснюється через цапфу 3, а відвід конденсату – через цапфу 4. Для спостереження за тиском пари, що надходить у сорочку плавника, казан має манометр 8. При плавки тротилу тиск пару повинен бути не більш 1,5атм. Щоб виключити можливість випадкового підвищення тиску пари вища цього рівня, плавник має запобіжний клапан 9. Для прискорення плавки тротилу його треба систематично перемішувати веслом. Переваги цього плавильного казану у порівнянні з плавниками іншого типу: придатний для плавки не лише однорідних вибухових речовин, але й для сумісного плавлення різних компонентів, що утворюють сплави, а також для виготовлення сумішів. Плавники інших систем використовуються тільки для плавки тротилу; плавильний казан легко містити в чистоті; можливість утворення місцевих перегрівів менше, ніж в інших плавниках.
Недоліки плавильного казана Михайлова: мала продуктивність. Казан ємкістю 500л дає приблизно 1500кг плавленого продукту у шестигодинну зміну; великі затрати ручного труда, тому що необхідно постійно перемішувати розплав; підвищена шкідливість для робочих.
Через вказані недоліки плавильні казани Михайлова у даний час майже повністю витиснуті з виробництва плавниками інших типів.
Змієвиковий плавник безперервної дії (рис.3.2) являє собою залізний
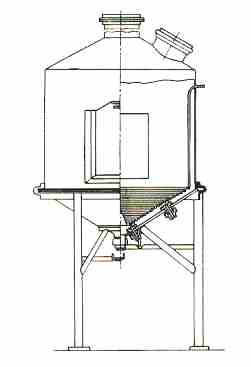 |
Рисунок 3.2 – Змієвиковий плавник безперервної дії
циліндр з конічним дном. Усередині апарату біля дна встановлені зміїве-ки з алюмінієвих труб, котрі обігріваються паром при тиску в 1,5атм. У дні апарату зроблений отвір для стоку розплавленої вибухової речовини, а в кришці є загруз очний люк і відвід для видалення пару і газу, що виділяються при плавленні.
Змієвиковий плавник володіє рядом переваг у порівнянні з плавильним казаном Михайлова. Продуктивність змієвикового плавника безперервної дії значно вище. Змієвиковий плавник діаметром 1200мм дає до 1000кг плавленого тротилу в час. При плавленні не потрібне систематичне перемішування розплавленого тротилу.
Головний недолік цього апарату полягає в тому, що його дуже важко промивати та очищувати.
Найчастіше ж використовується плавник Комісарова. Конічний плавник Комісарова (рис. 3.3) виготовляють з 4-5мм заліза
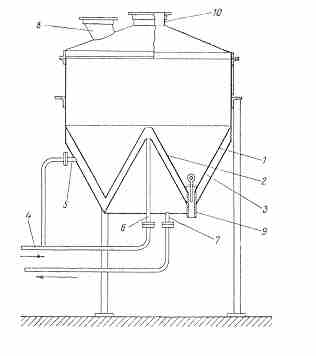 |
Рисунок 3.3 – Конічний плавник Комісарова
або хромонікілєвої сталі. Гріюча поверхня цього плавника являє собою сполучення двох конусів – великого зовнішнього 1 і малого внутрішнього 2. Ця поверхня обогрівається паровою сорочкою 3. Пар до цієї сорочки надходить паропроводом 4 через патрубки 5 і 6 (температура пари 110-115 0С). Конденсат відводиться через патрубок 7. Завантажений у плавник тротил під дією сили ваги попадає між гріючими поверхнями великого і малого конусів плавника. Розплав тротилу вільно витікає крізь зливний штуцер 9. Крізь патрубок 10 плавник поєднаний з витяжною вентиляцією. Тиск пару, який надходить до сорочки плавнику, повинен бути не більш 1,6 кг*с/см¬2 (0,6мПа). Для збросу надлишкового тиску на трубопроводі встановлений запобіжний клапан, який відрегульований на тиск 0,14мПа [6].
Перевага цього плавника у тому, що протягом усього часу плавлення зберігається безпосередній контакт матеріалу що плавиться з усією поверхню плавника. Цим конічний плавник Комісарова вигідно відрізняється від плавильного котла Михайлова, в якому тепло від гріючої поверхні до тротилу, що плавиться, надходить головним чином через розплав, що зменшує теплопередачу в декілька разів. Конічний плавник Комісарова має високу продуктивність. На відміну від змієвикового плавника, конічний плавник Комісарова не має труднощів в очищенні [1].
3.1.2 Виготовлення розплаву в лабораторних умовах
Виготовлення розплаву в лабораторних умовах передбачає підготовчу роботу, що пов’язана з переводом технологічного потоку з заводських умов на лабораторні. Тому робочими речовинами обираємо парафін та петролатум, виходячи з їх властивостей (є найменш небезпечними та мають температуру плавлення меншу ніж 100 оС), та в якості основного обладнання - водяну баню.
Водяна баня складається з електричної плити, на яку встановлюється ємкість з кольорового металу наповнену водою. В воду поміщаємо скляну ємкість, в яку послідовно будуть поміщатися навіски з речовин для їх подальшого плавлення. Поряд з плитою встановлюємо штатів з лапкою-держателем, в яку розміщуємо термометр, розрахований на вимірювання температури до 100 оС.
Порядок виконання роботи:
Починаємо процес з розбивання парафіну та зважування його на навіски 100г, 200г, 300г,400г на технічних вагах. В цей же час на нагріту електричну плитку встановлюють ємкість з водою та нагрівають її до температури 100 оС (температура кипіння води), після чого встановлюють в кипящу воду ємкість з першою навіскою 100г. Ведучи спостереження за процесом плавлення, фіксуємо час повного розплавлення навіски та температуру розплаву у цей момент. Таким же чином розплавляємо навіски, що залишилися.
Повторюємо весь процес для речовини – петролатума.
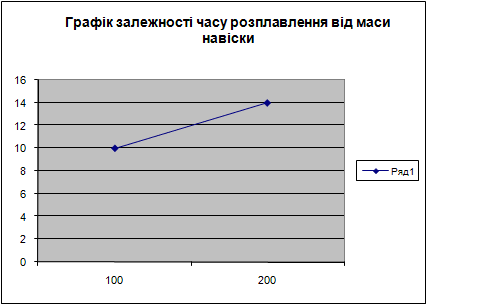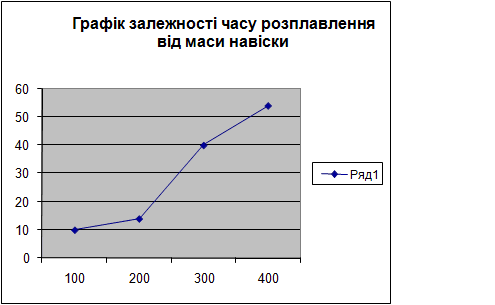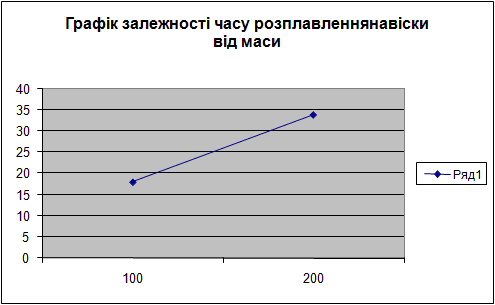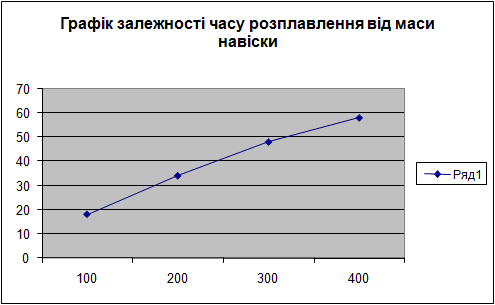 |
Кількість кадрів – 6, Кількість повторів – 10
3.2 Кристалізація розплаву
3.2.1 Виробництво лускуйок тротилу
Утилiзований тротил привозять зi складу або майстернi рознарядження цеху №1 або №5 у витрачальний погрибок автомашиною або трактором з причепом. Мiшки з тротилом розвантажують на вiзки ( не бiльш 12 мішкiв на вiзок по 30 кг). У по грибку мішки з ТНТ кладуть на дерев’яний полист у штабелi попартiйно.
З витрачального погрибка мiшки з тротилом транспортують до майстернi виготування ДПУ-830 Тл за допомогою пiдвисноi дороги. Пiдвисна дорога являє собою монорельс , який змонтований на стойках на висотi 2-3 м вiд грунту. Рух люльки по монтажу здійснюється за допомогою стального тросу, який приводиться у рух за допомогою електродвигуна. У погрибку мішки з тротилом навантажують на візок, у процесі перевіряють цільність мішків та наявність маркирування. Маркірування повинно бути чітким і містити: позначення продукту, номер партії, маса нетто, дату пакування. Візки встановлюють на люльку підвесної дороги фіксують гальмованим устаткуванням і транспортують до майстерні у відділ підготовки продукту до плавки. Транспорту- вання здійснюється полу автоматично, тобто контролювання руху люлькі здійснюється робітником на кінцевої стійки підвісної дороги. У приміщені приготування розплаву кожен мішок з тротилом проходять вхідний контроль (на цільність мішків, на зовнішній вигляд тротилу ( на відсутність сторонніх предметів та слідів забруднення)). З мішків тротил висипають у алюмінієвий ковш. Завантаження ковша не більш 80 кг. Якщо будуть виявлені признаки примочки тротилу, тоді буде додатковий розгляд майстера відділу технічного контролю, і такий продукт не допускається.
Тротил з ковша за допомогою пневматичної талі завантажують у пла вник Комісарова (250–300 кг). В міру розплавлювання тротил з плавника по перехідній трубі зливають у змішувач. Температура розплаву у змішувачі в момент початку злива тротилу повинна бути 80–85oС. Коли рівень розплаву у змішувачі досягне 20–25 см від верхнього торця завантажувального люка, подачу розплаву припиняють ( рівень перевіряють візуально через завантажувальний люк), перекидну трубу встановлюють над люком порожнього змішувача та процес повторюють. У змішувачі розплав тротилу підігрівають до температури 82–90oС при вимкнутої мішалки.
При досягненні розплаву необхідної температури, люк змішувача зачиняють кришкою з гумовою прокладкою, затягують "барашки" кришки за допомогою латунного прудка, та подають стисле повітря ( Р=0.11 мПа). Після відчинення проміжного клапану, розплав по масопроводу чере фільтр пересувається у проміжну ємкість (рівень розплаву у ємкості дорівнює 15–25 см від кришки), після цього подачу повітря у змішувач припиняють, знімають кришку з люка, зачиняють проміжний клапон. Змішувач готовий до приготування нової порції розплаву.
Лускуювання тротилу – особливо небезпечна операція. Вона відбувається на барабані лускування шляхом його соскаблювання з циліндричних та торцевих поверхонь барабану, що обертається. Цей барабан нижньою частиною занурений у розплавленний тротил, залитий у корито.
Включаємо подачу холодної води(температура не більш 25oС) у кожух барабана та горячої води (температура 84-98оС) -у кожух масопровода та корита. Потім відкриваємо клапан поживний, розплав тнт із ємкості почне поступати у корито барабану лускування до рівня 20 см. Закриваємо клапан. При подальшій роботі барабана лускування поживний клапан відкривається та зачиняється автоматично. Температура лускуйки не перевищує 50oС, якщо відбувається спекання 40о С, тоді потрібно знизити швидкість обертів барабану. Температура тротилу в кориті на 5-6oС вища температури плавління тротилу.
На тічку барабана одягаємо паперовий мішок і зажимаємо його пневмоциліндрами так, щоб при наповненні мішка він стояв на платформі вагів. При заповненні мішка тротилом, перекриваємо тічку заслонкою, відєднюємо мішок від тічки та зважуємо(вага мішка повинна бути 30 кг). Мішок прибираємо з вагів і ставимо на платформу. мішки на машину навантажуємо за допомогою стрічкового транспортеру.
3.2.2 Виробництво ДПУ
Приготування заливочної маси, для виготовлення литих зарядів і детонаторів ДПУ-830 Тл, виробляється у змішувачі для виготовлення шимазованого розплаву, який розташований у відділі заливки. Шимазований розплав складається з розплаву тротилу і його лускуйки.
Загрузла лускуйки тротилу у змішувач здійснюється по тічки через сіто (діаметр сітки складає 10мм). Перед початком праці перевіряють тем- пературу води у рубашці змішувача (tв=84-98oС), потім зачиняють промі- жний клапан на масопроводі подачі роплаву у барабан лускування і від- кривають проміжний клапан на масопроводі подачі розплаву у змішувач. При досягненні рівня розплаву в змішувачі приблизно 1/3-1/2 висоти баку (перевіряють через загрузочний люк змішувача за допомогою дерев’яного весла), перекривають проміжний клапан на маслопроводі , включають мішалку і додають лускуйки тротилу через тічку у змішувач ( загрузка лу- скуйки здійснюється невеликими порціями приблизно по 30-35кг ). При безперервному обертанні мішалки відбувається змішування маси до отри- мання однорідності. Час приготування заливочної маси складає 30-40 хвилин, а температура заливочої маси повинна бути 81-85oС ( допускається знижувати температуру заливочної маси за допомогою добавки нової порції лускуйки).Готовність маси визначається візуально, люк змішу вача зачиняють кришкою з гумковою прокладкою, закривають клапан ви тяжної вентиляції, надів на ручку ричага клапана противагу (5кг).В запобіганні опіків рук, роботу виробляють у рукавицях. По сигналу (заливщіці) подають у змішувач стисле повітря (початковий тиск стислого пові- тря 0,15-0,20 мПа , потім знижується і залишається постійним 0,03-0,08 мПа). Стисле повітря у змішувач подається за доповогою вентиля, який ро- зташован на повітряводі. Заливочна маса надходить до розливного клапану по масопроводу.
Перші розплавлені порції маси зливають у ведро, і відправляють на кристалізацію. Потім наливається маса заливки у спеціальне ведро, для визначення її готовності (готовність визначається за допомогою визначення діаметру розтікаємості , у якого припустимий боковий вівтар густоти складає 34-38 сантіметрів). Одбирати пробу безпосередньо із змішувача не допускається.
При отриманні задовільного результату перевірки густоти маси, робиться заливка детонаторів. Заливка виконується у заливочний іструмент, який складається із верхнього та нижнього фланців. На нижній фланець встановлюється оболонка для детонатора, потім на штирь нижнього фланця надівається пресована шашка із A-IX-I, потім надівається верхній фланець на оболонку. Після встановлювання заливочного інструменту, відкривається кран заливочного клапану і виконується зали- вка у футляр через вікна центрующої втулки. Наповнив футляр до рівня приблизно 40-60мм від зрізу, клапан закривається. Час витримки 3-5хв.,пі- сля виробляється доливка.Все це здійснюється разом з виховуванням розплаву у оболонках. Наповнення виконується до нижнього торця фланця. Час витримки залитого детонатора складає 10–15 хв. Після чого виконується розборка заливочного інструменту, його чистка та чистка детонаторів від залишків тротилу.
Детонатори після заливки йдуть на контроль якості. Контроль вико- нується по вазі, по зовнішньому вигляду, по проходженню калібр-пробки. Після контролю разом з кришкою детонатори відправляють на мар- кірування. Маркировка наноситься окремо на паперовий вкладиш. Вкладиш кріпиться до детонатора за допомогою надягання кришки на оболо- нку. Маркировка детонатора повинна містити: номер партії, рік виготов- влення, заводський номер детонатора. Також повинна бути маркировка на кришці детонатора при її виготовленні, і має містити: марку детонатора „ДПУ-830 Тл”, товарний знак або умовне позначення підприємство-виготовлювача [5].
Після маркировки детонатори йдуть на укупорку. Упаковуються детонатори у гафрированні ящики (по 24шт.). Вага кожного ящика з дето- наторами не більш 25кг. Детонатори вкладаються у ящик вертикально або горизонтально, щільно рядами (стінки ящику і проміжок між рядами запо- внюють макулатурою). Після вкладення детонаторів у ящик, кладеться паперова прокладка, закривається ящик за допомогою металевих клапанів і ліпкої стрічки (ширина стрічки 60-100мм). Перед заклеюванням ящика по місту стику ящика вставляють власне клеймо пакувальника. На бокової стороні ящика наклеюють ярлики: з одного боку – маркировка, з другого – знак небезпеки [7].
Готову продукцію відвозять на склад за допомогою автомашини або трактора з причепом. Загрузка у транспорт здійснюється за допомогою стрічкового конвеєра [3].