Биография

Автореферат
Библиотека
Ссылки
Отчет о поиске
Мир фотошопа

Биография |
 |
RUS | |||||||||||||||||||
Автореферат |
|||||||||||||||||||||
Библиотека |
UKR | ||||||||||||||||||||
Ссылки |
|||||||||||||||||||||
Отчет о поиске |
ENG | ||||||||||||||||||||
Мир фотошопа |
|||||||||||||||||||||
| Портал магистров ДонНТУ | ДонНТУ | |||||||||||||||||||||
 |
|||||||||||||||||||||
Колбаса Виктория Александровна |
|||||||||||||||||||||
Факультет: Экологии и химической технологии |
|||||||||||||||||||||
Кафедра: Химическая технология топлива |
|||||||||||||||||||||
Специальность: Химическая технология топлива и углеродистых материалов |
|||||||||||||||||||||
Тема выпускной работы: |
|||||||||||||||||||||
Исследование процесса извлечения сероуглерода из головной фракции сырого бензола |
|||||||||||||||||||||
Научный руководитель: к.т.н., доцент Крутько Ирина Григорьевна |
|||||||||||||||||||||
Реферат по теме выпускной работы |
|||||||||||||||
|
Введение 1 Аналитический обзор литературных материалов 1.1 Способы очистки сырого бензола от сероуглерода 1.2 Анализ методов переработки сероуглеродной фракции 2 Изучение физико-химических основ процесса извлечения сероуглерода из головной фракции сырого бензола 2.1 Свойства, получения и применения основных компонентов головной фракции сырого бензола 2.2 Методика проведения экспериментальных исследований 2.3 Методы анализа исходных реагентов и продуктов реакции 2.4 Химизм реакции взаимодействия сероуглерода с аммиаком 3 Результаты опытов Выводы Перечень ссылок |
|||||||||||||||
ВведениеВ процессе высокотемпературного коксования угольной шихты в коксовой камере вместе с коксом образуются летучие химические продукты, которые являются сложной неоднородной системой, которая состоит из газообразных и парообразных веществ, которые являются продуктом термического разложения каменного угля. Сырой бензол - продукт, который извлекается из коксового газа каменноугольным поглотительным маслом. Существуют сернокислотный метод и метод каталитической очистки сырого бензола от сернистых соединений, в результате которых происходит выделение сероуглеродной (головной) фракции. Одним из распространенных методов переработки головной фракции есть метод термической полимеризации, который имеет значительные недостатки. Поэтому на данное время актуальной является разработка новых методов очистки и переработки сероуглеродной фракции, а также выделение из нее чистых продуктов (например, тиомочевины или роданистого аммония и др.). Цель работы: исследование физико-химических основ извлечения сероуглерода из головной фракции сырого бензола путем связывания его химическими реагентами с получением ценных химических продуктов, безопасных при хранении, использовании и транспортировке. Актуальность работы:
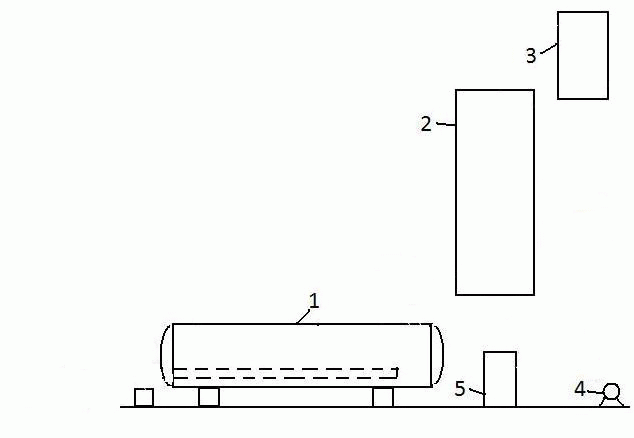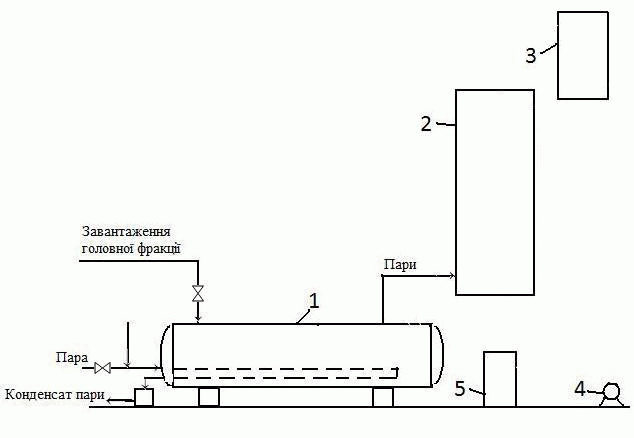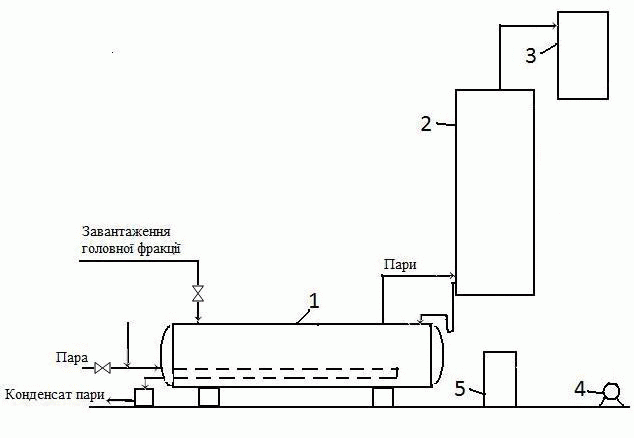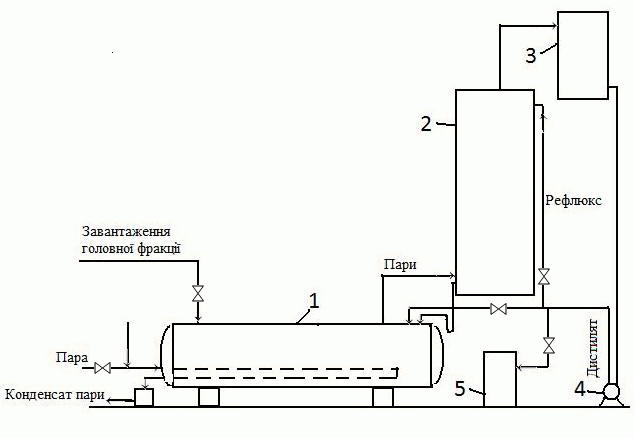
Объект работы: головная фракция сырого бензола. 1 Аналитический обзор литературных материалов1.1 Способы очистки сырого бензола от сероуглерода Сырой бензол извлекается из прямого коксового газа абсорбцией органическими поглотителями. Сырой бензол является сложной смесью химических (ароматических) соединений, главными из которых являются бензольные углеводороды (бензол и его гомологи), их содержание составляет 80–90 %. Как примеси в сыром бензоле содержатся ненасыщенные и сернистые соединения, фенолы, пиридиновые основания и др. При улавливании бензольных углеводородов из коксового газа поглотительными маслами в сыром бензоле содержатся легкие погоны поглотительного масла и нафталин [1]. Сернистые соединения сырого бензола являются вредными примесями и бензольные продукты от них должны быть освобожденные в процессе переработки. Наличие в сыром бензоле сернистых соединений исключает возможность непосредственного получения из него чистых продуктов без предыдущей очистки. Высокие требования по очистке предъявляются к бензольным продуктам, которые применяются для органического синтеза. Обусловлено это тем, что даже незначительные примеси серы в бензоле и толуоле, которые применяются для органических синтезов, вызывают быстрое отравление катализатора. В этой связи переработка сырого бензола должна проводиться таким образом, чтобы бензольные продукты не содержали сернистых соединений или же содержали их в очень незначительных количествах, при которых исключено их вредное влияние в процессе производства синтетических продуктов. Среди всех методов химической очистки бензольных углеводородов наиболее распространенным является сернокислотный метод. Преимуществами метода являются легкость управления процесса, который обеспечивает получение нужной степени очистки, простота и дешевизна. Недостатком метода является образование отхода производства – кислой смолки. В настоящее время широкое распространение получила очистка методом каталитического гидрирования, которая позволяет получить глубокую степень очистки без отходов производства. Сернокислотная очистка сырого бензола от непредельных и сернистых соединений проводится в специальных моющих аппаратах периодического или непрерывного действия. Химизм процесса гидроочистки заключается в том, что серосодержащие примеси гидрируются с образованием соответствующих углеводородов и сероводорода; азотосодержащие вещества дают аммиак и углеводороды; вещества, которые содержат кислород – углеводороды и воду. Ненасыщенные соединения обогащаются [1]. Метод каталитической гидроочистки дает возможность получать безсернистые продукты, но он значительно удорожает процесс переработки сырого бензола в результате больших капиталовложений и увеличение эксплуатационных расходов. Рентабельность процесса достигается благодаря большему выходу чистых продуктов и их большей ценности [2,3]. Сернокислотный метод нуждается в меньших капитальных затратах и меньших эксплуатационных расходах, но связан с потерями бензольных углеводородов и образованием нежелательных отходов производства – кислой смолки. Независимо от выбранного метода очистки сначала выделяют сероуглеродную фракцию сырого бензола, которая хранит ресурсы смолообразующих для производства полимерных смол дает возможность использовать сероуглеродную фракцию для получения сероуглерода и циклопентадиена. Процесс выделения сероуглеродной фракции осуществляется в ректификационной колонне с выносными подогревателями термосифонного типа. Первый бензол из хранилища непрерывно подается через фильтр на тарелку питания головной (сероуглеродной) колонны, в которой головная фракция отделяется от остатка бензол – толуол – ксилол (БТК). В укрепляющей части колонны должно быть обеспечено полное отделение бензола от головной фракции, поскольку бензол, который остался в главной фракции, практически не используется. Пары сероуглеродной фракции поступают из колонны в конденсатор-холодильник, откуда образовавшийся конденсат попадает в сепаратор для выделения воды, а затем в рефлюксный бачок. Из последнего часть обезвоженной головной фракции отводится на состав, но основная часть в виде рефлюкса подается на верхнюю тарелку колонны. В дальнейшем сероуглеродная фракция поддается переработке. Выход головной фракции 2 – 3 % от переработанного сырья. Состав сероуглеродной фракции зависит от условий ректификации и состава исходного сырого бензола. В зависимости от условий отбора головной фракции изменяется содержание ее наиболее высококипящего компонента — бензола. Содержание последнего в головных фракциях разных заводов составляет от 3—5 % до 50 %. Соответственно этому изменяется содержание остальных компонентов, в частности самых основных, — сероуглерода и циклопентадиена [3]. 1.2 Анализ методов переработки сероуглеродной фракции В состав головной фракции входят следующие компоненты: сероуглерод, циклопентадиен, легкокипящие ненасыщенны соединения (амилены) и насыщенные углеводороды, бензол. Головная фракция, которая получается непрерывной ректификацией сырого бензола, является желтой, неприятно пахнущей жидкостью. В настоящее время переработка головной фракции почти исключительно проводится методом термической полимеризации. Весьма распространенная раньше система сернокислотной очистки головной фракции в настоящий момент уже почти не применяется, поскольку приводит к образованию значительных количеств кислого смоления, очень большого теплового эффекта реакции из-за значительного содержания непредельных соединений, а следовательно, и к разогреванию загрузки и большим потерям. Большой тепловой эффект процесса приводит к необходимости очень медленной подачи кислоты, которая длится иногда всю смену, и к осуществлению процесса ступенчатой промывки — сначала слабой, потом более крепкой кислотой с проведением дистилляции между ними. Однако и в этих случаях потери сероуглерода продолжали оставаться весьма значительными, а непредельные соединения переводились в бесполезный отход производства — кислое смоление. Все эти обстоятельства привели к тому, что процесс сернокислотной очистки был вытеснен методом термической полимеризации, хотя последний в свою очередь также имеет значительные недостатки [2]. Впервые в промышленности процесс термической полимеризации головной фракции был осуществлен цехом ректификации Макеевского коксохимического завода. По этому способу (рис. 1.1) головная фракция загружается в куб ректификации, в котором, благодаря подогреву, происходит полимеризация циклопентадиена в димер, а также его полимеризация с некоторыми другими непредельными соединениями. Продукты, которые не полимеризуются и выделяются, конденсируются и возвращаются в куб. По окончании процесса полимеризации при тщательной дефлегмации начинают отбор дистиллята, причем отбирают легкую фракцию, технический сероуглерод, промежуточные фракции. В кубе в виде остатков ректификации остаются полимеры, которые являются более или менее концентрированной дициклопентадиеновой фракцией. |
|||||||||||||||
 |
|||||||||||||||
|
Рисунок 1.1 – Схема установки для термополимеризации и ректификации головной фракции: Длительность процесса термической полимеризации головной фракции — от 12 до 24 часов и зависит преимущественно от состава фракции. При проведении полимеризации непрерывно меняется состав загрузки в результате образования полимеров, а также потери легкокипящих углеводородов через воздушник. Целесообразно процесс полимеризации проводить по возможности быстро, чтобы уменьшить неминуемые потери сероуглерода через воздушник. Окончание процесса полимеризации определяется по прекращению изменения состава загрузки куба, который характеризуется обычным разгоном. 2 Изучение физико-химических основ процесса извлечения сероуглерода из головной фракции сырого бензола2.1 Свойства, получения и применения основных компонентов головной фракции сырого бензола В процессе ректификации сырого бензола выделяется головная фракция. В состав головной фракции входят такие компоненты:
Состав головной фракции зависит от условий ее отбора, а также от состава исходного сырого бензола. При наилучших условиях переработки сырого бензола I средний состав головной фракции характеризуется следующими данными % [1]: Выход головной фракции небольшой и колеблется в пределах 2-3 % от сырья, которое перерабатывается. Близость температур кипения сероуглерода и циклопентадиена (42.5 и 46.5 0С) при приблизительно одинаковом их содержании в головной фракции весьма затрудняет выделение концентрированной сероуглеродной фракции одной лишь ректификацией. Поэтому при переработке головной фракции использовано важнейшее свойство одного из основных компонентов – циклопентадиена – легко полимеризоваться с образованием димера – циклопентадиена – углеводорода, кипящего при 166.6 0С, причем процесс полимеризации циклопентадиена в дициклопентадиен происходит не только при повышении температуры, но и самопроизвольно. Чистый сероуглерод является почти бесцветной, сильно преломляющей жидкостью с эфирным, неприятным запахом; относительная плотность 1,262 г/см3 (при 20 °С), температура кипения 46 °С. Технический сероуглерод владеет неприятным запахом редьки. Пары сероуглерода загораются при чрезвычайно низкой температуре (236 0С), в результате чего это вещество очень огнеопасно [5,6]. Сероуглерод замечательно растворяет жиры и другие органические вещества, благодаря чему он находит значительное применение как растворитель. В очень больших количествах сероуглерод потребляется в производстве вискозного искусственного волокна. Сероуглерод достаточно ядовит, особенно для низших животных. Он применяется для уничтожения вредных насекомых (например, для борьбы с вредителем виноградной лозы — филлоксерой) [7]. Циклопентадиен представляет собой бесцветное легкодвижущее вещество, которое при -85 0С застывает в кристаллическую массу. Температура кипения 41 0С, растворяется в этаноле, диэтиловом эфире, бензоле, не растворяется в воде. Циклопентадиен владеет химическими свойствами диеновых углеводородов. Легко присоединяет галогены, галогеноводороды и др. Циклопентадиен – реакционное соединение благодаря наличию соединенных двойных связей. Циклопентадиен легко полимеризуется, скорость полимеризации при повышении температуры растет [8]. Циклопентадиен применяют для получения инсектицидов (альдрин, изодрин и другие), металоценов, циклопентана, циклопентена, гексахлорциклопентадиена и др. Существуют большие возможности использования циклопентадиена для синтеза препаратов со свойствами лекарственных веществ с цветочным запахом. Дициклопентадиен, который является димером циклопентадиена, образуется в головной фракции в результате полимеризации циклопентадиена. Дициклопентадиен представляет собой бесцветные кристаллы с резким запахом, растворяется в органических растворителях. Легко присоединяет H2, H2O, галогены, карбоновые кислоты. Полимеризация циклопентадиена происходит уже при комнатной температуре; при температуре около 100 °С процесс значительно ускоряется. При последующем повышении температуры, вместе с развитием обратной реакции (деполимеризации дициклопентадиена) ускоряются реакции образования высших полимеров — тримеров и даже тетрамеров. Чистый дициклопентадиен является кристаллическим веществом белого цвета. Существуют два пространственных изомера дициклопентадиена: α – форма с температурой плавления 32,9 °С и β – форма с температурой плавления 19,5 °С [9]. Произвольная полимеризация циклопентадиена в дициклопентадиен приводит к тому, что со временем состав головной фракции и характеристика ее разгона значительно будут изменяться. При хранении головной фракции содержание циклопентадиена в ней уменьшается, а дициклопентадиена увеличивается. Соответственно растет и плотность фракции [10]. Свойство циклопентадиена образовывать димер с резко отличающейся от остальных всех компонентов температурой кипения головной фракции послужила основой для его выделения. Получаемый дициклопентадиен одно время использовался для производства суррогата олифы, которая получается окислением дициклопентадиена. Свойство дициклопентадиена деполимеризоваться в циклопентадиен позволяет получать последний в достаточно чистом виде для использования его как сырье для производства инсектицида. Бензол - родоначальник углеводородов ароматического ряда. Представляет собой бесцветное вещество с характерным запахом, температура кипения 80,1 0С. Неограниченно растворяется в углеводородах, эфирах, хуже - в метаноле, не растворяется в этиленгликоле, глицерине; растворяет жиры, каучуки, гудрон, серу, фосфор, йод. Образует азеотропные смеси [5]. Для бензола характерная стойкость к действию высоких температур и окислителей. Бензол не изменяется под действием Н2CrO4 и КMnO4, из О2 в присутствии катализаторов (V, Мо) при 350 – 450 °С образует малеиновый ангидрид. Гидрируется до циклогексана в присутствии разных катализаторов. Щелочными металлами в жидком NH3 возобновляется до 1,4-циклогексадиена. Наиболее старый метод промышленного получения бензола: выделение его из предварительно охлажденных парогазовых продуктов коксования каменного угля абсорбцией органическими поглотителями, например маслами каменноугольного и нефтяного происхождения. Бензол выделяют также из жидких продуктов пиролиза нефтепродуктов, которые образуются в производстве этилена и пропилена. Основные области применения бензола (больше 80%): производство этилбензола, кумола и циклогексана; остальные - для получения анилина, малеинового ангидрида, как компонент моторного топлива для повышения октанового числа, как растворитель и экстрагент в производстве лаков, красок, ПАВ и др [9]. Амилены (пентены) – низко кипящие вещества, не растворяются в воде, растворяются в этаноле и диэтиловом эфире; образуют азеотропные смеси с метанолом, этанолом, диэтиловым эфиром, ацетоном, ацето-нитрилом и др. Присоединяют по двойной связи H2, галогены, галогеноводороды и т.п.; под действием H2SO4 превращаются в соответствующие амиловые спирты (при этом происходит частичная полимеризация); при нагревании с СО и H2 в присутствии Co2(CO)8 образуют смесь изомерных гексиловых спиртов. В промышленности пентен получает оксосинтезом из СО и H2 в присутствии Со; дегидрированием пентана в присутствии Cr2O3 – Al2O3; дегидратацией амиловых спиртов над Al2O3 при 380-450 0C или при действии 46-65 %-ой H2SO4 при 90-110 0C; пиролизом амилацетатов при 500-700 0C и др. [9]. Насыщенные углеводороды относятся к менее реакционно-способными органическими соединениями, однако они не являются химически инертными. При определенных условиях они вступают в реакции окисления, нитрации, сульфохлорирования и др. В промышленности насыщенные углеводороды получают в составе технических продуктов или выделяются из них при переработке нефти и природного газа, а также угля и горючих сланцев. Смесь разных алканов может быть получена синтезом на основе СО и Н2. Насыщенные углеводороды применяют в составе моторных и реактивных топлив, как сырье для химической и нефтехимической промышленности [9]. 2.2 Методика проведения экспериментальных исследований Для проведения реакции использовали головную фракцию сырого бензола и аммиак 25%-ный водный. В таблице 2.1 приведена характеристика головной фракции. Таблица 2.1 – Характеристика головной фракции |
|||||||||||||||
|
|||||||||||||||
|
Лабораторная установка представляет собой автоклав, который состоит из корпуса и крышки. В корпус вставляется стакан, который закрывается крышкой. В автоклаве есть гайка, которая обеспечивает открытие автоклава. В стакан помещали определенное количество головной фракции сырого бензола и 25%-ного раствора аммиака. Потом стакан помещали в корпус автоклава и плотно закрывали. Автоклав ставили в термостат, нагретый до определенной температуры. Автоклав нагревали до нужной температуры и выдерживали определенное время. После выдержки автоклав помещали на воздух, а затем охлаждали под водой приблизительно 30 минут. После этого смесь, которая находилась в стакане автоклава, перемещали в делительную воронку и разделяли на две фазы: аммиачно-солевой раствор и головную фракцию. 2.3 Методы анализа исходных реагентов и продуктов реакции Для хроматографического определения состава головной фракции сырого бензола и органической фазы после связывания CS2 аммиаком использовали хроматограф с детектором по теплопроводимости Кристалл Люкс – 4000. Условия хроматографирования [11]: Компоненты головной фракции определяются по хроматограмме, которая записывается потенциометром. Основные компоненты смеси проявляются в такой последовательности: легкокипящие (до С8) насыщенные углеводороды; легкокипящие (до С5) ненасыщенные углеводороды; сероуглерод (время удерживания относительно бензола 0,21); циклопентадиен (время удерживания относительно бензола 0,25); н-нонан (время удерживания относительно бензола 0,72); бензол. Опыт считается законченным после того, как пик бензола полностью будет вырисовываться на хроматограмме. В конической колбе с притершей пробкой емкостью 50 мл взвешивают с точностью до 0,0002 г 1 – 1,5 грамма н-нонана, после чего добавляют с точностью до 0,0002 г исследуемой пробы в количестве 10 – 15 грамма. После этого рассчитывается содержание н-нонана в полученной смеси, который должен составлять 10 – 15 % (по массе). Пробу тщательным образом взбалтывают в конической колбе и с помощью микрошприца вводят в хроматограф. Расчет содержания сероуглерода: определение содержания сероуглерода проводится путем сопоставления площадей пиков н-нонана и сероуглерода, которые определяются по хроматограмме. Расчет проводится по следующей формуле [11]: CCS2 = c*SCS2*100/(S*(100-c)*KCS2), где CCS2 – концентрация сероуглерода в головной фракции % (по массе); c – концентрация н-нонана в анализируемой смеси % (по массе); SCS2 – площадь пика сероуглерода, мм2; S – площадь пика н-нонана, мм2; KCS2 – калибровочный коэффициент. На рисунке 2.1 и 2.2 представлены хроматограммы головной фракции сырого бензола до и после исследование соответственно, из которых видно, что содержание сероуглерода уменьшается после проведения опыта.
Рисунок 2.1 – Хроматограма головной фракции сырого бензола до эксперимента
Рисунок 2.2 – Хроматограма головной фракции сырого бензола после эксперимента 2.4 Химизм реакции взаимодействия сероуглерода с аммиаком Процесс взаимодействия сероуглерода и аммиака может идти по разным механизмам в зависимости от условий проведения эксперимента. Схема 1, t ≥ 120°C S медл. || S=C=S + NH2−H ↔ H2N−C−SH (1) дитиокарбаминовая кислота S S || швидк. || NH3 + H2N−C−S−H ↔ H2N−C−S−NH4 (2) дитиокарбаминат аммония S S || || H2N−C−S NH4 → H2N−C−NH2 + H2S (3) тиомочевина _______________________________________ > 120 0С CS2 + 2NH3→ H2NC(S)NH2 + H2S (4) тиомочевина Cхема 2, t = 113°C S медл. || S=C=S + NH2−H ↔ H2N−C−SH (5) H2N−C−SH ↔ HN=C=S + H2S (6) роданистоводородная кислота NH2−H + HN=C=S → NH4S−C≡N (7) роданид аммония __________________________________________ <120 0С S=C=S + NH2−H → NH4S−C≡N + H2S (8) Схема 3. Изомеризация роданида аммония в тиомочевину, t ≥ 160°C S || NH4S−C≡N → H2N−C−NH2 + H2S (9) тиомочевина 3 Результаты опытовБыло исследовано влияние температуры, соотношения реагентов и времени контакта реагентов на степень извлечения CS2 из головной фракции сырого бензола. При увеличении времени контакта (рис. 3.1) степень извлечения CS2 увеличивается. При времени контакта 1 час степень извлечения составляет 85,22 %, при 5 часах – 97,1 %. Оптимальным временами для проведения последующих опытов было принято время – 3 часа. При увеличении отношения сероуглерода и аммиака (рис. 3.2) при постоянной температуре (t=120 0С) степень очистки повышается. При отношении 2:1 степень извлечения составляет 77,34 %, при 7:1 – 99,84 %.
Рисунок 3.1 – Зависимость степени извлечения CS2 от времени контакта головной фракции и аммиака
Рисунок 3.2 – Зависимость степени извлечения CS2 из ГФСБ от изменения
соотношение NH3 : CS2 При повышении температуры (рис. 3.3) степень очистки увеличивается. По результатами опытов видно, что при увеличении температуры в интервале 80 – 160 0С степень извлечения изменяется для пробы 1 от 75,51 до 99,11 %, а для пробы 2 от 91,76 % до 99,99 %. При увеличении температуры для пробы 2 наблюдается незначительное изменение степени извлечения CS2 из ГФСБ. Оптимальную температуру принимаем равной 115 – 120 0С.
Рисунок 3.3 – Зависимость степени извлечения CS2 от температуры Выводы Впервые исследована реакция взаимодействия сероуглерода с аммиаком в смеси ароматических соединений; Установлено, что при увеличении времени контакта степень извлечения CS2 увеличивается. Оптимальное время для проведения последующих опытов было принято равным 3 часа; Установлено, что при увеличении соотношения сероуглерода и аммиака при постоянной температуре (t=120 0С) степень очистки повышается. При молярном отношении NH3 : CS2 = 7:1 достигается практически полное извлечение сероуглерода из органической фазы в водную в форме роданистых соединений. При повышении температуры степень очистки увеличивается. Оптимальную температуру принимаем равной 115 – 120 0С; Показана принципиальная возможность практически полного извлечения сероуглерода из головной фракции методом обработки ее водным раствором аммиака с получением продуктов, которые можно использовать для органического синтеза. При написании данного автореферата магистерская работа еще не завершена. Окончательное завершение - декабрь 2010 г. Перечень ссылок
|
|||||||||||||||
| ДонНТУ | Портал магистров ДонНТУ | Автореферат | Библиотека | Ссылки | Отчет о поиске | Мир фотошопа |