Біографія

Автореферат

Біографія |
 |
RUS | |||||||||||||||||||
Автореферат |
|||||||||||||||||||||
| UKR | |||||||||||||||||||||
| ENG | |||||||||||||||||||||
| Портал магістрів ДонНТУ ДонНТУ | |||||||||||||||||||||
 |
|||||||||||||||||||||
Колбаса Віктория Олександрівна |
|||||||||||||||||||||
Факультет: Екології та хімічної технології |
|||||||||||||||||||||
Кафедра: Хімічна технологія палива |
|||||||||||||||||||||
Спеціальність: Хімічна технологія палива та вуглецевих матеріалів |
|||||||||||||||||||||
Тема випускної роботи: |
|||||||||||||||||||||
Дослідження процесу витягування сірковуглецю з головної фракції сирого бензолу |
|||||||||||||||||||||
Науковий керівник: к.т.н., доцент Крутько Ірина Григорівна |
|||||||||||||||||||||
Реферат з теми випускної роботи |
|||||||||||||||
|
Вступ 1 Аналітичний огляд літературних і патентних матеріалів 1.1 Способи очистки сирого бензолу від сірковуглецю 1.2 Аналіз методів переробки сірковуглецевої фракції 2 Вивчення фізико-хімічних основ процесу витягнення сірковуглецю із головної фракції сирого бензолу 2.1 Властивості, отримання та застосування головних компонентів головної фракції сирого бензолу 2.2 Методика проведення експериментальних досліджень 2.3 Методи аналізу вихідних реагентів та продуктів реакції 2.4 Хімізм реакції взаємодії сірковуглецю з аміаком 3 Результати дослідів Висновки Перелік посилань |
|||||||||||||||
ВступВ процесі високотемпературного коксування вугільних шихт в коксовій камері разом із коксом утворюються летючі хімічні продукти, які є складною неоднорідною системою, що складається з газоподібних і пароподібних речовин, що є продуктом термічного розкладання кам'яного вугілля. Сирий бензол - продукт, який витягується з коксового газу кам'яновугільним поглинаючим маслом. Існують сірчанокислотний метод та метод каталітичного очищення сирого бензолу від сірчастих сполук, в результаті яких відбувається виділення сірковуглецевої (головної) фракції. Одним з поширених методів переробки головної фракції є метод термічної полімеризації, який має значні недоліки. Тому на даний час актуальним є розробка нових методів очищення та переробки сірковуглецевої фракції, а також виділення з неї чистих продуктів (наприклад, тіомочевини або роданистого амонію та ін.). Мета роботи: дослідження фізико-хімічних основ витягнення сірковуглецю із головної фракції сирого бензолу шляхом зв’язування його хімічними реагентами з отриманням цінних хімічних продуктів, безпечних при зберіганні, використуванні та транспортуванні. Актуальність роботи:
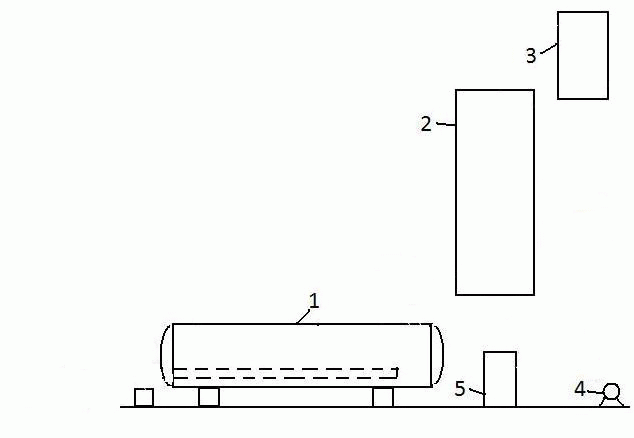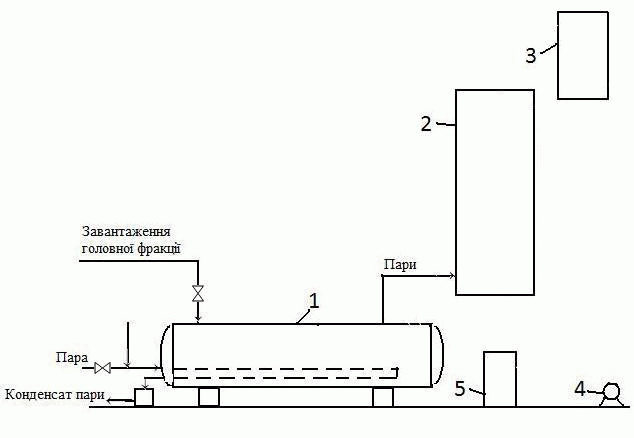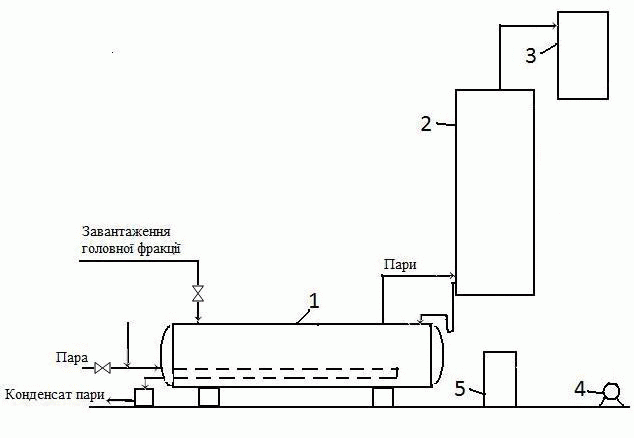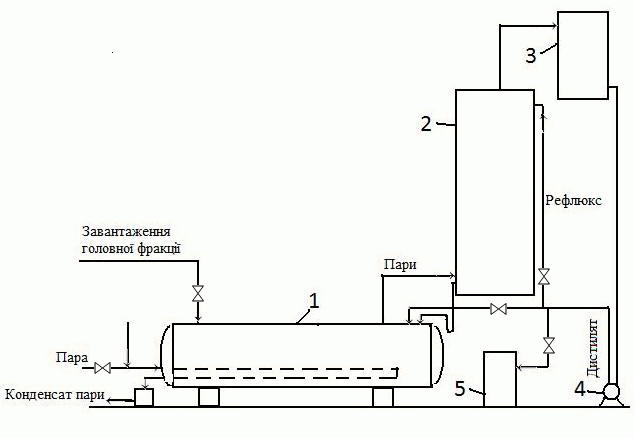
Об’єкт роботи: головна фракція сирого бензолу. 1 Аналітичний огляд літературних матеріалів1.1 Способи очистки сирого бензолу від сірковуглецю Сирий бензол витягується з прямого коксового газу абсорбцією органічними поглиначами. Сирий бензол є складною сумішшю хімічних (ароматичних) сполук, головними з яких є бензолові вуглеводні (бензол і його гомологи), їх зміст складає 80–90 %. Як домішки в сирому бензолі містяться ненасичені та сірчисті сполуки, феноли, піридинові основи і ін. При уловлюванні бензолових вуглеводнів з коксового газу поглинаючими маслами в сирому бензолі містяться легкі погони поглинаючого масла і нафталін. Сірчасті сполуки сирого бензолу являються шкідливими домішками і бензольні продукти від них повинні бути звільнені в процесі переробки. Наявність в сирому бензолі сірчастих сполук виключає можливість безпосереднього отримання з нього чистих продуктів без попередньої очистки. Високі вимоги по очистці пред’являються до бензольних продуктів, що застосовуються для органічного синтезу. Обумовлено це тим, що навіть незначні домішки сірки в бензолі та толуолі, які застосовуються для органічних синтезів, викликають швидке отруєння каталізатора. В зв’язку з цим переробка сирого бензолу повинна проводитися таким чином, щоб бензольні продукти не містили сірчастих сполук або ж містили їх в дуже незначних кількостях, при котрих виключений їх шкідливий вплив у процесі виробництва синтетичних продуктів. Серед усіх методів хімічної очистки бензольних вуглеводнів найбільш поширеним є сірчанокислотний метод. Перевагами метода являються легкість керування процесу, що забезпечує отримання потрібного ступеня очистки, простота і дешивізна. Недоліком метода є утворення відхода виробництва – кислої смолки. У сучасному часі широке поширення отримала очистка методом каталітичного гідрування, яке дозволяє отримати глибоку ступінь очистки без відходів виробництва. Сірчанокислотна очистка сирого бензолу від неграничних та сірчастих сполук проводиться в спеціальних миєчних апаратах періодичної або непреривної дії. Хімізм процесу гідроочистки полягає в тому, що сірковмісткі домішки гідруються з утворенням відповідних вуглеводнів та сірководня; азотовмісткі речовини дають аміак та вуглеводні; речовини, які містять кисень – вуглеводні та воду. Ненасичені сполуки збагачуються [1]. Метод каталітичної гідроочистки дає можливість отримувати безсірчасті продукти, але він значно здорожує процес переробки сирого бензолу внаслідок великих капіталовложень і збільшення експлуатаційних витрат. Рентабельність процесу досягається завдяки більшому виходу чистих продуктів та їх більшій цінності [2,3]. Сірчанокислотний метод потребує менших капітальних затрат та менших експлуатаційних витрат, але пов’язан з втратами бензольних вуглеводнів і утворенням небажаних відходів виробництва – кислої смолки. Незалежно від обраного методу очистки спочатку виділяють сірковуглецеву фракцію сирого бензолу, що зберігає ресурси смолоутворюючих для виробництва полімерних смол дає можливість використовувати сірковуглецеву фракцію для отримання сірковуглецю та циклопентадієну. Процес виділення сірковуглецевої фракції здійснюється в ректифікаційній колоні з виносними підігрівачами термосифонного типу. Перший бензол з хранилища непреривно подається через фільтр на тарілку живлення головної (сірковуглецевої) колони, у якій головна фракція відділяється від залишку бензол – толуол – ксилол (БТК) . У зміцнюючій частині колони повинно бути забезпечено повне відділення бензолу від головної фракції, оскільки бензол, який залишився в головній фракції, практично не використовується. Пара сірковуглецевої фракції поступає із колони до конденсатора-холодильника, звідки утворившийся конденсат потрапляє до сепаратора для виділення води, а потім у рефлюксний бачок. Із останнього частина зневодненої головної фракції відводиться на склад, але основна частина у вигляді рефлюкса подається на верхню тарілку колони. В подальшому сірковуглецева фракція піддається переробці. Вихід головної фракції 2 – 3 % від переробленої сировини. Склад сірковуглецевої фракції залежить від умов ректифікації і складу початкового сирого бензолу. Залежно від умов відбору головної фракції змінюється вміст її найбільш висококиплячого компоненту — бензолу. Зміст останнього в головних фракціях різних заводів складає від 3—5 % до 50 %. Відповідно цьому змінюється вміст решти компонентів, зокрема найосновніших — сірковуглеця і циклопентадієну [3]. 1.2 Аналіз методів переробки сірковуглецевої фракції До складу головної фракції входять наступні компоненти: сірковуглець, циклопентадієн, легкокиплячі ненасичені сполуки (амілени) та насичені вуглеводні, бензол. Головна фракція , яка отримується непреривною ректифікацією сирого бензола, являється жовтою, неприязно пахучою рідиною. В даний час переробка головної фракції майже виключно проводиться методом термічної полімеризації. Вельми поширена раніше система сірчанокислотного очищення головної фракції зараз вже майже не застосовується, оскільки приводить до утворення значних кількостей кислого смоління, дуже великого теплового ефекту реакції із-за значного змісту неграничних сполук, а отже, і до розігрівання завантаження і великих втрат. Великий тепловий ефект процесу приводить до необхідності дуже повільної подачі кислоти, що триває іноді всю зміну, і до здійснення процесу ступінчастої промивки — спочатку слабкою, потім міцнішою кислотою з проведенням дистиляції між ними. Проте і в цих випадках втрати сірковуглеця продовжували залишатися вельми значними, а неграничні сполуки переводилися в даремний відхід виробництва — кисле смоління. Всі ці обставини привели до того, що процес сірчанокислотного очищення був витиснений методом термічної полімеризації, хоча останній у свою чергу також має значні недоліки [2]. Вперше в промисловості процес термічної полімеризації головної фракції був здійснений цехом ректифікації Макіївського коксохімічного заводу. За цим способом (рис. 1.1) головна фракція завантажується в куб ректифікації, в якому, завдяки підігріву, відбувається полімеризація циклопентадієну в димір, а також його полімеризація з деякими іншими неграничними сполуками. Продукти, що не полімеризуються і виділяються, конденсуються і повертаються в куб. Після закінчення процесу полімеризації при ретельній дефлегмації починають відбір дистиляту, причому відбирають легку фракцію, технічний сірковуглець, проміжні фракції. У кубі у вигляді залишків ректифікації залишаються полімери, що є більш менш концентрованою діциклопентадієновою фракцією. | |||||||||||||||
 |
|||||||||||||||
|
Рисунок 1.1 – Схема установки для термополімеризації і ректифікації головної фракції: Тривалість процесу термічної полімеризації головної фракції — від 12 до 24 годин і залежить переважно від складу фракції. При проведенні полімеризації безперервно міняється склад завантаження внаслідок утворення полімерів, а також втрати легкокиплячих вуглеводнів через повітряник. Доцільно процес полімеризації проводити по можливості швидко, щоб зменшити неминучі втрати сірковуглеця через повітряник. Закінчення процесу полімеризації визначається по припиненню зміни складу завантаження куба, що характеризується звичайним розгоном. 2 Вивчення фізико-хімічних основ процесу витягнення сірковуглецю із головної фракції сирого бензолу2.1 Властивості, отримання та застосування головних компонентів головної фракції сирого бензолу В процесі ректифікації сирого бензолу виділяється головна фракція. До складу головної фракції входять наступні компоненти:
Склад головної фракції залежить від умов її відбору, а також від складу початкового сирого бензолу. За найкращих умов переробки сирого бензолу I середній склад головної фракції характеризується наступними даними % [1]: Вихід головної фракції невеликий і коливається в межах 2-3 % від сировини, що переробляється. Близькість температур кипіння сірковуглеця і циклопентадієну (42.5 і 46.5 0С) при приблизно однаковому їх вмісті в головній фракції вельми утрудняє виділення концентрованої сірковуглецевої фракції однією лише ректифікацією. Тому при переробці головної фракції використано найважливішу властивість одного з основних компонентів – циклопентадієну – легко полімеризуватися з утворенням диміра – циклопентадієну – вуглеводня, киплячого при 166.6 0С, причому процес полімеризації циклопентадієну в дициклопентадієн відбувається не тільки при підвищенні температури, але і мимоволі. Чистий сірковуглець є майже безбарвною, сильно заломлюючою рідиною з ефірним, неприємним запахом; відносна щільність 1,262 г/см3 (при 20 °С), температура кипіння 46 °С. Технічний сірковуглець володіє неприємним запахом редьки. Пара сірковуглеця займається при надзвичайно низькій температурі (236 0С), унаслідок чого ця речовина украй вогненебезпечна [5,6]. Сірковуглець чудово розчиняє жири і інші органічні речовини, завдяки чому він знаходить значне застосування як розчинник. У дуже великих кількостях сірковуглець споживається у виробництві віскозного штучного волокна. Сірковуглець досить отруйний, особливо для нижчих тварин. Він застосовується для знищення шкідливих комах (наприклад, для боротьби з шкідником виноградної лози — філоксерою) [7]. Циклопентадієн представляє собою безбарвну легкорухому речовину, яка при -85 0С застигає в кристалічну масу. Температура кипіння 41 0С, розчиняється етанолі, діетіловому ефірі, бензолі, не розчиняється у воді. Циклопентадієн володіє хімічними властивостями дієнових вуглеводнів. Легко приєднує галогени, галогеноводні та ін. Циклопентадієн – реакційна сполука завдяки наявності сполучених подвійних зв’язків. Циклопентадієн легко полімеризується, швидкість полімеризації при підвищенні температури зростає [8]. Циклопентадієн застосовують для отримання інсектицидів (альдрин, ізодрин і інші), металоценов, циклопентану, циклопентену, гексахлорциклопентадієну і ін. Існують великі можливості використання циклопентадієну для синтезу препаратів з властивостями лікарських речовин з квітковим запахом. Діциклопентадієн, що є диміром циклопентадієну, утворюється в головній фракції унаслідок полімеризації циклопентадієну. Діциклопентадієн представляє собою безбарвні кристали з різким запахом, розчиняється в органічних розчинниках. Легко приєднує H2, H2O, галогени, карбонові кислоти. Полімеризація циклопентадієну відбувається вже при кімнатній температурі; при температурі близько 100 °С процес значно прискорюється. При подальшому підвищенні температури, разом з розвитком зворотної реакції (деполімеризації дициклопентадієна) прискорюються реакції утворення вищих полімерів — тримерів і навіть тетрамерів. Чистий діциклопентадієн є кристалічною речовиною білого кольору. Існують два просторові ізомери діциклопентадієна: α – форма з температурою плавлення 32,9 °С і β – форма з температурою плавлення 19,5 °С [9]. Довільна полімеризація циклопентадієну в діциклопентадієн приводить до того, що з часом склад головної фракції і характеристика її розгону значно зміняються. При зберіганні головної фракції вміст циклопентадієну в ній зменшується, а діциклопентадієна збільшується. Відповідно зростає і щільність фракції [10]. Властивість циклопентадієну утворювати димір з різко відмінною від решти всіх компонентів температурою кипіння головної фракції послужила основою для його виділення. Отримуваний діциклопентадієн у свій час використовувався для виробництва сурогату оліфи, що отримується окисленням дициклопентадієна. Властивість діциклопентадієна деполімеризуватися в циклопентадієн дозволяє отримувати останній в достатньо чистому вигляді для використання його як сировина для виробництва інсектициду. Бензол - родоначальник вуглеводнів ароматичного ряду. Представляє собою безбарвну речовину з характерним запахом, температура кипіння 80,1 0С. Необмежено розчиняється у вуглеводнях, ефірах, гірше - в метанолі, не розчиняється у етилгліколі, гліцерині; розчиняє жири, каучуки, гудрон, сірку, фосфор, йод. Утворює азеотропні суміші [5]. Для бензолу характерна стійкість до дії високих температур і окислювачів. Бензол не змінюється під дією Н2CrO4 і КMnO4, з О2 в присутності каталізаторів (V, Мо) при 350 – 450 °С утворює малеїновий ангідрид. Гидрується до циклогексану в присутності різних каталізаторів. Лужними металами в рідкому NH3 відновлюється до 1,4-циклогексадієну. Найбільш старий метод промислового отримання бензолу: виділення його із заздалегідь охолоджених парогазових продуктів коксування кам'яного вугілля абсорбцією органічними поглиначами, наприклад маслами кам’яно-вугільного і нафтового походження. Бензол виділяють також з рідких продуктів піролізу нафтопродуктів, що утворюються в виробництві етилену і пропилену. Основні області застосування бензолу (більше 80%): виробництво етилбензолу, кумолу і циклогексану; решта - для отримання аніліну, малеїнового ангідриду, як компонент моторного палива для підвищення октанового числа, як розчинник і екстрагент в виробництві лаків, фарб, ПАР і ін [9]. Амілени (пентени) – низько киплячи речовини, не розчиняються у воді, розчиняються у етанолі і діетиловому ефірі; утворюють азеотропні суміші з метанолом, етанолом, діетиловим ефіром, ацетоном, ацето-нітрилом і ін. Приєднують по подвійному зв'язку H2, галогени, галогеноводні і т.п.; під дією H2SO4 перетворюються у відповідні амілові спирти (при цьому відбувається часткова полімеризація); при нагріванні із СО і H2 в присутності Co2(CO)8 утворюють суміш ізомерних гексилових спиртів. У промисловості пентени отримують оксосинтезом із СО і H2 в присутності Со; дегідруванням пентана в присутності Cr2O3 – Al2O3; дегідратацією амілових спиртів над Al2O3 при 380-45O 0C або при дії 46-65%-вої H2SO4 при 90-110 0C; піролізом амілацетатів при 500-700 0C і ін. [9]. Насичені вуглеводні відносяться до менш реакційноздібних органичних сполук, проте вони не є хімічно інертними. За певних умов вони вступають в реакції окислення, нітрації, сульфохлорування і ін. У промисловості насичені вуглеводні отримують у складі технічних продуктів або виділяють з них при переробці нафти і природного газу, а також вугілля і горючих сланців. Суміш різних алканів може бути отримана синтезом на основі СО і Н2. Насичені вуглеводні застосовують у складі моторних і реактивних палив, як сировина для хімічної і нафтохімічної промисловості [9]. 2.2 Методика проведення експериментальних досліджень Для проведення реакції використовували головну фракцію сирого бензолу і аміак 25%-вий водневий. У таблиці 2.2 приведена характеристика головної фракції. Таблиця 2.1 – Характеристика головної фракції | |||||||||||||||
Лабораторна установка представляє собою автоклав, який складається з корпуса і кришки . В корпус вставляється стакан , що закривається кришкою . В автоклаві є гайка, яка забезпечує відкриття автоклава. У стакан помістили певну кількість головної фракції сирого бензолу і 25%-вого розчину аміаку. Потім стакан помістили в корпус автоклава і щільно закрили. Автоклав ставили в термостат, нагрітий до певної температури. Автоклав нагрівали до потрібної температури і витримували певний час. Після витримки автоклав помістили на повітря, а потім охолоджували під водою приблизно 30 хвилин. Після цього суміш, яка знаходилася в стакані автоклава, переміщали в ділильну воронку і розділяли на дві фази: аміачно-сольовий розчин і головну фракцію. 2.3 Методи аналізу вихідних реагентів та продуктів реакції Для хроматографічного визначення складу головної фракції сирого бензолу та органічної фази після зв'язування CS2 аміаком використовували хроматограф з детектором за теплопровідністю Кристал Люкс – 4000. Умови хроматографування [11]: Компоненти головної фракції визначаються за хроматограмою, яка записується потенціометром. Основні компоненти суміші проявляються в такій послідовності: легкокиплячі (до С8) насичені вуглеводні; легкокиплячі (до С5) ненасичені вуглеводні; сірковуглець (час удержування відносно бензолу 0,21); циклопентадієн (час удержування відносно бензолу 0,25); н-нонан (час удержування відносно бензолу 0,72); бензол. Дослід вважається закінченим після того, як пік бензолу повністю вималюється на хроматограмі. До конічної колби з притертою пробкою ємкістю 50 мл зважують з точністю до 0,0002 г 1 – 1,5 г н-нонана, після чого додають з точністю до 0,0002 г досліджуваної проби в кількості 10 – 15 г. Після цього розраховується вміст н-нонана в отриманій суміші, який повинен складати 10 – 15 % (за масою). Пробу ретельно збовтують в конічній колбі та за допомогою мікрошприца вводять до хроматографа. Розрахунок вмісту сірковуглеця: визначення вмісту сірковуглеця проводиться шляхом зіставлення площей піків н-нонана і сірковуглеця, які визначаються за хроматограмою. Розрахунок проводиться за наступною формулою [11]: CCS2 = c*SCS2*100/(S*(100-c)*KCS2), де CCS2 – концентрація сірковуглеця у головній фракції, % (за масою);c – концентрація н-нонана в аналізуючий суміші, % (за масою); SCS2 – площа піка сірковуглеця, мм2; S – площа піка н-нонана, мм2; KCS2 – калібровочний коефіцієнт. На рисунку 2.1 та 2.2 представлені хроматограми головної фракції сирого бензолу до і після дослідження відповідно, з яких видно, що вміст сірковуглецю зменшується після проведення досліду.
Рисунок 2.1 – Хроматограма головної фракції сирого бензолу до експерименту
Рисунок 2.2 – Хроматограма головної фракції сирого бензолу після експерименту 2.4 Хімізм реакції взаємодії сірковуглецю з аміаком Процес взаємодії сірковуглеця і аміаку може йти по різних механізмах залежно від умов проведення експерименту. Схема 1, t ≥ 120°C S медл. || S=C=S + NH2−H ↔ H2N−C−SH (1) дітіокарбамінова кислота S S || швидк. || NH3 + H2N−C−S−H ↔ H2N−C−S−NH4 (2) дітіокарбамінат амонию S S || || H2N−C−S NH4 → H2N−C−NH2 + H2S (3) тіомочевина _______________________________________ >120 0С CS2 + 2NH3→ H2NC(S)NH2 + H2S (4) тіомочевина Cхема 2, t = 113°C S медл. || S=C=S + NH2−H ↔ H2N−C−SH (5) H2N−C−SH ↔ HN=C=S + H2S (6) роданистоводнева кислота NH2−H + HN=C=S → NH4S−C≡N (7) роданід амонию __________________________________________ <120 0С S=C=S + NH2−H → NH4S−C≡N + H2S (8) Схема 3. Ізомеризація роданіду амонию в тіомочевину, t ≥ 160°C S || NH4S−C≡N → H2N−C−NH2 + H2S (9) тіомочевина 3. Результати дослідівБуло досліджено вплив температури, співвідношення реагентів та часу контакту реагентів на ступінь витягування CS2 з головної фракції сирого бензолу. При збільшенні часу контакту (рис. 3.1) ступінь витягування CS2 збільшується. При часі контакту 1 година ступінь витягування складає 85,22 %, при 5 годинах – 97,1 %. Оптимальним часом для проведення подальших дослідів був прийнятий час – 3 години. При збільшенні відношення сірковуглеця і аміаку (рис. 3.2) при постійній температурі (t=120 0С) ступінь очищення підвищується. При відношенні 2:1 ступінь витягнення складає 77,34 %, при 7:1 – 99,84 %.
Рисунок 3.1 – Залежність ступеня витягнення CS2 від часу контакту головної
фракції та аміаку
Рисунок 3.2 – Залежність ступеня витягнення CS2 з ГФСБ від зміни
відношення NH3 : CS2 При підвищенні температури (рис. 3.3) ступінь очищення збільшується. За результатами дослідів видно, що при збільшенні температури в інтервалі 80 – 160 0С ступінь витягнення змінюється для проби 1 від 75,51 до 99,11 %, а для проби 2 від 91,76 % до 99,99 %. При збільшенні температури для проби 2 спостерігається незначна зміна ступеня витягнення CS2 з ГФСБ. Оптимальну температуру приймаємо рівною 115 – 120 0С.
Рисунок 3.3 – Залежність ступеня витягнення CS2 від температури Висновки Вперше досліджена реакція взаємодії сірковуглецю з аміаком у суміші ароматичних сполук; Установлено, що при збільшенні часу контакту ступінь витягнення CS2 збільшується. Оптимальний час для проведення подальших дослідів був прийнятий рівним 3 години; Установлено, що при збільшенні відношення сірковуглеця і аміаку при постійній температурі (t=120 0С) ступінь очищення підвищується. При мольному відношенні NH3:CS2 = 7:1 досягається практично повне витягнення сірковуглецю із органічної фази до водної в формі роданистих сполук. При підвищенні температури ступінь очищення збільшується. Оптимальну температуру приймаємо рівною 115 – 120 0С. Показана принципова можливість практично повного витягування сірковуглецю з головної фракції методом обробки її водним розчином аміаку з отриманням продуктів, які можна використовувати для органічного синтезу. При написанні данного автореферату магістерська робота ще не завершена. Остаточне завершення - грудень 2010 р. Перелік посилань
|
|||||||||||||||
| ДонНТУ | Портал магістрів ДонНТУ | Автореферат |