УДК 661.8, 678.02
ИЗВЛЕЧЕНИЕ СЕРОУГЛЕРОДА ИЗ ГОЛОВНОЙ ФРАКЦИИ СЫРОГО БЕНЗОЛА РАСТВОРОМ АММИАКА. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОЙ И ВОДНОЙ ФАЗ
Авторы: И.Г. Крутько, А.В. Кипря (ДонНТУ), А.С. Комаров (ЗАО «Донсталь»).
Источник: Наукові праці Донецького національного технічного університету. Серія: Хімія і хімічна технологія. - 2011. - Вип.17 (165). Научный интернет–журнал
Исследован состав и свойства продуктов, получаемых при обработке головной фракции сырого бензола водным раствором аммиака. Рассмотрен химизм процесса, исследовано влияние температуры на состав продуктов реакции в органической и водной фазах.
Ключевые слова: головная фракция сырого бензола, сероуглерод, аммиак, автоклав, циклопентадиен, дициклопентадиен.
Досліджено склад і властивості продуктів, діставаємих при обробці головної фракції сирого бензолу водним розчином аміаку. Розглянуто хімізм процесу, досліджено вплив температури на склад продуктів реакції в органічній та водній фазах.
Ключові слова: головна фракція сирого бензолу, сірковуглець, аміак, автоклав, циклопентадієн, діциклопентадієн.
Сырой бензол, получаемый в процессе коксования каменных углей, подвергается дальнейшей переработке для получения чистых продуктов. Схема переработки включает стадию предварительной ректификации, обеспечивающую отделение низкокипящих и высококипящих сернистых и непредельных соединений. Получаемая при этом смесь низкокипящих компонентов называется головной, или сероуглеродной фракцией. Выход головной фракции составляет 2,0-3,5 %. На предприятиях, перерабатывающих бензол, полученный из сернистых донецких углей, головная фракция содержит, %: 20-35 сероуглерода, 15-35 циклопентадиена, 20-50 бензола, 2-5 дициклопентадиена, до 10 непредельных (олефины C5H10) и до 4,0 насыщенных соединений (циклопентан и гомологи, пентан, гептан).
Сероуглерод и циклопентадиен обладают близкими температурами кипения (42,5 и 46,5°С соответственно) поэтому их практически невозможно разделить только ректификацией [1,2].
Для переработки головной фракции промышленное применение нашел метод термической полимеризации. Такой способ переработки головной фракции сырого бензола требует громоздкого оборудования, больших затрат времени и энергии, пожаро- и взрывоопасен. Процесс сопровождается большими (до 30 %) потерями сероуглерода, бензола, циклопентадиена, сырьем для получения которых является в данном случае каменный уголь – невозобновляемый сырьевой ресурс [3]. Упомянутые вещества являются весьма токсичными, попадая в атмосферу, они наносят вред окружающей среде.
Использование водного раствора аммиака в качестве химического реагента для извлечения сероуглерода из головной фракции сырого бензола позволит устранить приведенные выше недостатки, характерные для метода термической полимеризации [3]
Взаимодействие головной фракции с водным раствором аммиака целесообразно проводить в автоклаве, т.к. повышение давления благоприятно влияет на реакцию:
CS2 + 2NH3 → NH4SCN + H2S (1)
Кроме того, для связывания выделяющегося сероводорода требуется избыток аммиака:
H2S + 2NH3 → (NH4)2S (2)
Суммарное уравнение реакции при избытке аммиака:
CS2 + 4NH3 → NH4SCN + (NH4)2S (3)
Определение состава и свойств продуктов, полученных при контакте аммиака и головной фракции сырого бензола, необходимо для дальнейшей разработки способов их переработки. Поэтому в лабораторных условиях провели экспериментальные исследования, в которых использовали:
головную фракцию сырого бензола состава, %: CS2 – 32,9; циклопентадиен – 0,9; дициклопентадиен – 33,1; бензол – 25,6; легкие компоненты (непредельные, алканы, циклоалканы) – 7,5.
водный раствор 25 %-го аммиака.
Мольное соотношение NH3:CS2 = 5:1. Время контакта 3 часа. Температуру изменяли в интервале 85-160°С.
Несмотря на то, что аммиак и сероуглерод находятся в разных фазах (водной и органической), реакция их взаимодействия является гомогенной поскольку при t=85-160°С протекает в газовой фазе.
Однако после охлаждения полученной реакционной смеси продукты реакции распределяются между двумя фазами: водной и органической.
При взаимодействии аммиака с сероуглеродом можно получить роданид аммония, тиомочевину, дитиокарбаминат аммония, сульфид аммония [3]. Эти вещества, в основном, концентрируются в водной фазе. Состав водной фазы в зависимости от температуры представлен в таблице 1.
Таблица 1 – Состав водной фазы
|
№ п/п |
t, °С |
Содержание, % |
Степень превращения CS2 в NH4SCN, % |
|||
|
Роданид аммония |
Сернистые соединения в пересчете на сульфид аммония |
|||||
|
расчетное |
эксперимен тальное |
расчетное |
эксперимен тальное |
|||
|
1 |
85 |
13,8 |
9,3 |
12,3 |
16,9 |
67,4 |
|
2 |
100 |
16,1 |
11,3 |
14,3 |
18,0 |
70,2 |
|
3 |
115 |
17,6 |
14,9 |
15,6 |
19,4 |
84,7 |
|
4 |
160 |
18,3 |
14,8 |
16,3 |
11,9 |
80,9 |
Анализ состава водной фазы показал, что экспериментально найденное значение содержания роданида аммония меньше рассчитанного по реакции (3). Причем повышение температуры с 85 до 115°С способствует протеканию этой реакции, что подтверждается возрастанием степени превращения сероуглерода в роданид аммония с 67,4 до 84,7 %.
Неполное превращение сероуглерода при контакте с аммиаком в роданид свидетельствует о том, что часть сероуглерода взаимодействует с аммиаком с образованием либо тиомочевины по реакции
CS2 + 2NH3 → (NH2)2CS + H2S, (4)
либо дитиокарбамината аммония
CS2 + 2NH3 → H2NCS2NH4. (5)
Снижение степени превращения сероуглерода в роданид аммония при 160°С связано скорее всего с омылением последнего по реакции:
NH4SCN
+ H2O
![]() 2NH3
+ COS
(6)
2NH3
+ COS
(6)
или с изомеризацией его в тиомочевину.
Содержание сернистых соединений в водной фазе в пересчете на сульфид аммония при температуре 85-115°С превышает расчетное значение (табл.1), что можно объяснить присутствием в растворе других сернистых соединений (тиомочевины, дитиокарбамината аммония и др.).
Не исключено, что заниженные результаты получены вследствие изменения состава водной фазы при хранении, поскольку сульфид аммония является неустойчивым соединением и на воздухе окисляется, образуя полисульфиды. Одновременно может образовываться тиосульфат аммония по реакции:
6NH4OH + 4S → (NH4)2S2O3 + (NH4)2S + 3H2O (7)
Резкое снижение концентрации сульфида аммония при t=160°С может быть результатом изменения механизма протекающих реакций, что требует дополнительного изучения.
Состав органической фазы определяли хроматографическим методом. Результаты приведены в таблице 2.
Таблица 2 – Состав органической фазы
|
№ опыта |
t, °С |
Содержание, % |
|||||||||
|
CS2 |
Бензол |
ЦП |
ДЦП |
легкие |
Общее |
||||||
|
расч. |
эксп. |
расч. |
эксп. |
расч. |
эксп. |
расч. |
эксп. |
эксп. |
|||
|
1 |
85 |
10,6 |
34,1 |
33,5 |
1,20 |
0,04 |
44,0 |
43,8 |
10,1 |
6,2 |
94,14 |
|
2 |
100 |
5,8 |
36,0 |
36,4 |
1,27 |
0,07 |
46,6 |
45,6 |
10,3 |
6,9 |
94,77 |
|
3 |
115 |
2,1 |
37,4 |
36,8 |
1,31 |
0,07 |
48,4 |
46,6 |
10,8 |
7,3 |
92,87 |
|
4 |
160 |
0 |
38,2 |
44,2 |
1,34 |
0,44 |
49,3 |
19,4 |
11,3 |
6,7 |
70,74 |
Органическая фаза после извлечения сероуглерода представляет собой смесь бензола, дициклопентадиена (ДЦП), легких компонентов (непредельные и насыщенные), циклопентадиена (ЦП) и непрореагировшего сероуглерода. Плотность 0,880 г/см3.
Концентрация бензола при отсутствии потерь должна увеличиваться пропорционально количеству извлеченного сероуглерода, так как в условиях опытов бензол не участвует в химических превращениях. Это согласуется с экспериментальными значениями для температур 85-115 °С (табл.2). По-другому ведут себя циклопентадиен и дициклопентадиен.
Циклопентадиен – циклический диен – вследствие сопряженных двойных связей обладает высокой реакционной способностью. Циклопентадиен самопроизвольно переходит в димерную форму, которую легко можно перевести в мономер по схеме
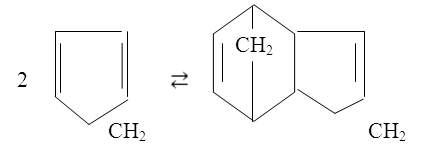 (8)
(8)
Состав равновесной смеси циклопентадиен – дициклопентадиен сильно зависит от температуры. С повышением температуры до 100°С скорость димеризации циклопентадиена резко возрастает. Процесс может не останавливаться на стадии образования димера по реакции (8), а идти дальше при температуре выше 100°С [1]:

Таблица 3 – Зависимость содержания циклопентадиена и дициклопентадиена от температуры
|
№ опыта |
t, °С |
Содержание ЦП+ДЦП, % |
Степень полимеризации ЦП, % |
Обнаруженное количество ЦП+ДЦП по отношению к исходному количеству, % |
|
|
расч. |
эксп. |
||||
|
1 |
85 |
45,2 |
43,84 |
96,7 |
97,0 |
|
2 |
100 |
47,87 |
45,67 |
94,5 |
95,4 |
|
3 |
115 |
49,71 |
46,67 |
94,6 |
93,9 |
|
4 |
160 |
50,64 |
19,84 |
67,2 |
39,2 |
Как можно видеть из
табл.3 степень димеризации циклопентадиена при повышении температуры
с 85 до 160°С
понижается с 96,7 до 67,2 %, что свидетельствует об интенсификации
обратной реакции деполимеризации дициклопентадиена в мономер (реакция
8). Одновременно в интервале температур 85-115°С наблюдается
уменьшение содержания суммы циклопентадиена и дициклопентадиена с
97,0 до 93,9 %, а при t=160°С обнаруженное количество
циклопентадиена и дициклопентадиена падает до 39,2 %. Объяснить это
можно протеканием в автоклаве процессов более глубокой полимеризации
циклопентадиена и дициклопентадиена по реакции 9 в тример, тетрамер,
а также образованием полимерных продуктов диенового синтеза
циклопентадиена с олефинами. Косвенным подтверждением этого может
служить уменьшение количества легких компонентов (табл.2) в
органической фазе.
Таким образом, исследование состава водной и органической фаз, полученных в результате взаимодействия водного раствора аммиака с головной фракцией, показало, что в данной системе протекают сложные физико-химические процессы. Характер и направление этих процессов зависят в значительной мере от температуры. Это обстоятельство следует учитывать при оптимизации технологических параметров извлечения сероуглерода из головной фракции.
Коляндр Л.Я. Новые способы переработки сырого бензола. – М.: Металлургия, 1976. – 192 с.
Коляндр Л.Я. Переработка сырого бензола. – Харьков: Металлургиздат, 1960. – 320 с.
Крутько И.Г., Кипря А.В., Колбаса В.А., Комаров А.С., Сацюк К.А. Физико-химические основы извлечения сероуглерода из головной фракции сырого бензола химическим методом // Наукові праці Донецького національного технічного університету. Серія: Хімія і хімічна технологія. – Донецьк: ДВНЗ «ДонНТУ», 2010. – Випуск 14 (162) – С. 85 – 90.