Реферат
Приведено автоматическое компьютерное толко- вание рентгеномаммограмм. Представлены методы компьютерной интерпретации рентгеномаммограмм. Показана высокая чувствительность программ автоматической диагностики в обнаружении звездчатых образований и кластеров микрокальцинатов.
Ключевые слова: маммограммы, компьютерная интерпретация, кластеры микрокальцинатов.
Предполагается, что в программах скрининга рака молочной железы (РМЖ) рентгенологи пропускают около 25% случаев рака, которые оказываются различимыми при контрольных исследованиях [3]. Более того, если принять во внимание минимальные признаки, ретроспективно выявляемые на маммограммах, то этот показатель повышается до 50% в зависимости от субъективности критериев, используемых при ретроспективном анализе. Проблема ошибок при скрининге должна также рассматриваться в свете требуемой высокой специфичности. Например, в Дании только 4–5 женщин из 1000 болеют РМЖ, тогда как положительное предсказательное значение на сегодняшний день составляет 55%. С учетом минимальной выраженности многих признаков РМЖ, краткости времени, затрачиваемого радиологом на чтение маммограмм, и необходимости чтения всех случаев двумя специалистами данная проблема приобретает особое значение.
Часть проблемы незамеченных образований лежит в области неадекватного их поиска [15]. Если неявная патология, например небольшое скопление микрокальцинатов, не располагается внутри образования, оно легко может быть пропущено. Тем не менее ретроспективно при чтении рентгенограмм органов грудной клетки и маммограмм было установлено, что многие просмотренные специалистом патологические очаги привлекали к себе больше внимания, чем нормальные области [8]. Эти данные свидетельствуют о том, что механизмы восприятия деталей также играют важную роль. Кроме того, около половины ошибок при скрининге относятся к погрешностям интерпретации, т.е. злокачественные образования неправильно трактуются как доброкачественные.
Оцифровка маммограмм позволяет использовать компьютерную обработку изображений для выявления микрокальцинатов, очагов уплотнения и звездчатых образований. Данные программы могут обозначать подозрительные области, значительно уменьшая при этом количество ошибок. Данный подход признан удовлетворительным во многих исследованиях [1, 7]. Тем не менее ни одно из этих исследований не привело к каким-либо значимым результатам, способным повысить эффективность скринига, где доля патологических случаев составляет несколько процентов.
Другой подход к компьютерной оценке маммограмм заключается в помощи рентгенологу при интерпретации характера очага. При этом большинство исследований в этой области направлено на дифференциальную диагностику скоплений микрокальцинатов.
Оцифровка маммограмм производится с использованием цифровых дигитайзеров на основе рентгеновских фотопленок, полученных традиционным способом. Необходимо помнить, что программы часто не очень устойчивы в оценке изображений, полученных из различных источников. Каждая система имеет свои собственные характеристики по передаче шума и контраста, расположению меток и маркеров. Последнее провоцирует дополнительные проблемы, и наиболее простой путь их решения — адаптация программы к кон- кретному аппарату. Методы выявления патологических очагов на маммограммах можно дифференцировать на два основных. В первом случае программа позволяет оценить уровень подозрительности регулярно расположенных точек по всей молочной железе (МЖ), во втором — разделить всю МЖ на области, а затем для каждой из них определить уровень подозрительности.

Рис. 1. Этапы автоматического выявления кластеров микрокальцинатов: исходное изображение (I), первичная оценка после усреднения шума (II), когда кальцинаты остаются белыми, а все остальные точки — черными (III), удаление точек, вероятность которых быть кальцинатами минимальна (IV).
Все методы выявления микрокальцинатов основаны на использовании одного или более фильтров, определяющих локальный контраст каждой точки области интереса, обычно соответствующей всей МЖ. Микрокальцинаты имеют высокий контраст. Однако встречаются и другие структуры с высоким контрастом, например стенки сосудов и тонкие прослойки соединительной ткани. Кроме того, не может быть отдифференцирован от микрокальцинатов и шум. Таким образом, только отбор точек с высоким контрастом не может быть методом выявления микрокальцинатов, поскольку дает слишком много ложноположительных заключений. При автоматизированном распознавании используются разные методы. На первой стадии обработки часто определяются области, подозрительные на наличие микрокальцинатов, а во второй стадии удаляются ложноположительные сигналы “шума” с использованием математических моделей, отображающих распределение “шума” в ткани МЖ.
Метод, разработанный нами, представлен на рис. 1. На стадии предпроцесинга “шум” определяется как функция интенсивности сигнала, позволяющая конвертацию маммограмм в “серую шкалу” с известным постоянным уровнем шума. Такое усреднение шума позволяет значительно упростить последующий анализ [5], поскольку делает алгоритм распознавания менее зависимым от методики получения изображения. При обработке изображения рассчитывается локальный контраст в двух проекциях и выдается значение, позволяющее оценить линейный контур образования. С помощью данного алгоритма можно расценивать все точки как фон, эмульсию (конвертируется в черный цвет) и микрокальцинаты (белые). Данный процесс обладает высокой чувствительностью, поскольку можно определить истинные кальцинаты. Затем исключаются ложные микрокальцинаты, когда оценивается вероятность данной точки быть частью микрокальцината, выявляемая числом других микрокальцинатов, расположенных рядом. Пример данной оценки представлен на рис. 2.
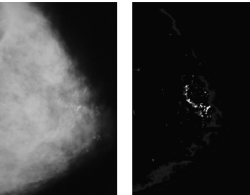
Рис. 2. Пример автоматического выделения кластера микрокальцинатов.
В большинстве случаев, пропущенных при рентгенографическом скрининге, отмечается наличие объемного образования [3], и данный признак является наиболее важной маммографической находкой при инвазивном РМЖ. Такие образова- ния часто обнаруживаются с трудом, будучи прикрытыми фиброзной тканью, особенно при малых размерах опухоли.
Компьютерной обработкой присутствия образования занимались многие группы исследователей. Lau и Bischof [9], Ng и Bischof [12] пытались определить наличие объемного образования путем сравнения яркости и особенностей текстуры в соответствующих областях правосторонней и левосторонней маммограмм. Регистрация осуществлялась путем прикрепления трех контрольных меток на коже МЖ и соске и двух — на грудной стенке. Разработана методика выявления объемных образований, основанная на субтракции левой и правой маммограмм после автоматической их синхронизации. Потенциально подозрительные области обнаруживались на субтракционных изображениях и классифицировались в зависимости от особенностей последних. Было получено от 90% истинно положительных результатов для образований более 2 мм, до 30% для опухолей около 1 см при уровне ложноположительных заключений около 2 ложных опухолей на одно изображение. Miller и Astley [10] изучали проблему выявления асимметрии плотности паренхимы, установив, что в основе получения ложноположительных результатов лежит неадекватная регистрация. В большинстве случаев рентгенологи сравнивают плотность паренхимы правой и левой МЖ по квадрантам. Поскольку в большинстве случаев РМЖ локализуется в железистой ткани и может быть легко ею скрыт, рентгенологи часто специально определяют форму железистого диска. Исследователи пытались дифференцировать жировую и нежировую ткани и выявить асимметрию формы железистой ткани в обеих МЖ. Brzakovic et al. [2] описали алгоритм определения очагов на основе непрерывной логики. В тесте из 12 изображений, содержащих объемное образование неправильной формы, в 8 случаях программа его обозначила точно. Ложноположительных заключений зафиксировано не было. Petrik et al. [13] добились улучшения контрастирования контура образования после введения контрастных веществ.
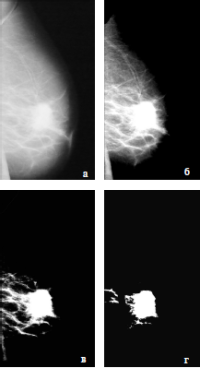
Рис. 3. Автоматическое выявление звездчатых структур. Тень грудной мышцы на маммограмме (а) убирается, снижается интенсивность сигнала подкожнойобласти (б). Выявляются яркие зоны (в), для которыхзатем определяется спикулизация. Яркие пятна соответствуют звездчатым областям (г).
Большинство злокачественных образований имеет неровный контур и часто окружено радиальными спикулами. В некоторых случаях центральная плотность снижена или отсутствует. Kegelmeyer et al. [7] описали метод выявления звездчатых образований, основанный на анализе гистограмм ориентации контура образования. Данные обоих методов суммировали с использованием дерева двоичных решений для оценки принадлежности точки к норме или патологии. Такой алгоритм кажется более эффективным по сравнению с другим, описанным Wood и Bowyer [16]. Аналогичная методика была разработана и нами на основе статистического анализа карты ориентации линий. Идея в общем состоит в том, что подозрительной считается любая область, в которую направлено много точек, особенно если такое повышение плотности прослеживается в различных направлениях. Подсчеты проводились внутри области МЖ, затем рядом расположенные зоны с высоким уровнем подозрительности объединялись с образованием подозрительных областей. Перед расчетом с изображения удаляли фон и затенение грудной мышцы на косых маммограммах. Пример такого преобразования показан на рис. 3б. Данный этап представляет собой удаление грудной мышцы и снижение интенсивности сигнала рядом с кожей. Такое изображение используется в качестве исходного для выявления ярких областей (рис. 3в). После обнаружения таких областей окружающие ткани анализируются на предмет наличия спикулизации.
Ориентацию точек оценивали с использованием методики, основанной на теории градуированного пространства Гаусса. При наличии линейной структуры для данной точки метод позволяет точно установить ее ориентацию, тогда как шум дает случайные значения. После этого два оператора определяют радиальные направления прямых линий. Первое соответствует общему числу точек, сходящихся в интересующем направлении. Если данное количество превышает значение случайного фона, образованного значениями хаотично расположенных линий, то данная область признается подозрительной. Однако если увеличение количества точек ориентировано только в нескольких направлениях, то данное образование вряд ли может быть центром звездчатой структуры. Вместе с тем, если спикулы расходятся во многих направлениях, последнее повышает вероятность наличия звездчатой структуры. Для оценки данной составляющей должен быть второй оператор, определяющий однонаправленность карты ориентации. На рис. 3г представлен пример выявления звездчатых образований, расположенных внутри гистологически верифицированного злокачественного узла.
Чувствительность программ автоматической диагностики в обнаружении звездчатых образований и кластеров микрокальцинатов достаточно высока при приемлемой частоте ложноположительных заключений. При оценке асимметрии плотности диагностическая ценность таких программ несколько ниже. Так, при одном ложноположительном очаге/изображении частота истинно положительных заключений для образований диаметром от 8 до 14 мм составляет всего 30%. Аналогичные данные приводятся и для образований неизвестных размеров [13]. Для очагов микрокальцинатов и звездчатых образований чувствительность и специфичность составляют 90%. Для сравнения: положительное предсказательное значение в 20% случаев и частоту ошибок в 0,5% [4] стандартно показывают рентгенологи, читающие маммограммы при скрининге РМЖ, выдавая в среднем 20 ложноотрицательных результатов на 1000 случаев. Это соответствует значению в 0,01 ложноположительных заключений/изображений с учетом того, что в каждом случае оцениваются 2 маммограммы, снятые в косой проекции. Таким образом, диагностическая ценность программ и заключений рентгенологов находятся на различных уровнях, однако необходимо заметить, что рентгенологи часто проводят дифференциальную диагностику выявленных очагов, исключая явно доброкачественные.
Литература
- Astley S., Hutt I., Adamson S. et al. Automation in mammography: computer vision and humen perception // Proc. 1st International Workshop on Digital Mammography. SPIE. — 1993. — Vol. 1905. — P. 716–730.
- Brzakovic D., Brzakovic P., Neskovic M. An approach to automated screening of mammograms // Proc. 1st International Workshop on Digital Mammography. SPIE. — 1993. — Vol. 1905. — P. 690–701.
- Dijk J.A.M. van Verbeek L.M., Hendriks J.H.C.L., Holland R. The current detectability of breast cancer in a mammographic screening program // Cancer. — 1993. — Vol. 76, N6. — P. 1933–1938.
- Fletcher S.W., Black W., Harris R. et al. Report of the international workshop on screening for breast cancer // J. Natl. Cancer Inst — 1993. — Vol. 85. — P. 1644–1656.
- Karssemeijer N. Adaptive noise equalization and detection of microcalcification clusters in mammography // Int. J. Patt. Recogn. Art. Intell. — 1993. — Vol. 7. — P. 1357–1367.
- Kegelmeyer W.P., jr., Allmen M.C. Dense feature maps for detections of calcifications // Digital mammography / A.G.Gale (ed.) — Elsevier, 1994. — Vol. 1069. — P. 3–12.
- Kegelmeyer W.P., jr., Pruneda J.M., Bourland P.D. et al. Computer-aided mammographic screening for spiculated lesions // Radiology. — 1994. — Vol. 191. — P. 331–337.
- Krupinski E.A., Nodine C.F. Gaze duration predicts the locations of missed lesions in mammography // Digital Mammography / A.G.Gale (ed.). — Elsevier, 1994. — Vol. 1069. — P. 399–405.
- Lau T.K., Bischof W.F. Automated detection of breast tumors using the asymmetry approach // Copmut. Biomed. Res. — 1991. — Vol. 24. — P. 273–295.
- Miller P., Astley S. Detection of asymmetry using anatomical features // Proc. 1st International Workshop on Digital Mammography. SPIE. — 1993. — Vol. 1905. — P. 433–442.
- Netsch T. Detection of microcalcification clusters in digital mammograms: a scale-space approach // Digitale Bildverarbeitung in der Medizin / D.Arnolds et al. (eds.). — Frieburg, 1996.
- Ng S.L., Bischof W.F. Automated detection and classification of breast tumors // Comput. Biol. Res. — 1992. — Vol. 25. — P. 218–237.
- Petrick N., Chan H.P., Sahiner B., Wei D. An adaptive density-weighted contrast enhancement fikter for mammographic breast mass detection // IEEE Trans. Med. Imaging. — 1996. — Vol. 15. — P. 59–67.
- Strickland R.N., Hahn H.I. Wavelet transforms for detecting microcalcifications in mammograms // IEEE Trans. Med. Imaging. — 1996. — Vol. 15. –P. 218.
- Vyborny C.J. Can computers help radiologists read mammograms? // Radiology. — 1994. — Vol. 191. — P. 315–317.
- Woods K.S., Bowyer K.W. Computer detection of stellate lesions // Digital mammography / A.G.Gale (ed.). — Elsevier, 1994. — P. 221–230.