Автор:
Салыкбаева А.С., Исаева С.Х.
Источник: «НАУКА И ОБРАЗОВАНИЕ — 2011» / Матеріали VII міжнародної наукової конференції молодих вчених. — Євразійський національний університет імені Л.Н. Гумільова, 2011, с.: 372–376
В настоящее время одним из наиболее эффективных методов разделения, извлечения и очистки веществ является жидкостная экстракция органическими растворителями. Она применяется в технологии редких, цветных и благородных металлов, в химическом анализе. На современном этапе развития науки и промышленности особое значение приобретает экологическая безопасность технологических процессов, а, следовательно, повышаются требования к свойствам экстрагентов, исключая применение пожароопасных, токсичных и высоколетучих растворителей. Одним из путей решения данной проблемы является использование легкоплавких органических соединений в качестве экстрагентов.
В случае неорганических веществ особый интерес представляют экстракционные системы «водный раствор – расплав органического вещества». Особенностью данного типа экстракции является существование органической фазы в жидком состоянии только при повышенных температурах. После экстракции и охлаждения экстракционного сосуда до комнатной температуры образуется застывшая компактная масса расплава, которую легко отделить от водной фазы и хранить достаточно долгое время. Такие экстракционные системы впервые были предложены Кузнецовым и сотр. [1]
Основными преимуществами систем, в которых экстрагентом является расплав органического соединения или смеси веществ являются экологическая безопасность, простота выполнения процесса, высокая экстракционная способность. В качестве легкоплавких органических реагентов широко применяются 8–оксихинолин, салицилальдоксим, бензоилацетон, дибензоилметан, нафтол, алифатические карбоновые кислоты [2].
В данной работе рассматриваются особенности использования высших карбоновых кислот в экстракции на примере извлечения ионов никеля стеариновой кислотой. Экстракция карбоновыми кислотами носит катионообменный характер [3]. При этом в случае использования расплава карбоновой кислоты отсутствует гидратация и сольватация экстрагируемых соединений.
С целью определения оптимальных условий экстракции ионов никеля стеариновой кислотой было исследовано влияние следующих факторов: значения рН водной среды, соотношения объема фаз, температуры и времени контакта фаз. Определение степени экстракции производилось путем нахождения количества никеля в водной фазе фотометрическим методом [4]. В качестве реагента на никель использовался диметилглиоксим.
Кислотность водного раствора является одним из основных факторов, которые оказывают значительное влияние на селективность процесса извлечения ионов металлов. Природа металла и применяемого экстрагента также определяет интервал значений рН, в котором металл извлекается полностью.
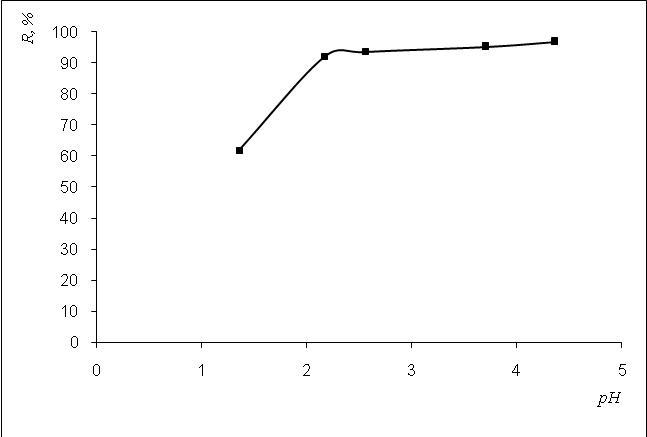
Исследования проводились при температуре 80 °С, соотношении объемов фаз 1:5 и времени экстракции 2 мин. Изучение влияния рН водного раствора на степень экстракции никеля (II) проводилось для концентрации металла 5•10-5 моль/л в широком интервале рН от 1,0 до 5,0. Установлено, что степень экстракции в интервале рН 1,36 – 2,17 резко увеличивается с 62 до 92 %, и при рН = 4,36 достигает максимума 97 % при рН = 4,36 (рис.1).

Рисунок 1 — Зависимость степени извлечения никеля (II) в системе водный раствор — расплав стеариновой кислоты от равновесного значения рН водной фазы
Если представить данные экспериментальные значения в системе координат lgD — pH, где D — коэффициент распределения металла, то наблюдается прямолинейная зависимость (табл. 1).
| № | pHравн | Свод. фазы после экстракции | Сорг. фазы | D | lgD | R, % | ||
| г/л•10-3 | моль/л•10-5 | г/л•10-3 | моль/л•10-5 | |||||
| 1 | 1,36 | 1,143 | 1,937 | 1,857 | 3,148 | 1,625 | 0,211 | 61,9 |
| 2 | 2,17 | 0,238 | 0,404 | 2,762 | 4,681 | 11,6 | 1,064 | 92,06 |
| 3 | 2,56 | 0,191 | 0,323 | 2,809 | 4,762 | 14,75 | 1,169 | 93,65 |
| 4 | 3,70 | 0,143 | 0,242 | 2,857 | 4,843 | 20 | 1,301 | 95,24 |
| 5 | 4,36 | 0,095 | 0,161 | 2,905 | 4,923 | 30,5 | 1,484 | 96,83 |
| 6 | 4,72 | 0,095 | 0,161 | 2,905 | 4,923 | 30,5 | 1,484 | 96,83 |
Для определения возможности концентрирования металла с помощью данной системы было изучено влияние соотношения объемов фаз на степень извлечения металла. Во время исследования менялся объем расплава стеариновой кислоты, объем же водной фазы оставался постоянным и равным 20 мл. Объем расплава экстрагента менялся от 1 до 10 мл, концентрация металла была постоянной и равной 5•10 -5 моль/л, температура 80°С, время контакта фаз 2 мин. Высокая эффективность экстракции никеля (II) достигается при соотношении 1:2 и остается неизменной до изученного в работе интервала соотношений объемов органической и водной фазы, что показано на рис. 2.
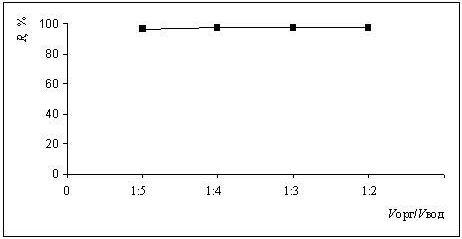
Рисунок 2 — Зависимость степени экстракции от соотношения объемов водной и органической фазы
Температура может оказывать сильное влияние на процесс количественного извлечения никеля. В жидкостной экстракции изменение температуры приводит к изменению растворимости исследуемых веществ как в органической, так и в водной фазе. Поэтому было проведено исследование зависимости экстракции металла от температуры в оптимальных условиях. Установлено, что изменение температуры в интервале от 70 до 90 °С практически не влияет на степень экстракции никеля (II).
На рис. 3 представлены результаты изучения влияния времени контакта фаз на экстракцию. В исследуемом случае время достижения экстракционного равновесия составляет 2 мин.
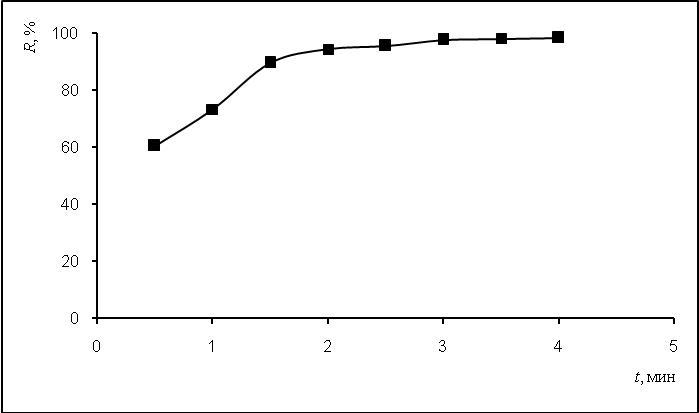
Рисунок 3 — Зависимость степени экстракции от времени контакта фаз
Анализируя полученные данные, можно сделать вывод о том, что ионы никеля (II) количественно извлекаются стеариновой кислотой при рН = 4,36, температуре 80 °С, соотношении органической и водной фаз 1:5, время экстракции должно составлять не менее 2 мин.
Таким образом, были определены оптимальные условия экстракции никеля и выявлено, что большей эффективности процесса способствуют: