Аннотация
Васильченко Ю. М., Кодолов В. И., Волкова Е. Г. – Исследование процесса адсорбции ацетона на поверхности углеродных металлсодержащих наноструктур В работе проведено исследование сорбционной способности углеродных металлсодержащих наноструктур различного состава по отношению к ацетону. На основании значений сорбционной способности проведен расчет удельной поверхности нанопродуктов. Определена степень десорбции ацетона с поверхности указанных образцов.
Введение
Исследования сорбционной способности наноструктур являются источником фундаментальных знаний о поверхностных явлениях. Прикладное использование результатов данных исследований также обширно. Уникальные сорбционные свойства наноструктур позволяют применять их в качестве сенсорных устройств [1], селективных мембран и сорбирующих материалов [2]. Большие надежды возлагаются на использование наноструктур в качестве резервуаров для хранения различных веществ [3].
Модификация полимеров с помощью углеродных наноструктур (УНС) позволяет получать материалы с улучшенными эксплуатационными свойствами, такими как прочность, термостабильность, газопроницаемость, электропроводность [4].
Основной проблемой в получении таких композитов является необходимость равномерного распределения активных наночастиц в полимерной матрице. Для решения этой проблемы наноструктуры вводят в состав полимера в виде тонкодисперсных суспензий или золей с органическим растворителем. Правильный подбор растворителя позволяет обеспечить хорошую совместимость матрицы и наночастиц, достичь однородного состава композиции.
Цель работы: исследование адсорбции жидкого и парообразного ацетона на поверхности углеродных металлсодержащих наноструктур. Задачи: 1) Определение сорбционной способности углеродных металлсодержащих наноструктур по отношению к ацетону. 2) Выявление углеродных металлсодержащих наноструктур с наибольшей активностью к ацетону. 3) Оценка удельной поверхности углеродных металлсодержащих наноструктур. 4) Определение степени десорбции ацетона с поверхности углеродных металлсодержащих наноструктур.
Теоретическое обоснование эксперимента
Сорбционная способность образцов определяется как процентное содержание адсорбированного вещества по отношению к начальной массе адсорбента.
УНС обладают высокой сорбционной способностью, которая обусловлена многими факторами [5]. Во-первых, аналогами УНС, являются хорошо изученные адсорбенты – аморфный углерод или углеродные пленки. Во-вторых, наноструктуры являются объектами с высокой удельной поверхностью и поверхностной энергией. В-третьих, сорбционная способность исследуемых образцов значительно возрастает при наличии дефектов поверхности отдельных наноструктур и их агломератов. Заполнение внутренних полостей нанопродукта или индивидуальных наноструктур адсорбатом может развиваться под действием капиллярного эффекта. Кроме того, дополнительное увеличение сорбционной способности может быть достигнуто за счет предварительной обработки нанопродукта химическими и физическими методами.
В случае адсорбции многоатомных молекул, таких как ацетон, конечный результат процесса будет зависеть не только от температуры, давления, формы поверхности, но и от пространственной ориентации молекулы адсорбата относительно поверхности адсорбента. Поэтому оценка сорбционной способности материалов по отношению к сложным веществам должна носить усредненный характер.
Большинство проведенных исследований адсорбции ацетона на поверхности УНС указывает на химическую природу этого процесса.
В работе [6] образцы одностенных углеродных нанотрубок (УНТ), полученных методом термокаталитического разложения угарного газа при высоком давлении, погружались в ацетон и в течение часа подвергались ультразвуковой обработке. Адсорбция ацетона исследовалась с помощью температурно программируемой десорбции. Увеличенное значение энергии адсорбции ацетона на поверхности УНТ (1,0-2,5) эВ по сравнению с аналогичным значением для поверхности графита (0,33 эВ) и активированного угля (0,4 эВ) указывает на смену физического механизма адсорбции молекул ацетона на химический механизм при переходе от плоской графитовой поверхности к искривленной поверхности наноструктур.
В работе [7] исследована адсорбция гексана, бензола, трихлорэтилена и ацетона на многослойных УНТ двух типов. Среди исследованных веществ самая высокая сорбция достигнута при использовании ацетона в качестве адсорбата. При этом высокие значения энергий адсорбции и десорбции свидетельствуют о химическом механизме адсорбции ацетона на дефектах поверхности УНТ. Аналогичным образом установлено, что адсорбция остальных веществ имеет физическую природу. Из двух типов УНТ наибольшую сорбционную способность проявили наноструктуры, поверхность которых была покрыта слоем аморфного углерода. На основании этих данных сделан вывод о решающей роли структурных дефектов в сорбции органических веществ на поверхности УНТ.
Возникновение как физической, так и химической адсорбции ацетона на поверхности УНС в процессе ультразвуковой (УЗ) обработки отмечено в работе [8]. Автором этой работы предложена схема химического взаимодействия молекулы ацетона и нанотрубки на месте ее структурного дефекта (рис. 1). При этом в реакцию может вступить как целая молекула ацетона, так и ее фрагменты, образованные в процессе нагрева системы выше комнатной температуры.
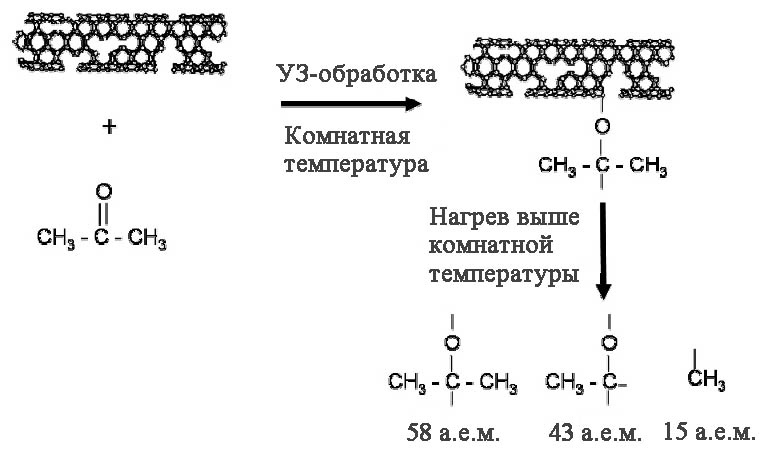
Рисунок 1 – Схема взаимодействия молекулы ацетона и нанотрубки в ходе УЗ обработки
Квантово-химическое моделирование адсорбции ацетона на поверхности углеродных металлсодержащих наноструктур
Теоретическая возможность протекания процесса адсорбции ацетона на поверхности углеродных металлсодержащих наноструктур (УМНС) исследовалась методами квантовой химии с помощью программного продукта HyperChem v.6.03 в приближении РМ3 по стандартной схеме градиентного поиска состояния с минимальной энергией. В ходе расчетов атомы в молекулах смещались таким образом, чтобы каждое последующее их положение понижало полную энергию системы.
Адсорбция ацетона на поверхности углеродной пленки (аналог активированного угля) смоделирована с помощью квантово-химического расчета системы, содержащей молекулу антрацена из 3 углеродных колец, валентности которых скомпенсированы атомами водорода, и молекулу ацетона.
Результаты геометрической оптимизации рассматриваемой системы свидетельствуют о том, что молекула ацетона взаимодействует с фрагментом углеродной пленки (антраценом). Это видно по возникшему искривлению пространственной структуры молекулы антрацена и по отрыву атома водорода от одной из метильных групп в молекуле ацетона (рис. 2).
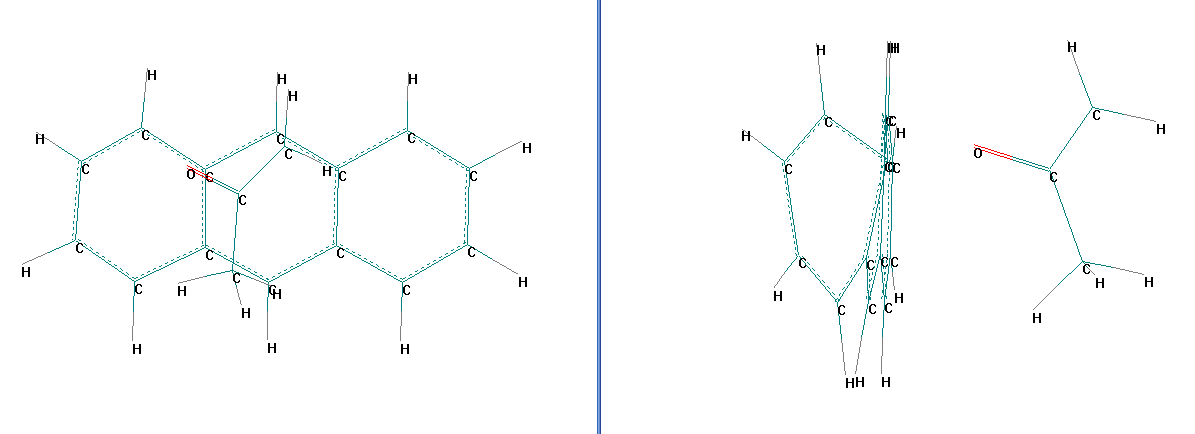
Рисунок 2 – Структура оптимизированной системы, отражающей сорбцию молекулы ацетона на поверхности углеродной пленки
В ходе моделирования процесса адсорбции ацетона на поверхности УМНС, последние аппроксимировались структурой, состоящей из 5 углеродных колец, оптимизированной в присутствии характерного для данного нанопродукта катиона металла.
Известно, что процентное содержание фенольной формы ацетона в чистом ацетоне при нормальных условиях составляет 0,0025 %. Однако отщепление атома водорода от метильной группы ацетона в присутствии углеродной пленки и катиона металла, по данным моделирования, говорит о том, что процентное содержание енольной формы ацетона в системе в процессе адсорбции может увеличиться. Поэтому, при моделировании процесса адсорбции, использованы молекулы ацетона в кетонной и в енольной формах, взятых в соотношении 1:1.
В результате геометрической оптимизации предложенной системы оказалось, что длина связи между атомами водорода и углерода lC-H в метильных группах молекул ацетона в кетонной и енольной формах увеличилась в 2,5-3 раза по сравнению с исходной величиной. Это свидетельствует об отрыве атома водорода от молекул адсорбата с образованием соответствующих радикалов, что и было учтено на заключительной стадии расчетов.
Из рисунка 3 видно, что отторжения молекул ацетона в двух возможных формах от поверхности углеродной пленки не происходит, ионы металла стимулируют процесс взаимодействия компонентов системы, играя координирующую роль.
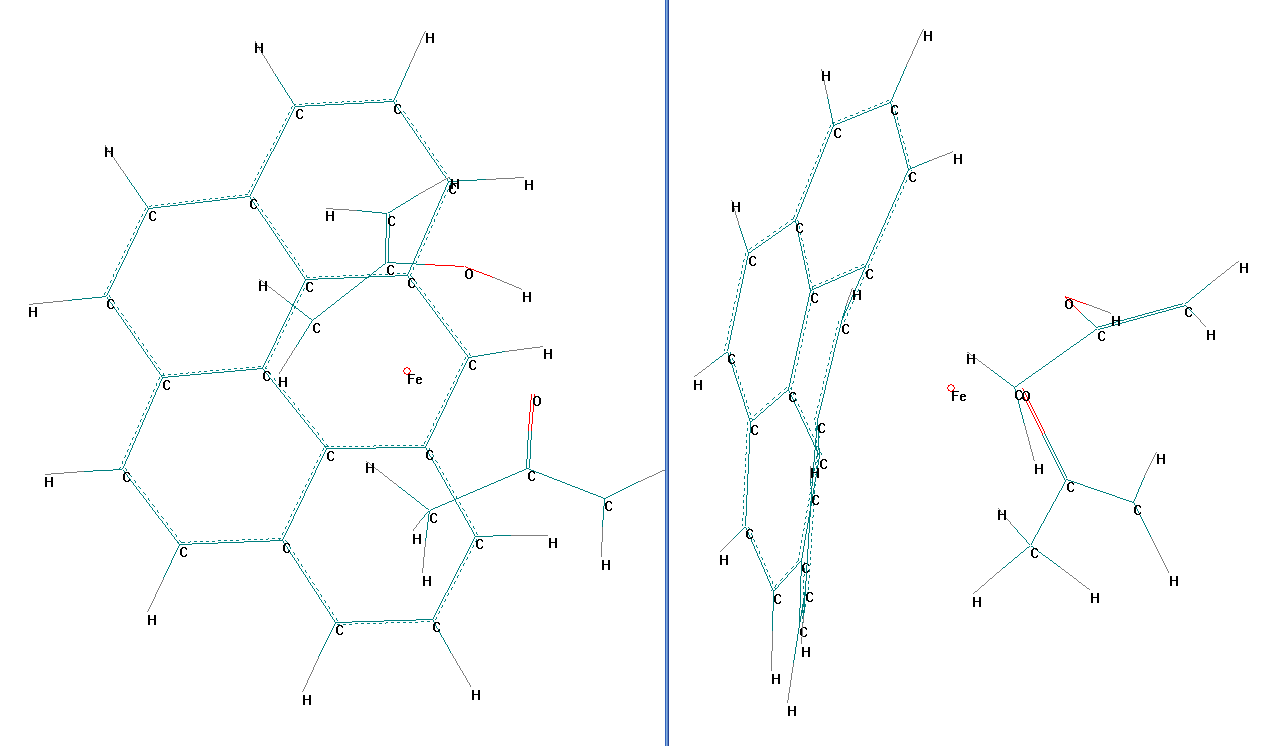
Рисунок 3.1 – Структура оптимизированной системы, отражающей сорбцию молекул ацетона в кетонной и енольной формах на поверхности УМНС (нанопродукт на основе оксида железа)
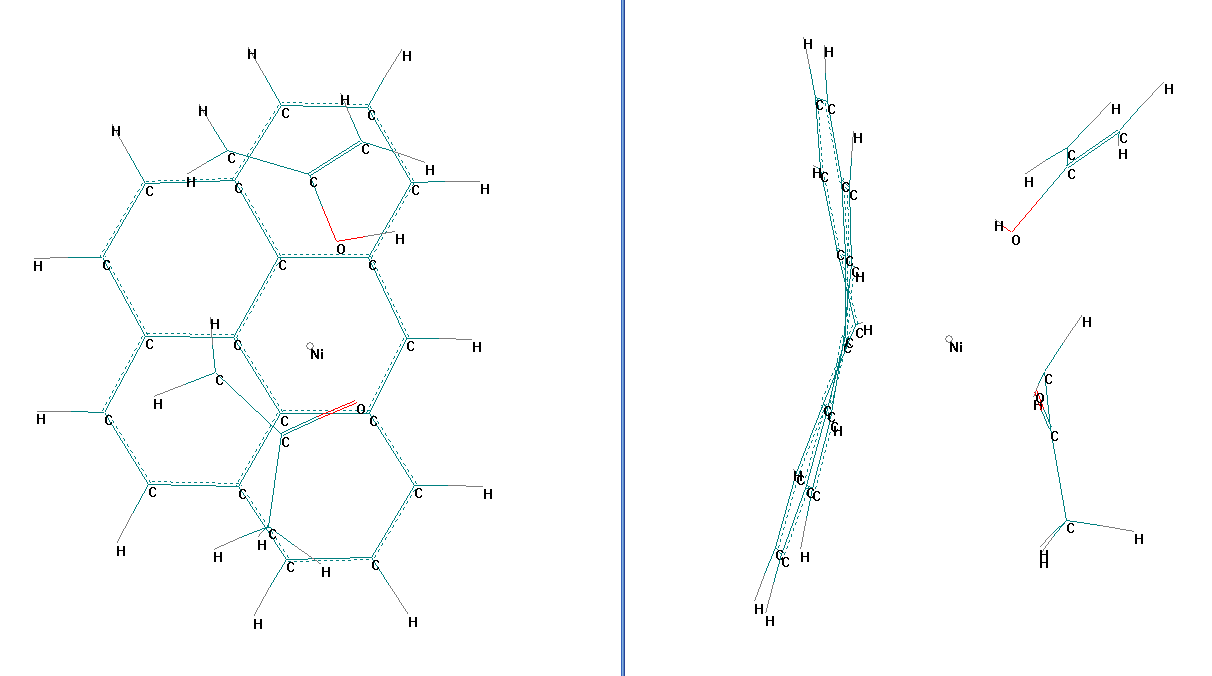
Рисунок 3.2 – Структура оптимизированной системы, отражающей сорбцию молекул ацетона в кетонной и енольной формах на поверхности УМНС (нанопродукт на основе оксида никеля)
Таким образом, с помощью квантово-химических расчетов установлена теоретическая возможность протекания адсорбции ацетона на поверхности УМНС. Показано, что взаимодействие компонентов приводит к изменению химического состава адсорбата за счет отщепление атомов водорода и образования соответствующих радикалов. Адсорбция сопровождается изменением пространственной структуры как адсорбента, так и адсорбата, что должно быть учтено при объяснении механизма адсорбции и расчете величины удельной поверхности нанопродуктов.
Список использованной литературы
1. Chopra S., McGuire K., Gothard N., and Rao A. M. Selective gas detection using a carbon nanotube sensor // Appl. Phys. Lett. 2003. V. 83, № 11. P. 2280-2282.
2. Valcarcel M. et al. Carbon nanostructures as sorbent materials in analytical process // TrAC. 2008. V. 27, №. 1. Р. 34-43
3. Нечаев Ю. С. О природе, кинетики и предельных значениях сорбции водорода углеродными наноструктурами // Успехи физических наук. 2006. Т. 176, № 6. С. 581-610.
4. Жогова К. Б., Давыдов И. А. Методы модификации полимерных материалов углеродными наноструктурами // Научная сессия МИФИ – 2005 : Сборник научных трудов. Часть 2. М. : МИФИ, 2005. С. 41-42.
5. Елецкий А. В. Сорбционные свойства углеродных наноструктур // Успехи физических наук. 2004. Т. 174, № 11. С. 1191-1231.
6. Chakrapani N. et al.Chemisorbtion of Aceton on Carbon Nanotubes // J. Phys. Chem. B. 2003. V. 107, № 35. Р. 9308-9311.
7. Shin Y., Li M. Adsorption of selected volatile organic vapors on multiwall carbon nanotubes // J. Hazardous Materials. 2008. V. 154, Issue 1-3. P. 21-28.
8. Feng X. Application of single walled carbon nanotubes in environmental engineering: adsorption and desorption of environmentally relevant species studied by infrared spectroscopy and temperatur programmed desorption : dis…. Ph.D. 2005. Pittsburg. 126 p.