Сравнительный анализ клинических показателей у больных обследованных групп

Примечание. * – на момент выписки из стационара; D – различия показателей достоверны по сравнению с таковыми у больных группы А (P<0,05–0,0001). То же в табл. 2.
О.С. Сычев, Д.Т. Малидзе, В.Н. Чубучный, Т.В. Гетьман, О.А. Епанчинцева
Институт кардиологии им. Н.Д. Стражеско АМН Украины
(директор – проф. В.Н. Коваленко), г. Киев
Ключевые слова: прогрессирующая стенокардия, внезапная кардиальная смерть, прогно- зирование
Внезапная кардиальная смерть (ВКС) – одна из наиболее сложных проблем современной кардиологии. Почти у 80% больных ВКС возникает на фоне ишемической болезни сердца (ИБС) [1, 3, 4, 9]. ВКС наступает приблизительно у каждого пятого пациента с ИБС [11]. Часто ВКС является первым и единственным проявлением заболевания. Совершенствование методов лечения и диспансеризация больных в значительной мере зависит от возможности прогнозирования ВКС.
Если в отношении прогнозирования ВКС больных, перенесших инфаркт миокарда (ИМ) в клинической практике существуют строгие критерии, основанные на результатах крупных международных исследований, проведенных у десятков тысяч больных, в отношении больных, перенесших нестабильную стенокардию (НС), единого мнения нет, что обусловлено значительно меньшим числом исследований по этой проблеме [12].
Целью исследования было определение наиболее информативных клинико-инструментальных факторов риска ВКС больных, перенесших прогрессирующую стенокардию (ПС), а также разработка алгоритмов индивидуального прогнозирования ВКС.
Материал и методы
Проспективное наблюдение в течение 4 лет проведено у 205 больных, все мужчины, в возрасте от 31 до 71 года, в среднем (51,2±0,6) года, перенесших ПС. Диагноз ПС устанавливали на основании критериев ВОЗ (1979). В исследование не включали пациентов с сердечной недостаточностью (СН) IIA стадии и выше, нарушениями атриовентрикулярной проводимости, блокадой ножек пучка Гиса, декомпенсированными сопутствующими заболеваниями, грубыми нарушениями опорно- двигательного аппарата, а также тех, которые применяли кордарон в течение 4 нед до момента исследования.
При госпитализации стенокардия покоя отмечена у 83,4% больных, еще у 8,8% она была в предыдущем месяце, но в течение 48 ч ее не наблюдали. Ночная стенокардия отмечена у 51% больных, изменения ЭКГ в покое – у 45,9%. У 7,8% пациентов приступов стенокардии покоя не было, и обострение ИБС проявлялось лишь снижением толерантности к физической нагрузке. Таким образом, если использовать классификацию E. Braunwald [6], НС IB класса отмечена в 7,8% больных, IIB класса – в 8,8%, IIIB класса – у преобладающего количества больных (83,4%). Артериальная гипертензия диагностирована у 62,9%, сахарный диабет – у 5,4% больных. По данным коронарографии поражение ствола левой венечной артерии (ВА) было у 17,6% больных, трех ВА – у 27,5%, двух – у 21,5%, одной – у 33,4%. Интактными ВА были в 17,6% наблюдений. ИМ перенесли 52,5% больных, последний ИМ – в среднем (3,5±0,3) года назад. Трансмуральные и крупноочаговые рубцовые изменения выявлены у 71,2%, мелкоочаговые – у 28,8%, поражение передне-перегородочно-верхушечно-боковой области левого желудочка (ЛЖ) – у 50,3%, задне-нижней – у 49,7% больных. Постинфарктный кардиосклероз отмечен у 77,5% пациентов, перенесших один ИМ, у 22,5% – более одного ИМ. Постинфарктная аневризма ЛЖ обнаружена у 7,8% больных, СН I–IIA стадии – у 21%, фракция выброса (ФВ) ЛЖ составляла 40% или меньше – у 18%.
Всем больным после выписки из стационара назначали нитраты, b-блокаторы (преимущественно пропранолол), антагонисты кальция, аспирин, тиклопедин и другие лекарственные средства в качестве симптоматической терапии в соответ ствии с общепринятыми рекомендациями в стандартных дозах.
Для решения поставленных задач использовали комплекс методов, включающих, кроме клинического наблюдения, контроля электрокардиограммы (ЭКГ) и артериального давления, инструментальные исследования: двухмерную эхокардиографию, холтеровское мониторирование (ХМ) ЭКГ в течение 24 ч, нагрузочные тесты – велоэргометрию (ВЭМ) и чреспищеводную электрокардиостимуляцию (ЧПЭКС), селективную коронарографию (которую проводили после стабилизации клинических признаков).
Все исследования проводили после стабилизации состояния больных, в среднем через (7,2±0,5) сут лечения, повторные исследования – через 6 мес.
Конечной точкой (КТ) исследования была ВКС. Не анализировали показатели больных, у которых возник нефатальный ИМ, или умерших не внезапно.
Статистическая обработка данных проведена с помощью программы Statistica for Windows, v. 5.1. Для определения различия показателей в группах использовали критерий Стьюдента – для количественных переменных и критерии Фишера и c2 – для качественных показателей.
Для индивидуального прогнозирования ВКС у больных, перенесших ИМ, создана база данных в системе Access. Составлена специальная форма для ввода данных каждого обследованного, включавшая 150 показателей, в которой отражены их величины при госпитализации, во время повтор ных исследований, а также динамика течения основного заболевания. Информационную ценность признака определяли по формуле для количества информации (А.М. Яглом, 1973). В качестве основного алгоритма прогнозирования использовали вычислительную процедуру Байеса (И.И. Гихман и соавт., 1979). В рамках базы данных использована программа для оптимального выбора прогностических интервалов показателей, определения их информационной ценности, а также получения частотной оценки вероятности встречаемости интервалов в соответствующих группах обследованных и индивидуального прогнозирования.
Результаты и их обсуждение
В течение 4 лет наблюдения больных, перенесших ПС, ВКС отмечена у 44 (21,4%). В 29 (14%) наблюдениях по разным причинам контакт с больными был утерян до окончания срока наблюдения, эти больные исключены из процесса построения модели прогнозирования.
Все пациенты распределены на две группы. В группу А включены 44 больных, у которых возникла ВКС, в группу Б – 161 пациент, выживший в течение периода проспективного наблюдения. ВКС считали смерть, которая наступила в течение 1 ч после резкого усугубления симптомов ИБС на фоне ее стабильного течения [11]. Пациентов, о которых медицинский персонал или родственники точную информацию о времени смерти дать не могли, в анализ не включали (табл. 1).
Таблица 1
Сравнительный анализ клинических показателей у больных обследованных
групп

Примечание. * – на момент выписки из стационара;
D – различия показателей достоверны по сравнению с таковыми у больных
группы А (P<0,05–0,0001). То же в табл. 2.
Пациенты группы А были более старшего возраста, существование ИБС было более длительным (табл. 1). У них достоверно более продолжительным был срок, необходимый для стабилизации состояния, больше число ангинозных приступов за сутки, более часто выявляли постинфарктный кардиосклероз (ПИК), аневризму ЛЖ, СН, стенокардию покоя и ночную стенокардию. Кроме того, в этой группе отмечено достоверно большее число пораженных ВА.
Данные сравнительного анализа показателей инструментальных исследований в группах больных в динамике наблюдения приведены в табл. 2.
Таблица 2
Сравнительный анализ динамики показателей инструментальных методов
исследования

У больных группы А на всех этапах наблюдения были достоверно более высокими конечно-диастолический (КДО), конечно-систолический (КСО) объем, более низкая ФВ ЛЖ. Величина ударного объема (УО) достоверно не различалась в группах. Также не было достоверных различий размера левого предсердия и толщины стенки ЛЖ. Отмечено достоверное снижение за период наблюдения сократимости ЛЖ у больных группы А, которое сопровождалось его дилатацией.
На всех этапах обследования у больных группы А были более низкими уровень пороговой нагрузки, продолжительность нагрузки, выполненная работа, двойное произведение и уровень энергозатрат. Кроме того, при повторном обследовании через 6 мес у них отмечено достоверное увеличение частоты желудочковых нарушений ритма во время нагрузки и снижение индекса энергозатрат.
Сравнительный анализ данных, полученных при применении ЧПЭКС, свидетельствовал о достоверно более низких значениях пороговой частоты стимуляции и более глубокой депрессии сегмента ST у больных группы А.
По данным сравнительного анализа показателей ХМ у больных группы А достоверно более высокими были средняя частота сокращений сердца (ЧСС) за сутки, число эпизодов болевой и безболевой ишемии миокарда, ее суммарная продолжительность за сутки, глубина депрессии сегмента ST, количество желудочковых нарушений ритма (желудочковых экстрасистол (ЖЭ) и пробежек желудочковой тахикардии (ЖТ)), а также класс желудочковых аритмий (по Б. Лауну).
В целях определения предикторов ВКС для каждого показателя подбирали прогностические интервалы так, чтобы информативность соответствующего признака была максимальной.
Из 150 показателей для создания прогностической базы отобраны 39 по критерию максимальной информационной ценности, 20 наиболее ин формативных из них приведены в табл. 3. Показатели приведены в порядке убывания информативности.
Таблица 3
Информативность показателей долгосрочного прогноза ВКС у больных,
перенесших ПС

Наиболее информативными показателями для прогнозирования ВКС больных, перенесших ПС, на момент выписки из стационара оказались (в убывающем порядке) следующие: порог стимуляции при ЧПЭКС 120 имп./мин и меньше, изменения ЭКГ при ЧПЭКС (депрессия сегмента ST больше чем 2 мм), КСО более 90 мл, поражение более чем двух ВА, а также систолический индекс, выполненная работа при ВЭМ, конечно-систолический (КСР), конечно-диастолический (КДР) размер и КДО.
Для обследованной группы из 205 больных проведено индивидуальное прогнозирование с помощью персонального компьютера по 39 показателям. Чувствительность прогнозирования ВКС у больных, перенесших ПС, составила 79,5%, специфичность – 89,4%, прогностическая ценность – 88,2%. Всего в основной группе получено 86,9% правильных ответов.
В целях упрощения прогнозирования ВКС у больных, перенесших ПС, разработаны специальные таблицы. При выборе прогностических показателей исходили из концепции, что как краткосрочный, так и длительный прогноз у пациентов с ИБС в основном зависит от таких факторов, как состояние функции ЛЖ, наличие ишемизированного миокарда и электрической нестабильности миокарда желудочков [7, 8, 10]. Для каждой таблицы выбирали по 3 наиболее информативных показателя, которые отражали перечисленные факторы (табл. 4, 5). Результативность правильного прогнозирования составила соответственно 77,8 и 75%. Значительное повышение риска ВКС наблюдают при сочетании нескольких неблагоприятных факторов.
Таблица 4
Вероятность ВКС у больных, перенесших ПС, в зависимости от величины
КСО, порога стимуляции при ЧПЭКС и наличия пробежек ЖТ
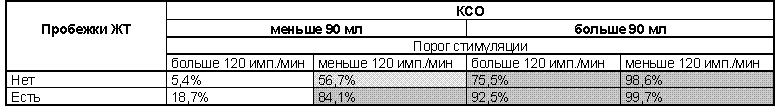
Примечание:![]() –
неопределенный прогноз;
–
неопределенный прогноз; ![]() –
наиболее неблагоприятное сочетание факторов. То же в табл. 5.
–
наиболее неблагоприятное сочетание факторов. То же в табл. 5.
Таблица 5
Вероятность ВКС у больных, перенесших ПС, в зависимости от величины
КДО, числа пораженных ВА и класса желудочковой экстрасистолии

Таким образом, полученные в нашем исследовании результаты согласуются с данными мета-анализа исследований при НС за последние 30 лет [13]. Выявленные нами предикторы являются общими для разных форм ИБС и соответствуют основным механизмам возникновения ВКС у больных (сочетание органического поражения миокарда и транзиторных функциональных факторов риска) [2, 5, 9].
Полученные результаты свидетельствуют о необходимости наиболее раннего выявления факторов риска, что обеспечивает возможность адекватного выбора тактики лечения больных после перенесенных кардиоваскулярных событий. Необходимы более обширные исследования по изучению риска ВКС у больных, перенесших ПС, с включением большего количества пациентов, а также с использованием таких неинвазивных методик, как изучение вариабельности ритма сердца и барорефлекторной чувствительности, оценка дисперсии и вариабельности интервала QT, альтерации зубца Т.
Выводы