Сборник "Технология коагулянтов" под ред. Ткачева К.В.- Л.: "Химия",1974, с.71-76.
Современные тенденции в производстве
сульфата алюминия за рубежом
(По материалам патентной литературы)
Основными потребителями сульфата алюминия являются коммунальное хозяйство и водоочистка. Значительные его количества требуются также для целлюлозно-бумажной, легкой, химической и других отраслей промышленности. В настоящее время у нас в стране и за рубежом производство сульфата алюминия в основном базируется на применении в качестве сырья гидроокиси алюминия, являющегося дефицитным и дорогостоящим продуктом. В связи с этим характерной чертой современных технологических разработок является привлечение в качестве исходного материала таких недефицитных видов сырья, как низкосортные бокситы, каолины глины, алуниты.
В ряде стран, особенно в США, большое внимание уделяется прямой переработке низкосортных бокситов, имеющих малое содержание железа, на сульфат алюминия
[1 - 6]. Для стран, не обладающих значительными запасами бокситов с низким содержанием железа, первостепенное значение имеет организация производства сульфата алюминия с применением в качестве сырья каолинов и глин [7 - 12]. Работы в этом направлении проводятся практически во всех промышленно развитых странах.Необходимой стадией переработки каолинов и глин является перевод содержащегося в них глинозема в кислоторастворимое состояние. Существуют три направления для решения этого вопроса.
Наиболее традиционным является обжиг во вращающихся барабанных печах. Его основной недостаток - значительный унос пыли с дымовыми газами. Ряд патентов
[13 - 15] предлогает мероприятия по предотвращению этого явления. Согласно [13], сырье перед одпчей в печь следует гомогенезировать, используя для этой цели аппараты, применяемые в кирпичной промышленности (бегуны, смесители и др.), а сам обжиг в течение времени, которое в несколько раз превышает обычно применявшееся. Известна [15] также более сложная схема подготовки сырья для обжига. Глину содержащую каолин, прессуют в пластинки толщиной 6,4 - 15,9 мм, которые затем расслаиваются на чешуйки. Последние нагревают при 149 - 427 0С и прокаливают во вращающейся печи. Очень простое усовершенствование предлагается в патенте США [14]: подачу измельченной глины рекомендуется, производить противотоком продуктам сгорания; в этом случае унос материала сводится к минимуму из-за образования небольших шариков глины в процессе пребывания ее в барабане.Не рассматривая вопрос о пылеуносе, авторы патента ГДР [16] предлагают с целью увеличения выхода
Al2O3после кислотной обработки измельчать подаваемое на обжиг сырье в струйной или вибрационной мельнице.Для уменьшения пылеуноса и одновременно получения более быстро разделяющейся суспензии рекомендуется [17] добавлять к измельченной глине определенное количество воды и серной кислоты с тем, чтобы масса после смешения содержала 5 – 25% Н
2О и 1 – 5% Н2SО4 по отношению к весу глины. Полученную массу выдерживают 15 – 30 мин и направляют на обжиг во вращающуюся барабанную печь.Радикальное изменение технологии, предусматривающее совмещение операций прокалки и кислотной обработки, рекомендуется в патентах [18, 19]. Смысл заключается в предварительном смешении каолина с серной кислотой и подаче этой смеси на обжиг. Полученный после обжига материал подвергается водному выщелачиванию. В результате, согласно приведенным сведениям, извлечение А1
2O3 достигает 96,0 [18] или даже 99,5% [19]. Подобное ведение процесса позволяет также снизить температуру обжига до 250 0С. Однако серьезные опасения вызывает возможность потери значительных количеств серной кислоты с отходящими газами.Значительное количество патентов посвящено автоклавному способу переработки глиноземсодержащих силикатов [20 – 24]. Процесс осуществляют следующим образом: каолин или глину суспендируют с 25%-ной Н
2SО4, и обрабатывают в автоклаве непрерывного действия, снабженном мешалкой, при 145 – 200 0С и не менее 3 атм в течение 4 – 6 ч. Степень извлечения А12O3 составляет 99,82% [21] или 80,7% [23]. Значительные работы по промышленному освоению этого способа ведутся в ПНР, однако большие трудности, связанные с конструктивным оформлением процесса, задерживают его внедрение.Весьма близкие способы, отличающиеся лишь применением вместо серной кислоты раствора сульфата трехвалентного железа [25] или отработанного сернокислотного травильного раствора [26], запатентованы в ФРГ и США. Мы не располагаем сведениями о промышленной проверке этих патентов, но учитывая, что все производство сульфата алюминия старается базироваться на сырье с возможно меньшим содержанием железа, так как очистка от последнего связана с большими трудностями, рассчитывать на внедрение этих способов в производственную практику не приходится.
Особое внимание уделяется очистке растворов сульфата алюминия от железа. При получении сульфата алюминия с целью использования его в качестве коагулянта в коммунальном хозяйстве и водоочистке эта операция не является обязательной. Для этого, как и для получения грубых сортов бумаги, пригоден так называемый
[27] технический сульфат алюминия с содержанием железа до 0,5%. Однако для хороших сортов бумаги необходим продукт с содержанием железа не более 0,005%, а некоторые производства требуют [28], чтобы содержание железа не превышало 0,00005%.Авторы патентов [29, 30] рекомендуют начать очистку от железа до получения растворов сульфата алюминия. Так, согласно [29], обжиг сырья следует вести в окислительной атмосфере, чтобы перевести Fе
2+ в Fе3+. Напротив, в соответствии с данными [30] обжиг надо вести в восстановительной атмосфере, а затем обожженный материал подвергнуть магнитной сепарации. Однако эти полумеры явно не решают вопроса очистки, как не решают его и традиционные методы очистки [20, 31 – 34]. В число этих методов входят: 1) обработка глиноземсодержащего материала при недостатке Н2SO4; 2) окисление Fе2+ до Fе3+ в растворе различными окислителями с последующим отделением; 3) удаление железа путем электролиза.Основным направлением работ по получению очищенного от железа сульфата алюминия явилась кристаллизация последнего из растворов. Необходимо отметить, что подобная очистка попутно решает задачу ликвидации одной из наиболее трудноосуществимыми стадий процесса – концентрирования растворов.
В ряде патентов [3, 26, 35 – 37
] рекомендуется проводить кристаллизацию сульфата алюминия из растворов путем добавления 78%-ной Н2SO4 в количестве, необходимом для выделения А12(S04)3,. Процесс проводят при постепенном понижении температуры от 70 0С до комнатной. Выделенные кристаллы гидратированного сульфата алюминия отделяют от маточного раствора на фильтре. Маточный раствор, в котором содержатся серная кислота и сульфат железа, используют для обработки свежей порции прокаленного материала.Однако сравнительно несложная на первый взгляд операция высаливания кристаллогидрата А1
2(S04)3 связана в действительности со значительными трудностями, которые вызваны получением кислых солей типа А12(SО4)3*3Н2SO4*7Н2О; А12(SО4)3*Н2SO4*Н2О; А12(SО4)3*Н2SO4*12Н2О [36, 37]. В тех случаях, когда получаемый сульфат алюминия является полупродуктом для дальнейшей переработки на глинозем, такой метод кристаллизации может оказаться оправданным, хотя улавливание образующихся при термической обработке SO2 и SO3 и концентрирование получаемой слабой Н2SO4, также не являются легкими операциями. Применение же подобных кислых кристаллогидратов в качестве товарного продукта невозможно. Поэтому в указанных выше патентах предлагаются дополнительные операции с целью перевода кислой соли в нейтральную. К ним относятся: 1) промывка кристаллов на фильтре насыщенным раствором чистого сульфата алюминия; 2) промывка кристаллов .46%-ной или концентрированной Н2SO4, 3) последующая термическая обработка кислого сульфата при 140 – 180 0С или растворение промытых кристаллов в их кристаллизационной воде путем нагревания, нейтрализация полученного расплава при помощи гидроокиси алюминия и повторная кристаллизация.В связи с этим рекомендуется
[38 – 40] в раствор, содержащий А12(SО4)3, и Н2SO4, вводить затравочные кристаллы чистого сульфата алюминия. Но и подобное усовершенствование, по-видимому, не гарантирует получение нейтрального сульфата, так как патенты [38, 39] предполагают проведение после отделения кристаллов операций, аналогичных описанным выше, а в патенте [40] указывается, что этот способ должен быть применим для кристаллизации как А12(SO4)3*16-18Н2О, так и солей А12(SО4)3*xН2SO4*yН2О . Более того, одним из пунктов этого патента прямо защищается получение в результате кристаллизации в подобных условиях А12(SО4)3*Н2SO4*12Н2О.Наиболее удовлетворительное решение вопроса кристаллизации А1
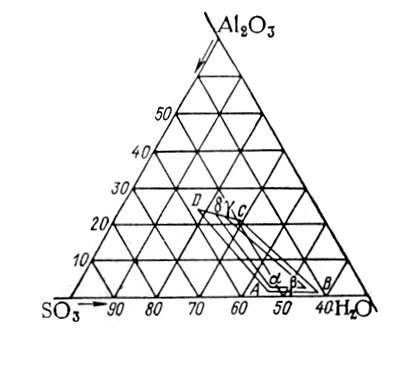
2(SО4)3 из раствора, содержащего Н2SO4, найдено в патенте [41]. Авторы рекомендуют кристаллизовать А12(SO4)3, из растворов разбавленной Н2SО4 при повышенных температурах в присутствии затравки из А12(SO4)3*5,5–6Н2О. На рис. 2.1 точки А, В, С, D – вершины четырехугольника, ограничивающего состав раствора, который, кристаллизуясь при 105 – 140 0С, дает возможность получить А12(SО4)3*4-8Н2О.
Метод очистки раствора А1
2(SО4)3 от железа, основанный на осаждении сульфата железа из раствора, предлагается в патенте ПНР [43].Большой интерес
, на наш взгляд, представляют опубликованные в последнее время патенты, описывающие очистку растворов сульфата алюминия от железа и некоторых других примесей путем применения анионообменников и других веществ, обеспечивающих селективное извлечение примесей из растворов [44 - 49].Для производства сульфата алюминия, основывающегося на каолинах и глинах, существенное значение приобретает вопрос концентрирования слабых растворов
. Ряд патентов [50 - 53] посвящен проведению процесса вакуум-выпарки растворов А12(SО4)3, совмещенный зачастую с "прерывистой кристаллизацией", разработанной Х. Кречмаром [51, 52]. Согласно патентным описаниям, подобное осуществлние процесса позволяет одновременно решать вопросы очистки растворов от железа, доводя содержание последнего в них до 0,003 – 0,005% (в пересчете на Fе2О3). Следует однако заметить, что проведение процесса вакуум-выпарки связано с серьезными технологическими и конструкционными затруднениями.Значительное внимание уделяется в патентных разработках вопросу кристаллизации А1
2(SO4)3 из расплава. Эта стадия производства, как видно из обнаруженных материалов, в настоящее время является узким местом производства, особенно в связи с повышением со стороны потребителей требований к виду поставляемого товарного продукта – желание получить его в гранулированном или мелкодробленном (но без пыли) виде, отсутствие слеживаемости и т. д. Судя по патентным источникам [54 – 59], ведется усиленная разработка способа кристаллизации сульфата алюминия из расплава на движущейся ленте.Интересное направление намечается в способе получения твердого сульфата алюминия в
[60]. Предложено производить напыление жидкого сульфата алюминия при 85 - 87 0С на передвигающиеся агломерационные частицы твердого сульфата алюминия. Охлаждение подаваемого в виде тонкой ленки расплава и его разбивание на капли производится с помощью вдуваемого в горизонтальном направлении холодного воздуха. Выгружаемый продукт содержит 14 - % Al2O3.В
двух патентах [61, 62] описаны способы дегидратации кристаллического сульфата алюминия. Первый из них предусматривает сушку кристаллогидрата воздухом при 1500С. При этом из продукта, содержащего 14,8% А12(SО4)3, получают сульфат алюминия с содержанием 23,4% А12(SО4)3. Авторы патента объясняют возможность подогрева до указанной температуры без плавления материала благоприятным строением его поверхности. Согласно патенту [62], обезвоживание А12(SО4)3*16-18Н2О, содержащего 2 - 12% избыточной H2SO4, осуществлялось во вращающейся сушилке при подъеме температуры от 85 до 149 0С.Появление ряда патентов
[41, 61, 62] свидетельствует о намечающейся тенденции к получению товарного продукта с более высоким содержанием Al2O3, чем по существующему на мировом рынке стандарту (17 - 18 %). Безусловно, получение такого продукта весьма перспективно в экономическом отношении, так как позволяет резко снизить стоимость перевозок.Основными направлениями в производстве сульфата алюминия за рубежом являются:
Литература