 Диоксид углерода (углекислый газ,
угольный ангидрид, углекислота) CO2 - соединение углерода с
кислородом, конечный продукт окисления углерода; бесцветный, обладающий
слегка кисловатым вкусом и запахом, газ [8]. Свойства диоксида углерода
приведены в таблице 2.
Диоксид углерода (углекислый газ,
угольный ангидрид, углекислота) CO2 - соединение углерода с
кислородом, конечный продукт окисления углерода; бесцветный, обладающий
слегка кисловатым вкусом и запахом, газ [8]. Свойства диоксида углерода
приведены в таблице 2. | № п/п | Наименование показателя | Ед.изм. | Значение |
| 1 | Молярная масса, M | г/моль | 44,011 |
| 2 | Температура плавления, tпл. | oС | - 56,65,2 ат |
| 3 | Температура сублимации, tвозг. | oС | - 78,47 |
| 4 | Плотность: -rг. -rтв. -rж. |
г/л | 1,9770 1,560-79 1,101-37 |
| 5 | Критические параметры:
-tкр. -pкр. -rкр. |
oC МПа г/см3 |
31,05 7,383 0,468 |
| 6 | Растворимость в воде | мл/ 100 г воды |
8820 2475 |
| 7 | Газовая постоянная, R | кДж/ (кг*К) |
0,188915 |
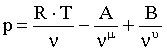 где А и В - функции
температуры.
где А и В - функции
температуры. 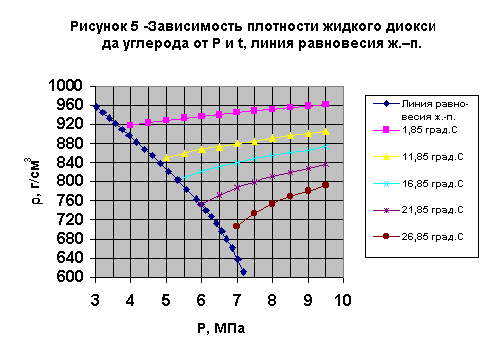
 где to=1, ro=rкр.;r -плотность
диоксида углерода; r, s - степени полинома.
где to=1, ro=rкр.;r -плотность
диоксида углерода; r, s - степени полинома.
