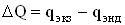Авторы: А.А. Агроскин, Е.И. Гончаров, Н.С. Грязнов
Время и место издания: Кокс и химия, 1972, № 8, С. 1–4
Тепловые свойства углей в пластическом состоянии
Термическая характеристика угля в пластическом состоянии в значительной степени определяет особенности процесса коксообразования. Отсутствие в литературе данных по этому вопроcy объясняется преимущественно трудностями соответствующих экспериментальных определений.
В нашем исследовании для нахождения эффективной и истинной теплоемкостей использован принцип диатермической оболочки, разработанный в применении к углям. Тепловой эффект реакций пиролиза определяли по величине площади, ограниченной кривыми эффективной и тайной теплоемкостей. Исследования выполнены в токе очищенного азота при скорости нагрева 10 град/мин.
Для увязки термических характеристик углей в пластическом состоянии с изменением этих характеристик на протяжении всего процесса пиролиза все определения выполнены в широком диапазоне изменения температур от 20 до 1000 °С.
Были испытаны пробы кузнецких углей технологических групп КЖ14 (ш. Тайбинская) и К13 (Судженская ЦОФ) и марки К2 (ш. Коксовая). Характеристика углей приведена в табл. 1.
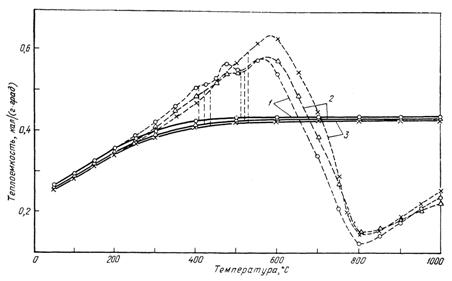 Сводные результаты определения эффективной и истинной теплоемкостей проб углей в интервале 50–1000° С представлены на рис. 1. Согласно этим данным, эффективная теплоемкость угля КЖ14 характеризуется двумя эндотермическими максимумами: при 475°С Ср=0,566кал/(г*град) и 575°С Ср=0,580 кал/(г*град) и экзотермическим минимумом при 800° С (Ср = 0,125 кал/(г*град)). Истинная теплоемкость этого угля достигает при 1000° С значения 0,436 кал/(г*град). Кривая изменения эффективной теплоемкости угля К13 также характеризуется тремя экстремальными точками при тех же температурах. Однако абсолютное значение максимума при 475° С несколько ниже и составляет 0,543 кал/(г*град). Кривая истинной теплоемкости этого угля во всем исследуемом интервале температур проходит несколько ниже соответствующей кривой угля КЖ14, что объясняется большей степенью метаморфизма угля К13.
Сводные результаты определения эффективной и истинной теплоемкостей проб углей в интервале 50–1000° С представлены на рис. 1. Согласно этим данным, эффективная теплоемкость угля КЖ14 характеризуется двумя эндотермическими максимумами: при 475°С Ср=0,566кал/(г*град) и 575°С Ср=0,580 кал/(г*град) и экзотермическим минимумом при 800° С (Ср = 0,125 кал/(г*град)). Истинная теплоемкость этого угля достигает при 1000° С значения 0,436 кал/(г*град). Кривая изменения эффективной теплоемкости угля К13 также характеризуется тремя экстремальными точками при тех же температурах. Однако абсолютное значение максимума при 475° С несколько ниже и составляет 0,543 кал/(г*град). Кривая истинной теплоемкости этого угля во всем исследуемом интервале температур проходит несколько ниже соответствующей кривой угля КЖ14, что объясняется большей степенью метаморфизма угля К13.
Для угля К2 эндотермический пик при 475 °С отсутствует, но величина эндотермического максимума при 575 °С возросла до 0,640 кал/(г*град).
Кривая истинной теплоемкости этого угля располагается еще ниже аналогичной кривой угля К13 (см. рис. 1).
Для более детального изучения изменения эффективной теплоемкости углей в пластическом состоянии определения были выполнены через 25° С, а в некоторых случаях и через 10° С (табл. 1, рис. 2).
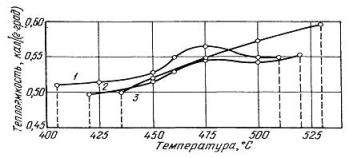
Таблица 1
| Уголь КЖ14 | Уголь К13 | Уголь К2 |
| t, °C | c, кал/(г*град) | t, °C | c, кал/(г*град) | t, °C | c, кал/(г*град) |
| 405 | 0.507 | 420 | 0.498 | 435 | 0.502 |
| 425 | 0.513 | 450 | 0.516 | 450 | 0.520 |
| 450 | 0.530 | 460 | 0.528 | 475 | 0.547 |
| 460 | 0.550 | 475 | 0.544 | 500 | 0.572 |
| 475 | 0.567 | 500 | 0.540 | 530 | 0.597 |
| 490 | 0.554 | 520 | 0.553 | - | - |
| 500 | 0.550 | - | - | - | - |
| 510 | 0.550 | - | - | - | - |
Как показали исследования, истинная теплоемкость углей в пластическом состоянии монотонно возрастает с температурой и не показывает никаких экстремальных значений (см. рис. 1). Структурно-химические преобразования органической массы углей при термическом воздействии являются результатом одновременно протекающих реакций деструкции и синтеза. Последние, как сопряженные реакции представляют собой элементы единого процесса – необратимой радикальной поликонденсации, вызывающей образование твердого остатка пространственного строения. Ход процесса и его конечный результат определяет соотношение скоростей этих частных реакций – деструкции и возникновения свободных радикалов, с одной стороны, и их рекомбинацией и насыщением водородом – с другой.
Реакции деструкции связаны с высокой энергией активации и требуют затрат большого количества тепла. Реакции ассоциации протекают с малой энергией активации или без нее, с уменьшением теплосодержания и сопровождаются выделением тепла. Поэтому при непрерывном течении процесса пиролиза тепловой эффект в каждый данный момент времени обнаруживается как превышение теплового эффекта одного знака над тепловым эффектом другого знака, т. е.
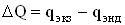
Переход углей в пластическое состояние и возникновение многофазной системы, или образование твердого обуглероженного остатка, минуя стадию пластического состояния, также определяется соотношением скоростей реакций деструкции и синтеза, зависящих как от скорости нагревания,так и от термостойкости, реакционной способности продуктов реакции и ресурсов активного водорода. Преобладание деструктивных явлений в начальной стадии процесса пиролиза (вследствие малой термостойкости углей), сопровождающееся перераспределением водорода, обусловливает возникновение низкомолекулярных парогазовых и олигомерных жидких продуктов, что определяет переход углей в пластическое состояние. Поэтому пластическое стояние должно сопровождаться эндотермическим эффектом (см. рис. 2).
Но преобладание деструктивных явлений способствует увеличению концентрации частиц с ненасыщенными связями и функциональными группами, что ускоряет обратный процесс — структурирование пластической массы и формирование твердого остатка (полукокса).
Структурирование пластической массы – ассоциация активных центров отчетливо проявляется на фоне эндотермического превращения в виде эндотермической седловины на кривых эффективной теплоемкости углей (рис. 1). У слабоспекающихся углей, например марки К2, этот эффект проходит вяло или вовсе отсутствует, поэтому не отражен на кривой эффективной теплоемкости.
Отмеченные особенности процесса пиролиза спекающихся и неспекающихся (или слабоспекающихся) углей согласуется тепловым изменением при переходе к полукоксу, по данным дифференциально – термического анализа. В табл. 3 приведены сводные результаты определения теплового эффекта реакции эндотермической стадии dН1, экзотермической стадии dН2, суммарного теплового эффекта пиролиза dН, а также значения теплового эффекта реакции пиролиза в пластическом состоянии dНпл. все данные отнесены к 1 г исходного сухого угля. В случае необходимости при помощи термогравиметрических кривых они могут быть пересчитаны на 1 г твердого остатка при данной температуре.
В соответствии с нашими прежними исследованиями, по мере повышения степени метаморфизма температура перехода от стадии преобладания эндотермических реакций к стадии экзотермических реакций повышается с 650 °С для угля КЖ14 до 705 °С для угля К2 (см. рис. 1).
Полученные значения теплот реакций пиролиза углей (см. табл. 3) выше значений, приводимых нами ранее. Это объясняется тем, что в данном исследовании принята конечная температура опытов 1000 °С, а в предыдущем 900 °С. В интервале температур 900–1000 °С экзотермический эффект реакции существенно возрастает, отсюда увеличивается и величина dН. В соответствии с ранее установленной закономерностью суммарный тепловой эффект с повышением сте¬пени метаморфизма углей уменьшается. Для указанной степени метаморфизма исходных углей величина dНпл в температурном интервале пластичности остается практически постоянной, изме¬няясь от -10,2 до -12,2 кал/г (см. табл. 3).
Таблица 2
| Угли | Тепловой эффект кал/г |
| dH1 | dH2 | сумма dH | dHпл |
| КЖ14 | -31.7 | +69.7 | +38.0 | -11.2 |
| К13 | -34.4 | +64.1 | +29.7 | -10.2 |
| К2 | -44.4 | +58.8 | +14.4 | -12.2 |
Выводы.
1. Изменение эффективной теплоемкости исследованных проб углей в интервале 20 – 1000°С характеризуется эндотермическим максимумом при 550 – 575 °С и экзотермическим минимумом при 800 – 820 °С. В эндотермической области в процессе пиролиза хорошо спекающихся углей возникает отклонение экзотермического характера, приуроченное к концу пластического состояния и началу образования полукокса.
2. Эффективная теплоемкость в пластическом состоянии изменяется от 0,507 до 0,550 для угля КЖ14; от 0,498 до 0,553 для угля К13 и от 0,502 до 0,597 кал/(г*град) для угля К2. Истинная теплоемкость монотонно возрастает с температурой и не проявляет никаких аномалий в пластическом состоянии.
3. Суммарный тепловой эффект пиролиза при нагреве до 1000 °С составляет +38,0 кал/г для угля КЖ14, +29,7 кал/г для угля К13 и +14,4 кал/г для угля К2. Тепловой эффект реакций в пластическом состоянии эндотермичен и практически не зависит от степени метаморфизма углей.
Cписок литературы
1. Еркин Л.Н., Лобанова Л.Н., Бернацкая М.А. - "Кокс и химия", 1958, №2, с. 23-30
2. Хольцк Д. - "Кокс и химия", 1970, №7, с. 20-26
3. Нефедов П.Я., Литвинов Е.М. - "Кокс и химия", 1975, №11, с. 13-17
4. Агроскин А.А., Гончаров Е.Н. - "Изв. вуз. Энергетика", 1965, №12, с. 14-19
5. Агроскин А.А., Гончаров Е.Н. - "Изв. вуз. Химия и химическая технология", 1967, №12 с. 1101-1103
 Сводные результаты определения эффективной и истинной теплоемкостей проб углей в интервале 50–1000° С представлены на рис. 1. Согласно этим данным, эффективная теплоемкость угля КЖ14 характеризуется двумя эндотермическими максимумами: при 475°С Ср=0,566кал/(г*град) и 575°С Ср=0,580 кал/(г*град) и экзотермическим минимумом при 800° С (Ср = 0,125 кал/(г*град)). Истинная теплоемкость этого угля достигает при 1000° С значения 0,436 кал/(г*град). Кривая изменения эффективной теплоемкости угля К13 также характеризуется тремя экстремальными точками при тех же температурах. Однако абсолютное значение максимума при 475° С несколько ниже и составляет 0,543 кал/(г*град). Кривая истинной теплоемкости этого угля во всем исследуемом интервале температур проходит несколько ниже соответствующей кривой угля КЖ14, что объясняется большей степенью метаморфизма угля К13.
Сводные результаты определения эффективной и истинной теплоемкостей проб углей в интервале 50–1000° С представлены на рис. 1. Согласно этим данным, эффективная теплоемкость угля КЖ14 характеризуется двумя эндотермическими максимумами: при 475°С Ср=0,566кал/(г*град) и 575°С Ср=0,580 кал/(г*град) и экзотермическим минимумом при 800° С (Ср = 0,125 кал/(г*град)). Истинная теплоемкость этого угля достигает при 1000° С значения 0,436 кал/(г*град). Кривая изменения эффективной теплоемкости угля К13 также характеризуется тремя экстремальными точками при тех же температурах. Однако абсолютное значение максимума при 475° С несколько ниже и составляет 0,543 кал/(г*град). Кривая истинной теплоемкости этого угля во всем исследуемом интервале температур проходит несколько ниже соответствующей кривой угля КЖ14, что объясняется большей степенью метаморфизма угля К13.