
Для виміру оксидів азоту в димових газах енергетичних установок використовується велика кількість найрізноманітніших методів, які можна умовно поділити на дві групи. До першої групи відносяться хімічні методи аналізу. Визначення здійснюють за допомогою сухих індикаторних порошків або рідинних селективних поглиначів. Погрішність виміру хімічними газоаналізаторами пов'язана з неповнотою поглинання оксидів азоту з аналізованої газової суміші.
До другої групи відносяться фізичні, фізико-хімічні та електрохімічні методи аналізу. Ця група методів дозволяє визначати вміст оксидів азоту в димових газах за допомогою приладів безперервної дії, у яких використовуються спектрометричні, люмінесцентні й електрохімічні датчики, а також монохроматичний лазерний промінь. Однак застосування приладів такого типу на електростанціях обмежено їхньою низькою надійністю роботи і високою вартістю.
При використанні фізичних, фізико-хімічних та електрохімічних аналізаторів помилки у вимірах виникають за рахунок компонентів, що заважають аналізу. Наприклад, при визначенні концентрації оксидів азоту інфрачервоним спектральним газоаналізатором на показання приладу впливає неконтрольований вміст водяних парів, а при визначенні люмінесцентним аналізатором погрішність виміру виникає за рахунок наявності в аналізованій газовій суміші речовин, здатних гасити люмінесценцію. Таким чином, при застосуванні різної апаратури, призначеної для визначення концентрації оксидів азоту в топкових газах, вибір стандартного методу має вирішальне значення. Із застосованих на практиці експлуатації енергетичного устаткування методів визначення концентрації оксидів азоту найбільш незалежним від впливу заважаючих факторів є хімічний метод, заснований на використанні в якості індикаторного реактиву розчину фенолдісульфокислоти. Цей метод у ряді країн (США, Японія, Австрія й ін.) є еталонним.
Метод визначення вмісту оксидів азоту в димових газах заснований на реакції окислювання оксидів азоту до азотної кислоти і на взаємодії останньої з ФДК з утворенням пікринової кислоти:

Отриману пікринову кислоту переводять у стійкий пофарбований нітроамонієвий хромоген, концентрацію якого в аналізованому розчині визначають фотоколориметричним методом.
Метод застосовують для аналізу газів, що містять оксиди азоту в діапазоні від 20 до 5000 мг/м3. Діапазон виміру може бути розширений за рахунок розведення водою пофарбованого розчину перед колориметруванням або за рахунок зменшення обсягу відібраної проби газу. Заважають визначенню неорганічні сполуки: нітрати, нітрити або органічні сполуки азоту, а також галогенмісткі сполуки. Перші завишають результати аналізу, останні - занижують.
При визначенні оксидів азоту в топкових газах важливо вибрати точку добору, що дозволяє одержувати представницькі проби, у яких відсутні втрати. На результати аналізу можуть впливати конструктивні особливості пробоотборників і їхній матеріал.
Газ, що відбирається з газоходу, пропускається через мірну газову піпетку, перед якою установлений фільтр із скловати для затримки твердих часток. Щоб відкоригувати обсяг відібраної проби газу, вимірюють температуру і тиск газу, що пропускається через систему добору. Після відключення піпетки від системи в неї вводять 10 - 15 мл кислотноперекисного поглинального розчину, струшують близько 1 хв і залишають на 16 г до повного окислювання і поглинання оксидів азоту.
Через 16 г розчин з газової піпетки з поглиненими оксидами азоту переносять у порцелянову випарну чашку ємністю 200 мл. В іншу випарну чашку поміщають 10 - 15 мл поглинального розчину для контрольного експерименту. Газову піпетку 2 - 3 рази ополіскують водою, змиви додають у випарну чашку. Таку ж кількість води додають у контрольний розчин, з яким роблять ті ж операції, як і з робочим розчином. Розчин у випарній чашці нейтралізують 4 %-ним їдким натром, перевіряючи середовище лакмусовим папером.
Розчини випарюють на водяній бані до сухого залишку, прохолоджують і обережно додають 2 мл ФДК по краплях, ретельно перемішуючи зміст чашки. Додають 1 мл дистильованої води, 4 краплі сірчаної кислоти і нагрівають на водяній бані протягом трьох хвилин при періодичному помішуванні. Розчини прохолоджують, додають при помішуванні 10 мл дистильованої води і потім по краплях концентрований розчин аміаку доти, поки надлишок аміаку не офарбить лакмусовий папір. При нейтралізації аміаком розчин офарблюється в жовтий колір. Розчин негайно фільтрують через фільтр у мірну колбу ємністю 100 мл. Випарну чашку обмивають кілька разів невеликими порціями дистильованої води і змиви фільтрують у ту ж колбу. Розчин у колбі доводять до мітки дистильованою водою.
При фільтруванні концентрованих проб фільтр може бути пофарбований у жовтий колір, тому його варто ретельно промити водою до зникнення фарбування. Розчини до колориметрування варто зберігати в темному місці.
Оптичну щільність розчину вимірюють за допомогою фотоелектричного спектрофотометра або фотометра при довжині хвилі 400 нм (ФЕК-60, світлофільтр № 2). По каліброваній кривій визначають вміст діоксиду азоту. Як розчин порівняння використовують контрольний розчин.
Декілька аліквот від 0 до 20 мл стандартного розчину азотнокислого калію поміщають у випарні чашки, додають 10 - 15 мл поглинального розчину і роблять визначення як описано вище при підготовці проби до аналізу. Калібровану криву будують у залежності від кількості діоксиду азоту та оптичної щільності розчину (рис. 1).

Реактиви:
Для приготування поглинального розчину в мірну колбу ємністю 1 л наливають 800 мл дистильованої води, додають 3 мл концентрованої сірчаної кислоти і перемішують. Додають 10 мл пероксиду водню (30 %) і доливають до мітки дистильованою водою. Розчин зберігають у прохолодному темної місці і використовують протягом одного місяця після приготування.
Розчин ФДК готують у такий спосіб. У колбу Кьєльдаля поміщають 150 мл сірчаної кислоти питомої ваги 1,84, потім додають 25 г фенолу і нагрівають на водяній бані до розчинення фенолу. Після охолодження додають 75 мл сірчаної кислоти, що димить, (олеум, зі змістом SO3 не менш 30 %) і нагрівають на водяній бані протягом двох часів. Прохолоджують і зберігають у темній пляшці.
Для приготування стандартного розчину 0,451 г азотнокислого калію, висушеного протягом 2 г при температурі 105 - 110 oС, розчинять у літровій мірній колбі дистильованою водою. 10 мл цього розчину поміщають у мірну колбу ємністю 100 мл і доливають до мітки дистильованою водою. 1 мл стандартного розчину відповідає 0,01 мл діоксиду азоту (0 oС, 760 мм рт. ст.) або 0,0205 мг діоксиду азоту. Розглянутий метод визначення концентрації оксидів азоту в димових газах заслуговує на увагу завдяки високій точності визначення (ступінь уловлювання 93 %), але вимагає великих витрат часу на окислювання і на підготовку робочого розчину до колориметрування.
Хімічний метод з використанням реактиву Грісу простий у виконанні і не вимагає дорогих і важкодоступних реактивів. При цьому він специфічний, тому що вплив супутніх компонентів усувається застосуванням спеціальних поглиначів, а робочі розчини з відібраної проби протягом тривалого часу зберігають сталість властивостей.
Після попереднього окислювання оксид азоту у вигляді азотної кислоти вступає в реакцію утворення барвника у водному розчині реактиву Грісу, що складається із сульфанілової кислоти і ?-нафтіламіна. Сульфанілова кислота при взаємодії з нітрит-іонами утворює діазосполучення, що легко перетворюється із ?-нафтіламіном в азобарвник зі стабільним фарбуванням, пропорційним вмістові нітритів в аналізованій пробі. Механізм визначення азобарвника може бути представлений наступною схемою:

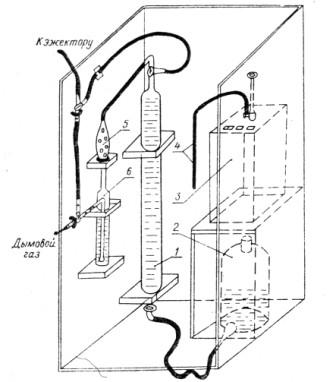
Методика визначення. Схема установки для визначення концентрації оксидів азоту представлена на рис. 2. Газ, що відбирається із газоходу, пропускається через фільтр із скловати 1 для затримки твердих часток і поглинальний сосуд із хлористим кальцієм 3 для поглинання водяних парів. У випадку газів з високим змістом сірчистого ангідриду (при вмісті сірки в паливі понад 2 %) газ пропускається через промивну судину (склянка Дрекселя) з 20 %-ним розчином гідроксиду калію 2.

Далі гази проходять через спеціальні сосуди з убудованим елементом 4, у які вводиться барвник (2 %-ний розчин перманганату калію + 15 %-ний розчин ортофосфорної кислоти). Для обраних розмірів сосуду 4 оптимальна витрата аналізованих газів, що забезпечує повне протікання реакції окислювання оксиду азоту до діоксиду азоту дорівнює 0,1 - 0,3 л/хв. Підтримка зазначеної витрати забезпечується за реометром 9. Окислений газ через пастку 5 надходити в газову мірну піпетку 7, ємністю 50 - 100 мл. У піпетку 7 з відібраною пробою після її відключення від системи вводять реактив Грісу (10 - 15 мл). Визначення оптичної щільності пофарбованого розчину роблять на фотоелектроколориметрі із зеленим світлофільтром при довжині хвилі 520 нм після повного розвитку фарбування (через 20 хв). Тривалість визначення, включаючи операцію добору проби, складає 20 - 30 хв. При роботі з реактивом Грісу необхідно мати на увазі, що фарбування з часом підсилюється, тому визначення оптичної щільності варто робити через визначені проміжки часу. Після початку реакції посилення ступеня фарбування розчину спостерігається протягом 20 хв і залишається постійним протягом 24 г.
Для одержання відтворених результатів необхідно, щоб в аналізованому газі не були присутні високі концентрації сильних газоподібних окислювачів і відновників, що може бути досягнуто введенням у схему добору спеціальних поглиначів, що дуже незначно занижують результати аналізу, поглинаючи частково з газу діоксид азоту. В газі утримується не більше 3 - 5 % діоксиду азоту, тому цим можна зневажити.
Для відносної оцінки вмісту оксидів азоту в топкових газах розроблений експрес-метод лінійно-колористичного визначення індикаторними трубками газоаналізатора УГ-2. Принцип роботи газоаналізатора типу УГ-2 заснований на вимірі довжини пофарбованого стовпчика, отриманого в процесі проходження через індикаторну трубку газу, що містить оксиди азоту. Індикаторні трубки заповнюються порошком, що являє собою реактив Грісу, що нанесений на силікагель. Довжина пофарбованого стовпчика індикаторного порошку в трубці пропорційна концентрації діоксиду азоту в газі. Приладом УГ-2 можна визначити концентрації оксидів азоту в газі до 200 мг/м3, а оскільки концентрації в топкових газах звичайно перевищують 200 мг/м3, варто розбавляти газ повітрям і вже потім робити аналіз.
Для аналізу газу приладом УГ-2 при розведенні аналізованої проби повітрям необхідна спеціальна приставка, основним елементом якої є аспіратор і ряд поглинальних сосудів для очищення газу (рис. 3). В якості замикаючої рідини рекомендується використовувати насичений розчин NaNO3.
Добір і розведення газу повітрям здійснюють у градуйованій бюретці, в якій точно фіксуються обсяги газу і повітря при атмосферному тиску. Газ при зіткненні із замикаючою рідиною швидше прохолоджується, швидше відбувається конденсація пара, краще очищається від твердих часток. Все це необхідно для дотримання технічних умов на прилад УГ-2.
При вимірі концентрацій оксидів азоту в топкових газах варто застосовувати порошки однієї дати випуску і використовувати індикаторні трубки з внутрішнім діаметром 2,55 мм. Для правильної оцінки вмісту оксидів азоту в газі приладом УГ-2 необхідно виконати кілька визначень при різних кратностях розведення газу повітрям і для кожної партії визначити оптимальний час контакту аналізованої газової суміші з порошком. З отриманих результатів потрібно взяти середнє арифметичне значення.
Для зменшення погрішності визначення за експрес-методом кожна партія індикаторних порошків повинна пройти перевірку на каліброваних газових сумішах. У результаті калібрування індикаторних порошків можуть бути встановлені деякі залежності у вигляді коефіцієнтів, за допомогою яких уточнюють розрахунок.
Метод визначення за допомогою індикаторних трубок газоаналізатора УГ-2, незважаючи на простоту, може призвести до істотних помилок, якщо не враховувати такі фактори, як межа чутливості виміру, спосіб приготування порошків, кратність розведення аналізованої проби і час контакту газу з індикаторним порошком.
Для повсякденної практики рекомендується використовувати метод, заснований на застосуванні реактиву Грісу, тому що він має найбільшу чутливість і для його виконання потрібні найменші витрати часу.