Материалы по теме выпускной работы: Реферат | Библиотека | Ссылки | Отчет о поиске | Индивидуальное задание
Сравнительные количественные исследования взаимоотношений структурной деятельности (КВСД) по небензодиазепиновым соединениям, связанным с бензодиазепиновым рецептором (БзР)
Д. Хаджипавлоуитина, Райни Гарг и Корвин Ханш
Отдел Фармацевтической Химии, Школа Фармацевтики, Салоникский Университет Аристотеля, Салоники, Греция, Отдел Химии, Университет Кларксон, Потсдам, Нью-Йорк 13699-5810, и Отдел Химии, Помона Колледж, Кларемонт, Калифорния 91711
1. Введение
Бензодиазепины (БЗД) являются альтернативными наркотиками в фармакотерапии лечения беспокойства и соответствующих эмоциональных проблем, бессонницы, состояния эпилепсии, и других конвульсивных состояний; они используются в качестве релаксантов для центральных действующих мышц, как предварительное средство, и как стимулирующие агенты в анестезиологии. Они действуют благодаря бензодиазепиновому рецепторному участку (БРУ) на семейство γ-аминобутириковый кислотный рецептор (GABAa) и были подвергнуты обширным количественным изучениям взаимоотношениям структурной деятельности (КВСД).1-4 Подавление GABAer-gic является одним из самых быстро развивающихся вопросов в неврофармакологии.5a Возникают новые терапевтические возможности благодаря увеличению понимания в молекулярном строении и разнообразию компонентов, вовлеченных в сигнальную трансдукцию, таких как рецепторы GABAa, рецепторы GABAb, and транспортеры GABA. Рецепторы GABAa являются главными тормозными невро-ротрансмиторными рецепторами в мозгах, на месте действия главных клинических важных наркотиков, и являются главными наркотическими целями, представляющими участки действий бензодиазепинов, барбитуратов, и нерво-стероидов. Эти рецепторы являются лигатурно-шлюзными хлоридными каналами, состоящими из пяти подединиц, которые могут принадлежать к восьми различным классам подединиц. Все подединицы обладают экстра-клеточной амино-предельной областью, содержащей консервированный дисульфидный мост, следующий за четырьмя Ирансмембранными сегментами. Рецепторы GABAa принадлежат к суперсемье пентамерических лигатурно-шлюзовых ионных каналов ("рецепторы циклопетли").5b При синапсисе рецепторы GABAa активируются кратким неуравновешивающему воздействию высоких концентраций GABA. На основе присутствия 7 подединичных семейств, включающих по меньшей мере 18 подединиц в центральной нервной системе (α 1-6, β1-3, γ1-3, €, θ, ρ1-3), рецепторы GABAa показывают чрезвычайную структурную разнородность. Большинство подтипов рецепторов GABAa в реальности кажутся состоящими из α-, β-, and γ-подединиц. Думают, что бензодиазепиновый участок должен быть расположен на интерфейсе соответствующей α-подчастицы (α 1-3, α5) и γ2-подчастицы. Классический бензодиазепиновый участок в основном находят на рецепторах GABAA на интерфейсе α- и γ2-подчастиц и могут оказаться нечувствительным диазипамом к точке мутации в a-подчастице, в которой хистидиновый остаток помещается к аргининовому остатку в рекомбинантные рецепторы.5с
Если БЗД связать с их рецепторами, они оказываются стимулирующими структурную замену, ведущую к увеличению пригодности рецепторов GABAa для рецепторов GABAa, ведущих к повышенному хлоридному притоку и гиперполяризации. БЗД взаимодействует с двумя классами распознавательных мест, "центральных" и "периферийных" (митохондриал) типов. До недавнего времени новая низкая близость диазепинового участка идентифицировалась по рекомбинантным рецепторам GABAa (α1β3γ2).5b
Рецепторы, содержащие α1-5-подчастицы в сочетании с любыми β-подчастицами и γ2-подчастицей, являются самыми распространенными в мозге. Данные рецепторы чувствительны к бензодиазепиновой модуляции. Главным рецепторным подтипом, собранных из подчастиц α1β2γ2 (диазепам-чувствительных рецепторов GABAa). Рецепторы GABAA , которые не отвечают клинически используемым лигандам, таким как диазепам, флунитразепам, клон-азепам, и золпидем, являются изобильным потоком в мозгах и значительно характеризуются α4- и α6-подчастицами (диазепам-чувствительных рецепторов GABAa). L-838.417.SL65.149, и CL 284,846 являются некоторыми новыми подтипами-селективных бензодиазепиновых местных лигандов, принимая во внимание что |3H]RY 80 может использоваться в качестве радиолиганд для проверки свойств рецепторов GABAa, содержащих α5 подчастицы.5d
Центральные рецепторы, размещенные на нейронных тканях 6,7a,b являются функционально связующими с хлоридно-ионофорным комплексом рецептора GABAa 7 и очевидно размещенным на синапсических мембранах.8 Центральные рецепторы БЗД служат связующим звеном классических фармакологических свойств клинически широко используемых БЗД6 (анксиолитических, противоконвульсивных, седативных, и мышечных релаксантов). Независимые GABAA-9'10 периферические или "митохондрические" бензодиазепиновые рецепторы (МБР) идентифицировались в широком спектре периферийных тканей также как в центральной нервной системе,11 а об их подклеточном размещении докладывалось главным образом как об "митохондрической",l2-14 ядерной,10,11 и в плазматической мембране.15,16 В течение последнего десятилетия МБР было объектом некоторых исследований, нацеленных на понимание его физиологической роли. Периферийный бензодиазепиновый рецептор (ПБР) является мульмерическим протеиновым комплексом, размещенным на внешней милохондрической мембране астроглиальных клеток и выражен как в центральных, так и периферийных тканях. Физиологическая роль митохондрического БЗР все еще не выяснена. Селективные ПБР лиганды на сегодня известны, как принадлежащие к структурно несоответствующим классам соединений, таких как БЗД, изоквины, имидазопиридины, 2-арил-3-индолеацетамиды, бензофурацетамиды, и бензотиазепины. Они вовлечены в различные клеточные функции, такие как торможение оксидативной фосфориляции,9 торможение клеточной пролиферации, и стероидогенезиса.16,17 БЗР являются уникальными в отношении того, как они соответствуют трем различным типам лигандов, которые действуют как аллостерические модуляторы комплекса рецепторов GABAa. GABA-или бензодиазепиновые стимулирующие структурные изменения, имеющие начало в экстра-клеточной области и трансдукцирующие на другие, аллостеричные связанные участки и ионный канал. Считают, что первоначальный импульс, который управляет аллостеричным движением, влечет за собой некоторую переустановку непосредственно в связующем участке. В действительности, аллостеричные модуляторы могут либо увеличить (агонизирование) или уменьшить (инверсию агонии) GABAA-побуждающих ионный приток Cl-. Третья группа лигандов, взаимодействующих с аллостеричным участком рецептора GABAa, не влияет на побуждаемый GABAA-ионный приток, но антагонизирует (антагонисты) действия агонизаторов и инверсии агонизаторов. Взаимная связь данных трех типов БЗР лигандов может быть объяснена на основании изменений в структуре рецептора с его незанятого положения в состоянии покоя.18,19 Аргумент для однородности связующих участков БЗР может находиться в деятельности, демонстрируемой после малых структурных модификаций соединений с подобными связующими взаимодействиями. Таким образом, все соединения, которые связаны с БЗР, должны иметь определенные общие характеристики, позволяющие для распознания рецептором, невзирая на тип деятельности. Многие показанные типы соединений для связи с БЗР, например, БЗД, арилпиразоло-квинолины, β-карболины, имидазопи-ридазины, и цикло-пирролоны. Считают, что агонисты БЗД связаны с участками, ассоциируемыми с рецептором GABAA, ионным каналом связующего рецептора. GABAa действует на по меньшей мере два различных рецепторных типа.20-24 Действие БЗД кажется ограниченным синаптическими эффектами GABAa, которые связуются рецепторами GABAa. Структурная форма рецепторного комплекса, связующего агонистов БЗД (например, диазепам) имеет малое сродство для GABAa на его ассоциируемом участке. Равновесие является структурной формой рецепторного комплекса, связующего инверсивные агонисты БДЗ (например, β-карболины), которые имеют слабую близость для GABAa и, таким образом, не ассоциируются с открытием ассоциированного ионного канала. Наркотики-антагонисты на БЗР предотвращают связывание либо агонистов или инверсивных агонистов. В настоящее время, только два различных подтипа БЗР, БЗ1Р и БЗ2Р, могут быть различимы фармакологически.
Сравнительное моделирование (синонимичное с термином "гомологическое моделирование") базируется на наблюдении, что в семействах протеиновых, структура больше сохранена, чем ее последовательность. Благодаря отсутствию некоторых больших боковых цепочек, объем бензодиазепиновой зоны больше, чем у такой же зоны GABAa. Соперничающие агонисты препятствует действию связывания в частично накладывающейся зоне. По той причине, что они больше чем агонисты, зональная геометрия требует, чтобы они расширялись в дальнейшем в ближайшую мембрану равной расщепления и таким образом блокировали аллостерические изменения, которые повлекут за собой движение на дополнительной стороне основной стороны.5b Молекулярные механические подходы, комбинирующиеся со сравнительным моделированием, могут предоставить дополнительную и комплектующую информацию по отношению к структурным изменениям, предлагаемым от электронного кристаллографического исследования. Исследования молекулярного моделирования25 установили, что все лиганды БЗД делятся по присутствию в них ароматических или гетероароматических A колец, которые считаются подверженными π/π складированию с ароматическими аминокислотными остатками внутри рецептора, также как и протоно принимающая группа, которая существует в той же плоскости ароматического A кольца и взаимодействует с хистидиновым остатком на рецепторе. 5-фенил ароматическая группа, C, может способствовать стеричному или гидрофобическим взаимодействиям с рецептором. Для агониста, замещение пара-позиции на кольце C является стерически неблагоприятным. Амид азота, его метиловый заместитель, и 4,5-(метиленеймино) группа не требуется в витро- связывании лигандов. Замещение 3-х позиционного метилена или имина азота является стерически неблагоприятным для деятельности агониста, но не влияет антагонисты.
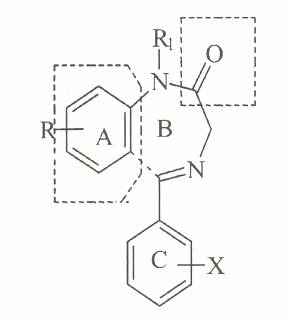
В продолжение к нашим предыдущим исследованиям количественно-структурных 4 по БЗД, мы представляем новое исследование КВСД по некоторым не-БЗД связям с рецепторами GABAA/БЗ.