 |
Англійський
|
Англійський
 |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Про автора
Про автора
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Реферат за темою випускної роботиАктуальність роботи полягає в наступному: 1) Відсутня інформація про масштаби забруднення фторидами і нітратами біологічних об'єктів; 2) Помітна біологічна активність і висока токсичність фторидів і нітратів роблять необхідним вивчення процесів їх трансформації і міграції. Мета роботи – визначення вмісту фторидів і нітратів в природних водах селитебных територій Донецької області. Наукова новизна – вперше здійснити оцінку масштабів забруднення природних вод нітратами і фторидами з використанням карт-схем. В задачі досліджень входило: 1) збір і аналіз інформації щодо шляхів надходження, токсичності нітратів і фторидів, а також методів визначення їх вмісту в природних водах селітебних територій Донецької області; 2) відбір і аналіз проб води; 3) обробка результатів дослідження проб води; 4) складання карт-схем, які описують масштаби забруднення нітратами і фторидами. Гострою проблемою нашого часу є неконтрольоване забруднення навколишнього середовища, пов'язане з діяльністю людини. Особливо небезпечним є забруднення водних ресурсів, зокрема питних в селітебних районах, оскільки їх запаси обмежені. Українці отримують питну воду не тільки з систем централізованого водопостачання. Приблизно третина населення країни користується водою з підземних джерел. Це, як правило, сільські колодязі. Ґрунтові і підземні води часто використовуються населенням для питних цілей, проте саме вони мають тенденцію до акумуляції токсичних забруднень. У зв'язку з цим доцільними є дослідження і контроль підземних вод, які використовують для питних цілей. НітратиАнтропогенні джерела нітратів підрозділяються на аграрні (мінеральні і органічні добрива, тваринницьке виробництво), індустріальні (відходи промислового виробництва і стічні води) і комунально-побутові (використання осадків стічних вод як добрива або з метою меліорації земель). Разом з розглянутими вище аграрними джерелами збільшення рівня нітратів в агроландшафтах може бути обумовлене і іншими формами сільськогосподарської діяльності. Так, заміна традиційних систем землеробства з участю і чергуванням різноманітних культур інтенсивнішими і спеціалізованими технологіями, які сприяють посиленню мінералізації органічної речовини ґрунту і руйнуванню її структури, обмеження площ, зайнятих травами, відкриття кормових угідь під постійну ріллю, підвищення ваги машин і їх використання на постійних технологічних коліях, відсутність захисних зон навколо полів приводять до посилення винесення азоту поверхневого і того, що знаходиться усередині ґрунту. Введення в сівозміни чистої пари сприяє інтенсивній утворенню і накопиченню нітратів в ґрунті, які можуть втрачатися при тривалому випаданні опадів або короткочасних, але рясних зливах. Втрати нітратів з ґрунту зростають при насиченні сівозмін просапними культурами, агротехніка яких вимагає великого числа міжрядних обробок. Як непрямий чинник, який збільшує вірогідність винесення нітратів з дренажним стоком з ґрунту, можна розглядати вапнування ґрунту, яке стимулює мінералізаційні процеси. Концентрація нітратів у водоймищах зростає при меліорації перезволожених земель і в перші роки їх сільськогосподарського використання. Найбільш високий рівень нітратів виявляється в магістральних водостоках, що приймають дренажні води. Тривале сільськогосподарське використання осушених земель приводить до деякого підвищення вмісту нітратів і в ґрунтових водах. Токсичний вплив на людинуВиявлено два способи окислення гемоглобіну HbFe2+. При прямому окисленні роль окислювача грають нітрит-аніони [4]: Під час непрямого окислення гемоглобіну спочатку нітрити окислюються до нітратів з утворенням пероксиду водню, потім останній вступає в реакцію із залізом гемоглобіну [4]: HbFe2+ + 2Н2О2 + 4Н+ → HbFe3+ + 4Н2О. Загрозою для життя є накопичення в крові 20% і більш за метгемоглобіну (HbFe3+). Найбільша ж небезпека підвищеного вмісту нітратів в організмі полягає в здатності нітрит-іона брати участь в реакції нітрозування амінів і амідів, в результаті якої утворюються нітрозосполуки, що мають канцерогенну і мутагенну дію. Утворення нітрозосполук відбувається при взаємодії азотистої кислоти з вторинними амінами як в продуктах харчування в процесі їх кулінарної обробки, так і всередині організму [4]: N-нітрозосполуки мають загальну структуру: 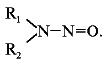 Особливо небезпечна MtHb для дітей – понижена кислотність шлункового соку призводить до розвитку мікроорганізмів-редуцентів [1]. Виділяють три основні клінічні форми MtHb: безсимптомну – вміст MtHb до 5%; легку – MtHb до 5 – 10% з ціанозом, тахікардією; і важку MtHb – до 20% з ціанозом, тахікардією, нудотою, блюванням, головними болями. За взаємодії нітритів з амінопохідними сполуками утворюються потенційні канцерогени – N- нітрозосполуки (НС), які включають N-нітрозоаміни. Останні є потенційними канцерогенами. Крім злоякісних новоутворень, НС характеризуються органотропною, мутагенною, ембріотоксичною і тератогенною дією. Нітрати з організму людини виводяться лише на 70 – 80%. ДСД нітрозо амінів – 1 мкг/кг, нітратів для дорослого населення – 5 мг/кг. Токсичний вплив на рослиниНітрати, які поступили в рослини, відновлюються за схемою: 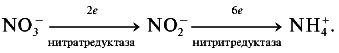 Перший етап відновлення нітрату протікає відповідно за рівнянням [4]: 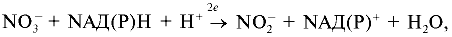 где NAД(Р)H – нікотинамідаденіндінуклеотидфосфат відновлений, NAД(Р)+ – нікотинамідаденіндінуклеотидфосфат окислений. Нітратредуктаза – фермент класу оксидоредуктази, яка синтезується в клітках у відповідь на надходження NO3-; на нього особливо багате молоде листя і кінчики коріння [4]. Нітрит, що утворюється, не накопичуються, а швидко відновлюються до NH4+ за допомогою ферменту – нітритредуктази: 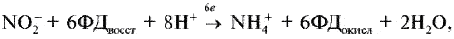 где ФД – ферредоксин – залізовмісний білок, що виконує функції перенесення електронів. В таблиці 1 приведені середні і граничні масові долі нітрат-іона в продуктах харчування [5]. Таблиця 1 – Масові долі нітрат-іона в продуктах харчування
З таблиці виходить, що немає жодного продукту харчування, в якому допускається не контролювати вміст нітратів. Цей висновок в рівній мірі відноситься і до води, особливо колодязної [5]. Токсичний вплив на гідробіонтиПоведінка нітратів в ґрунтіПідпорогова концентрація нітратів у воді, що визначають за органолептичним показником – 400 мг/л [1]. Вважають, що одним з небезпечних видів забруднення водних джерел є забруднення сполуками азоту. У більшості грантів основним азотним іоном-мігрантом є NO3-, що зумовлено його надзвичайно високою мобільністю. Водна міграція при цьому є переважаючою формою. Процеси механічної, фізико-хімічної та хімічної адсорбції цього іону незначні, їх спостерігають у дуже кислих ґрунтах, де переважають мінерали типу каоліну. Найбільшу вертикальну міграцію спостерігають на ґрунтах легкого механічного складу з низькою поглинальною здатністю. Важливе значення має те, що внесення мінеральних добрив збільшує мінералізаційну здатність ґрунту, чим підсилює вертикальну міграційну здатність NO3- ґрунтового походження. Азот добрив при цьому фіксується ґрунтовим комплексом і його міграція проявляється меншою мірою. У більшості ґрунтів серед багатьох показників, від яких залежить міграційна здатність NO3- (механічний склад, вид культури, вологість ґрунту, мікробіологічна активність, дози азотних добрив) за однакових інших умов, вплив азотних добрив виявився переважаючим [1]. Нітратний азот здатний вимиватися з інфільтраційними водами на значну глибину. Дослідженнями, проведеними на чорноземі опідзоленому при тривалому застосуванні добрив (35 років) було встановлено вимивання нітратів на глибину близько 10 м з максимумом нагромадження на глибині 2-4 м. П. Копитко (1999 р.) вказує, що в інтенсивних плодових насадженнях нітрати можуть мігрувати на глибину 25 м. Методи визначенняНормативні документи: для питних вод ГОСТ 4192-82, для мінеральних вод ГОСТ 23268. 8-78, для стічних вод ПНД Ф14.1:2:3-95. Метод може застосовуватись для визначення нітриту в поверхневих водах із вмістом від 0,007 до 0,35 мг N/л [2]. Метод заснований на здатності первинних ароматичних амінів у присутності азотистої кислоти давати інтенсивно забарвлені діазосполуки. Оптичну щільність утвореної діазосполуки визначають при X= 536 нм. Лінійна залежність між оптичною щільністю розчинів і концентрацією нітриту зберігається в межах від 0,007 до 0,350 мгN/дм3. Мінімальна визначувана концентрація 0,007 мгN/дм3. Відносне стандартне відхилення U при концентраціях від 0,080 до 0,300 мгN/дм3 складає 2%, при концентраціях < 0,080 мгN/дм3 — 10%. Тривалість визначення одиничної проби 50 хв. Серія з 6 проб визначається протягом 1 год. [2]. Визначенню заважають сильні окислювачі і чи відновите в концентраціях, що рідко зустрічаються в природних водах. Дія тривалентного заліза, двовалентної ртуті, срібла, вісмуту, тривалентної сурьми, свинцю, тривалентного золота, хлорплатинатів і метаванадатів в сильно-забруднених водах усувається розбавленням досліджуваної проби дистильованою водою, яка не містить нітриту. 2 Потенціометричний [6, 9] Суть методу: нітрати в досліджуваному розчині визначають по зміні ЕДС ланцюгу, який складається з нітратселективного електроду, електроду порівняння, вимірювального осередку з досліджуваним розчином і лабораторного рН-метра або іономера. Метод застосовують при визначенні масової концентрації нітратів від 50 до 500 мкг/дм3. Нижня межа виявлення складає 25 мкг/дм3 [6]. Електрод вимірювальний нітратселективний з електричним опором 0,1-0,9 мОм в діапазоні молярних концентрацій нітратів С від 10-4 до 10-1 моль/дм3 крутизна електродної характеристики (55±4) мВ/рС. Електрод заповнюють розчином азотнокислого калія з молярною концентрацією 10-1 моль/дм3. Перед вимірюванням електрод витримують протягом 24 ч в розчині азотнокислого калія з молярною концентрацією 10-4 моль/дм3 [6]. ФторидиВ організм людини фториди поступають з водою, продуктами харчування, лікарськими препаратами, пестицидами, і значна їх частина є результатом діяльності людей [10]. Токсичний вплив на людинуҐрунтТоксичний вплив на рослини і мікроорганізмиТоксичний вплив на гідробіонтиМетоди визначення– варіант А – заснований на здатності фторид-іона утворювати розчинний в воді потрійний комплекс бузково-синього кольору, до складу якого входить лантан, алізаринкомплексон і фтор. Інтенсивність забарвлення розчину фотометрують при довжині хвилі λ = (600±10) нм [3]. Визначенню фториду сильно заважають алюміній і залізо, зв'язуючи його в комплекс і занижуючи результати. Допустима масова концентрація алюмінію не вище 0,2 мг/дм3, заліза – не вище 0,7 мг/дм3. – варіант Б – заснований на тому ж принципі, що і варіант А, але для підвищення оперативності вимірювання оптичної щільності визначення проводять у водно-ацетатному середовищі, в якому повнота розвитку забарвлення потрійного комплексу лантану, алізаринкомплексона і фториду досягається через 15 хв. 2 Потенціометричний [3] Метод дозволяє визначати сумарну концентрацію фторидів (усіх його форм: іона фториду, його комплексних сполук). Для визначення використовують електродну систему, що складається з фторидного іонселективного електроду і допоміжного хлор-срібного електроду. Вимірювання потенціалу фторидного електрода проводять високоомним рН-метром-міллівольт-метром, замінивши скляний електрод на фторидный, або приладом іономером (нітратомером). Визначення можливе при масовій концентрації алюмінію не вище 40 мг/дм3, заліза – не вище 40 мг/дм3 [3]. Дослідження водиОдним з найбільш швидких і точних методів, за допомогою якого визначають вміст нітратів, є метод прямої потенціометрії з використанням іонселективних до нітрат-іонам електродів [6, 9]. Прилад, принцип дії якого заснований на цьому методі, називається нітратомером (іономером) (рисунок 1). 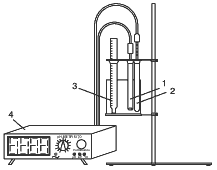 1 – нітратселективний електрод; 2 – допоміжний електрод; 3 – термометр; 4 – іономер. Рисунок 1 – Схема установки для анализа Дані по вмісту нітратів в пробах води з різних водних джерел області приведені в таблиці 2. Таблиця 2 – Вміст нітратів в пробах води з різних водних джерел
На рисунку 2 показана кількість проб води з перевищенням вмісту нітратів від загальної кількості аналізованих проб води. 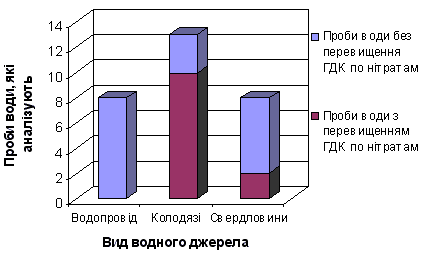 Рисунок 2 – Відношення проб води з перевищенням ГДК по нітратах до загальної кількості проб води Дані, які були отримані, свідчать про те, що 77% проаналізованих зразків води з питних колодязів мають вміст нітратів вище за ГДК (для нітратів складає 45,0 мг/л). Цей показник в аналізованій воді в 2,00 – 11,0 разів перевищує ГДК (порівняльна характеристика наведена на рисунках 3, 4). 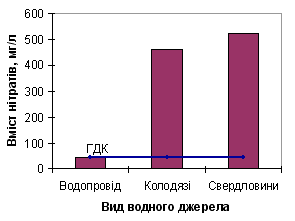 Рисунок 3 – Порівняння середнього вмісту нітратів у пробах води з різних водних джерел 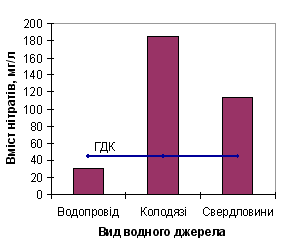 Рисунок 4 – Порівняння масимального вмісту нітратів у пробах води з різних водних джерел Найбільший вміст нітратних іонів встановлений у воді колодязів с. Желане (Ясинуватський р-н) – в 11 разів перевищення ГДК – і в с. Червоне (Красноармійський р-н) – в 7 разів перевищення ГДК. Також встановлено, що в колодязній воді спостерігається коливання вмісту нітратів – від 3,1 до 460,0 мг/л, у воді зі свердловин – від 2,6 до 525,0 мг/л. Таким чином, контроль за вмістом нітратів і фторидів у воді є важливим завданням. Зменшення надходження азоту в геологічний кругообіг можливе при вживанні наступних заходів: 1 посилення біологічного кругообігу шляхом нормованого застосування добрив; 2 рівномірного їх розподілу по поверхні полів; 3 обробки схилів так, щоб максимально знизити поверхневий стік. ПРИМІТКА. При написанні даного автореферату магістерськая робота ще не завершена. Остаточне завершення: грудень 2009 р. Повний текст роботы і матеріали за темою можуть бути отримані у автора або його керівника після вказаної дати. Література
© ДонНТУ 2009 Прокопенко Наталя Юріївна
|
 Про автора
Про автора
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||