
Факультет экологии и химической технологии
Специальность: Химическая технология высокомолекулярных соединений
Практическая ценность результатов работы заключается в разработке методики изучения физико-химических свойств процессов кристаллизации и плавления высокомолекулярных веществ в условиях университетской лаборатории. Работа с изучаемыми веществами является опасной, поэтому требует специальных условий, которые в данное время предоставляет Донецкий казенный завод химических изделий, что составляет трудности и неудобства для студентов и предподавателей. Выходом является выбор веществ, схожих по свойствам с тринитротолуолом, а также разработка оборудования для проведения опытов.
Актуальность. Выполненная работа позволит проводить большее количество практических занятий для изучения материала при более безопасных и материально выгодных условиях.
1 ВЫБОР ОРГАНИЧЕСКОГО ВЕЩЕСТВА, КОТОРОЕ ИМЕЕТ ТЕМПЕРАТУРУ ПЛАВЛЕНИЯ ДО 100oC.
1.1 Тринитротолуол
Тротил – это кристаллическое вещество бледно-желтого цвета, относится к бризантным взрывным веществам.1.2 Нафталин
Нафталин-С10Н8 твердое кристаллическое вещество с характерным запахом, который в воде не растворяется, но хорошо – в органических веществах: бензоле, эфире. Перегоняется с водным паром.
Н. (от грецьк. naphtha – нефть), ароматический углеводород; температура плавления 80,3 оС, температура кипения 218 оС; летающие, возгоняются при 500 оС; плотность 1,15-17 г/см3 (150 оС).
Н. по химическим свойствам согласный с бензолом: легко нитруется, сульфируется, взаимодействует с галогенами. Отличается от бензола тем, что легче вступает в реакции.
В промышленности Н. получают в основном с каменноугольной смолы (которой его 8-10%), а также выделяют из продуктов пиролиза нефти. Последний значительно чище каменноугольного. Н. легко вступает в реакции электрофильного замещения (например, галогенирование, нитрование, сульфирования, алкирования). При этом скорость замещения в a-положении больше, чем в b-положении, однако b-размещении Н. термодинамически стабильнее a-размещенных. Поэтому обычно получаются смеси изомеров, состав которых зависит от характера реагента, катализатора, растворителя, температуры, времени реакции и других факторов. При хлорировании Н. на холоде в присутствии FeCl3 получаются a-хлорнафталин и 1,4- и 1, 5-дихлорнафталины; при взаимодействии с хлористым ацетилом в присутствии AlCl3 в хлорэтане получается a-ацетилнафталин, а в отсутствии растворителя – смесь a- и b-производных; сульфирование при низких температурах дает нафталинсульфокислоту, которая при нагревании переходит в изомер. Дальнейшее сульфирование приводит к смеси ди- и полисульфокислот Н.; при этом не образуется сульфокислоты, которые содержат сульфогруппы в орто-. пара- и пере- (т.е. 1,8 или 4,5) положениях. Нитрирование Н. дает нитронафталин; изомер получается обходными путями.
Гидрирование Н. дает тетралин и декалин, окисление – фталевый ангидрид.
Н. имеет важное значение как исходное вещество для получения большего количества органических пола продуктов (главным образом фталевого ангидрида) и красителей ( на основе нафтолов, нафтиламинов и их сульфокислот).
Ближайшие гомологи Н. – метилнафталины – также есть в каменноугольной смоле и имеют общие с Н. свойства. Их используют, например, для синтеза так называемых регуляторов роста растений; полиметилнафталины – инсектициды; соли сульфокислот гомологов Н. используются в качестве эмульгаторов.
1.3 Гипосульфит
Натрия гипосульфит (натрия тиосульфат) – бесцветные прозрачные кристаллы без запаха с моноклинной решеткой; температура плавления 48,50 оС (с разл.); 1,715 г/см3; солоновато-горький на вкус. Полученные ди- и гомо гидраты, которые плавятся инкогруентно соответственно при 65,5 и 74 оС, а также метастабильные тетра- и гексагидраты.
Очень легко растворяется в воде (1:1), практически не растворяется в спирте. При температуре близко + 500 оС. Гипосульфит плавится в криталлизационной воде. Водный раствор (30%, рН 7,8–8,4) стерилизуют при температуре + 1000 оС на протяжении 30 мин (на 1л раствора прибавляют 20г натрия гидрокарбоната). Гипосульфит натрия оказывает противо токсичную, противовоспалительное и десенсибилизирующее действие.
Как противотоксичное средство гипосульфит натрия используют при отравленнии соединениями мишьяка, ртути, свинца (образовываются неядовитые сульфиты), синильной кислоты и ее солями (образовываются менее отравляющие роданистые соединения), солями йода, брома.
Гипосульфит – восстановитель; сильные окислители с хлором хлора и слабые с йодом в нейтральных растворах. Гипосульфит для удаления хлора при отбеливании тканей, как закрепитель в фотографии, реактив в йодометрии.
1.4 Парафин
Парафин – високоподібна вещество, смесь межевих вуглевонів (алканів) состава от С18Н38 к С35Н72. Температура плавления 40-65 оC, щильність 0,880-0,915 г/см3 (15 оC). Получают главным образом из нефти. П Применяют для приготовления парафинистой бумаги, пропитка дерева в спичечном и карандашном производствах, также как изоляционный материал, химическое сырье и т.д. В медицине используется для парафинолечения. Парафіни представляют собой смесь твердых углеводородов метанового ряда преимущественно нормального строения с 18-35 атомами углерода в молекуле и температурой плавления 45-65 оС. В парафинах обычно удерживается некоторое количество изопарафиновых углеводородов, а также углеводородов с ароматическим или нафтеновым ядром в молекуле.
Парафин – вещество белого цвета кристаллического строения с молекулярной массой 300—450, в расплавленном состоянии имеет малую вязкость. Величина и форма кристаллов парафина зависят от условий его выделения: из нефти парафин выделяется в виде мелких тонких кристаллов, а из нефтяных дистиллятов и дистиллятных рафинатов селективного очищения – в виде больших кристаллов. При быстром охлаждении выделяемые кристаллы мельче, чем при медленном. Парафини инертны к большинству химических реагентов. Они окисляются азотной кислотой, кислородом воздуха (при 140 оC) и некоторыми другими окислителями с образованием разных жирных кислот, аналогичных жирным кислотам, которые удерживаются в жирах растительного и животного происхождения. Синтетические жирные кислоти, полученные окислениям парафина, применяют вместо жиров растительного и животного происхождения в парфюмерной промышленности, при производстве смазываний, моечных средств и других продуктов. Парафіны могут быть выделенные также из других продуктов, напр., с озокерита. В зависимости от фракционного соединения, температуры плавления и кристаллической структуры парафины разделяют на жидкие (температура tпл 27 оC), твердые (tпл = 28—70 оC) и микрокристаллические (tпл > 60—80 оC) – церезины. При одинаковой температуре топ. церезины отличаются от парафинов большей молекулярной массой, густотой и вязкостью. Церезины энергично реагируют с дымной серной кислотой, с соляной кислотой, в то время как парафины реагируют с ними слабо. При перегонке нефти церезины концентрируются в осадок, а парафин перегоняется с дистиллятом. Церезины, которые концентрируются в остатке после перегонки мазута, представляют собой смесь циклоалканов и в меньшем количестве твердых аренов и алканов. Изоалканов в церезине сравнительно мало. По степени очищения парафини разделяют на гачи (петролатумы),которые содержат до 30% (масс.) масел; неочищенные парафины (церезины) с содержанием масел до 6% (масс.); очищенные и высокоочищенные парафины (церезины). В зависимости от глубины очищения они имеют белый цвет (високоочищенные и очищенные марки) или слегка желтоватый и от светло-желтого до светло-коричневого (неочищенные парафины). Для парафина характерная пластинчатая или ленточная структура кристаллов. Очищенный парафин имеет плотность 881—905 кг/м3. Церезины представляют собой смесь углеводородов с количеством углеродных атомов в молекуле от 36 до 55 (от С36 к С55). Их вытягивают из естественного сырья (естественного озокерита также остатков высокопарафинистых сортов нефти, получаемых при ее переработкке) и делают синтетически из окисла углерода и водорода. В отличие от парафинов, церезины имеют мелкокристаллическое строение. Температура плавления 65—88 оC, молекулярная масса 500—700. Парафины широко используют в электротехнической, пищевой (парафины глубокого очищения; tплавл = 50—54 оC; содержание масел 0,5—2,3 % по массе), парфюмерной и другой областях. На основе церезина изготовляют разные композиции в промышленности бытовой химии, вазелины; они используются также как загустители в производстве пластических смазываний, изоляционных материалов электро- и радиотехнику и восковых смесях.
Неочищенные твердые парафины делают методами: 1) обезмасливание гачей и петролатумов – побочных продуктов производства (депарафинизации) масел с применением растворителей (смеси кетона, бензола и толуола, дихлоретан), получая при этом неочищенные парафины (с гача) и церезины (с петролатума); 2) выделение и обезмасливание парафина из дистиллятов высокопарафинистых нефтей смесью кетона, бензола и толуола; 3) кристаллизации твердых парафинов без применения растворителей (путем охлаждения в кристализаторах и фильтропресування). Неочищенные парафины после этого облагораживают с использованием кислотно-щелочного, адсорбционного (контактного или перколяционного) или гидрогенизационного доочистка (для удаления нестабильных веществ, которые окрашивают и имеют мероприятие). Жидкие парафины выделяют из дизельных фракций депарафинизацией с использованием избирательных растворителей (смесь ацетона, бензола и толуола), концертной депарафинизацией (в производстве низькозастывающего дизельного топлива) и адсорбции на молекулярных ситах (выделение жидких парафинов С 10 – с помощью пористого синтетического цеолита).
Анализируя свойства перечисленных веществ, избираем для проведения методики исследования процессов плавления и кристаллизации такие вещества, как парафин и петролатум. Выбор обосновывается их наименьшей опасностью и небольшой температурой плавления [4].
2 ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ ПЛАВЛЕНИЯ И КРИСТАЛЛИЗАЦИИ
2.1 Физико-химические основы процесса плавления
Метод изготовления детонаторов заливкой характеризуется наполнением жидкой массой из ВР в оболочку детонатора которая утверждает и воссоздает монолитный разрывной заряд, который владеет высокой плотностью и механической прочностью. Таким образом физико-химическим процессом представляет собой процесс плавления тротила, и процесс его кристаллизации.
Под плавлением поймут процесс перехода вещества из кристаллического состояния в жидкое. Если твердое кристаллическое вещество нагревать, то по достижению определенной температуры, его температура остается постоянной, а вещество начинает переходить из твердого в жидкое. Это явление и носит название плавления.
Теплота, тратится на переход вещества из кристаллического состояния в жидкое (при температуре плавления), называется скрытой теплотой плавления.
Теплота, которая поглощается веществом в процессе плавления, при охлаждении выделяется в окружающая среды в той же количестве при обратном процессе, называется кристаллизацией.
У твердого кристаллического взрывного вещества молекулы располагаются в узлах пространственной решетки. Молекулы взрывного вещества у кристаллической решетки содержатся силами Ван-Дер-Вальса, которые, кроме того, определенным чином ориентируют молекулы органического взрывного вещества относительно друг друга. При нагревании увеличивается амплитуда теплового колебания молекул вокруг их положения равновесия у решетки. Нагревание приводит к увеличению средних размеров между молекулами и к расширению кристаллу, но не изменяет относительно расположения молекул в кристалле.
Тепловое колебание молекул в кристалле подчиняется закону Максвелла о расположении скоростей молекул. Из этого закона вытекает, что даже при низких температурах я относительно не большой средней кинетической энергии молекул у кристаллической решетки всегда есть некоторое количество молекул, которые в следствии взаимодействия с соседними молекулами имеют как угодно большую кинетическую энергию. Молекула , которая получила на некоторый миг энергию более чем необходимую для того, чтобы вырваться из предыдущего состояния, в котором ее удержат силы Ван-Драл-Вальса, оставляет это состояние и занимает другой, передавая лишнюю энергию другой молекуле. В новом состоянии молекула будет колебаться вокруг своего состояния равновесия к тому времени, пока снова не получит избыточную энергию, которая достаточная для перехода к новому состоянию. Такая схема так называем внутреннего выпаривания молекул.
Молекулы, которые испаряются, перемещаются по узлам кристаллической решетки. Это приводит к нарушению ее идеального порядка: в кристалле, кроме молекул, которые занимают узлы решетки, оказываются подвижные, дислоцированные молекулы и узлы, не заполненные молекулами, свое подобные "отвори". Количество дислоцированых молекул и "дырок" возрастает с повышением температуры и достигает максимума при температуре плавления.
При температуре плавления средний запас кинетической энергии молекул становится на столько большим, а силы Ван-Дер-Вальса, в следствие увеличения расстояния между молекулами, на столько ослабеют, что предоставление веществу нового количества теплоты переводит молекулы из их стойкого состояния в узлах кристаллической решетки и к неустойчивому, и кристаллическая структура разрушается.
Несмотря на те, что кристалл и жидкость представляет собой качественно разные состояния вещества, структура и свойства жидкости во многом подобный структуре и свойствам твердого вещества. При плавлении кристаллического вещества происходит сравнительное небольшое увеличение объема (при плавлении тротила его объем увеличивается приблизительно на 13%, ведь расстояние между молекулами увеличивается не на столько, чтобы могло состояться коренное изменение в строении вещества). Теплоёмкость при плавлении почти не изменяется или увеличивается в незначительных размерах. Таким образом, характер теплового движения молекул вещества во время плавления существенно не изменяется. При температуре, которая не значительно превышает температуру плавления, жидкость способна выдерживать большие разрывные усилия. Жидкость владеет текучестью (как и тротил), это основная особенность отличает ее от твердого тела.
2.2 Физикo-химические основы процесса кристаллизации
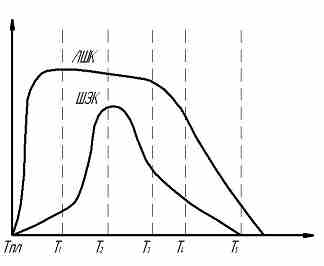
Процесс кристаллизации взрывных веществ, в частности тротила, из расплава до этого времени изученная недостаточно. На основе практических присмотрел можно считать, что для большего количества взрывных веществ, которые используют для заливки, зависимость скорости образования центров кристаллизации и линейной скорости кристаллизации похожая с характером зависимости, что отображенная на рис.2.1. Кривая ШЗЦ достигает максимума позднее чем кривая ЛШК, и идет на снижение раньше, чем кривая ЛШК.
Как что такие вещества кристаллизовать при медленном охлаждении, чтобы ?Т достигло такого же значения, при котором ЛШК уже достигла своего максимума, а ШЗЦ еще имеет незначительную величину (Т1), то выходят крупно хрустальные отливки. Если кристаллизацию вести при охлаждении, достаточного для того, чтобы на протяжении всего процесса поддерживать величину Т на равные, соответствующему максимуму ШЗЦ (Т2), то при этом выйдет отливки с мелкокристаллической структурой.
 |
Рисунок 2.1 – Зависимость скорости создания центров кристаллизации (ШЗЦ) и лилейной скорости кристаллизации (ЛШК) от переохлаждения
При еще более быстром охлаждении, достаточному для поддержки величины Т на равные, что отвечает Т3 или Т4 выходят мелко хрустальные отливки. Если охлаждении вести на столько быстро, чтобы кристаллизация шла при температуре Т5, то отливки будет иметь аморфную структуру с вкрапленными к ней отдельными кристаллами. Таким образом, пение представления или близость положений максимума обеих кривых вещества легко кристаллизуется, и ее тяжело или не возможно получить при охлаждении расплава в аморфном состоянии. Кристаллизация тротила начинается при уравняло небольшом переохлаждении. При охлаждении расплавленного тротила в металлическом бачке емкостью 60 л при беспрерывном перемешивании деревянным веслом изменение температуры расплава происходит приблизительно так, как это изображено на кривой зависимости температуры от времени смешивания на рис 1.2.Такой ход охлаждении тротила возможно объяснить тем, что при температуре до 79,40 оС скорость образования центров кристаллизации практически равняется нулю. Начиная с 97,40 оС, когда Т достигает величины приблизительно 10 оС, кривая ШЗЦ идет доверху, кристаллизация начинается и, в следствие выделения скрытой теплоты кристаллизации, температура взрывного вещества быстро повышается к температуре утверждения.
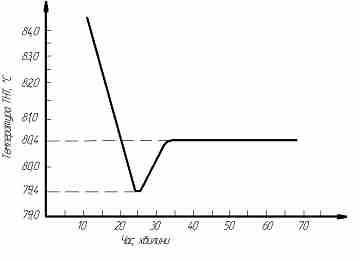 |
Рисунок 2.2 – Кривая охлаждения тротила при перемешивании
При медленном охлаждении расплавленного тротила выходят отливки с крупно хрустальной структурой. Это объясняется тем, что при малых значениях Т скорость создания центров кристаллизации ничтожно имела. Тротил в мелко кристаллическом состоянии может быть получено при очень быстром охлаждении, т.е. в условиях кристаллизации при больших Т.
Если холодную металлическую пластинку погрузить в расплав тротила, то в результате быстрого переохлаждения на ее поверхности образуется тонкий пласт мелко хрустального тротила. Однако получить таким путем разрывные заряды с мелко хрустальным построением невозможно через неосуществимость довольно быстрого охлаждения расплава, залитого в каморру.
Здание отливки, полученной с расплавленного и залитого в холодную оболочку тротила, при чем возникает большое количество центров кристаллизации, образующих тонкий пласт мелко хрустального тротила. Но при дальнейшем выделении скрытой теплоты кристаллизации, малая теплоємкість уже созданной пробки твердого тротила и быстрое увеличение температуры оболочки приводят к росту температуры расплава и его ?Т становится недостаточной для образования новых центров кристаллизации.
Скорость роста грани кристаллу пропорциональная коэффициенту теплопроводности кристаллу в направлении, перпендикулярно возрастающей грани, а также градиенту температуры и назад пропорционально скрытой теплоте кристаллизации и плоскости кристаллу.
Итак, быстрее возрастают те кристаллы, направление максимальной теплопроводности которых совпадает с направлением от стенки оболочки к геометрической оси обращения разрывного заряда. Эти кристаллы быстро опережают своих соседей, оставляют их возможности дальнейшего роста и распространяются по расплаву в виде столбиков, которые перпендикулярные поверхности охлаждения. Таким образом, выходит заряд крупно кристаллического построения с небольшим, прилегающий непосредственно к стенке оболочки, пластом, что созданный с мелких беспорядку ориентированных кристаллов.
Для получения мелкокристаллических разрывных зарядов высокой плотности и достаточной механической прочности расплавленное взрывное вещество к заливке ее в каморру БП или какой-либо изделие насыщают таким количеством центров кристаллизации, которой достаточно для образования мелко кристаллического построения даже в том случае, если утверждение ее будет проходить без образования новых центров кристаллизации. Насыщение расплава центрами кристаллизации является задачей подготовки взрывного вещества к заливке [2].
3 МЕТОДИКА ИССЛЕДОВАНИЯ
3.1 Изготовление расплава
3.1.1 Изготовление расплава в плавителях
Для плавки тротила используются аппараты трех видов: плавильный котел Михайлова, змеевиковый плавник беспрерывного действия и конический плавник.
Плавильный котел Михайлова есть медный луженный сосуд полусферической формы 1 из хромоникелевой постоянные, снабженный паровой рубашкой 2 (рис.3.1).
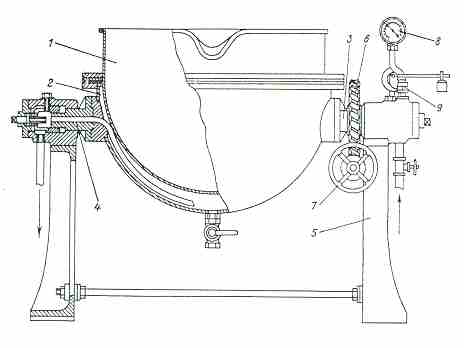 |
Рисунок 3.1 – Плавильный котел Михайлова
В рубашке, которая также имеет форму полусферы, есть две цапфы 3 и 4. Котел опирается на чугунные стойки 5. На цапфе 4 закрепленная шестерня червячной передачи 6, с помощью которой оборачивая штурвал 7, котел при сливу из него расплавленного тротила можно наклонять под любым углом. Подведение пары осуществляется через цапфу 3, а отвод конденсата – через цапфу 4. Для наблюдения за давлением пары, которая поступает в рубашку плавника, котел имеет манометр 8. При плавке тротила давление пара должен быть не более 1,5атм. Чтобы исключить возможность случайного повышения давления пары высшая этого уровня, плавитель имеет предупредительный клапан 9. Для ускорения плавки тротила его треба систематически перемешивать веслом. Преимущества этого плавильного котлу в сравнении с плавниками другого типа: пригодный для плавки не только однородных взрывных веществ, но и для совместного плавления разных компонентов, которые образовывают сплавы, а также для изготовления смесей. Плавители других систем используются только для плавки тротила; плавильный котел легко содержать в чистоте; возможность образования местных перегревов меньше, чем в других плавниках.
Недостатки плавильного котла Михайлова: малая производительность. Котел емкостью 500л дает приблизительно 1500 кг плавленного продукта в шестичасовое изменение; большие затраты ручного труда, так как необходимо постоянно перемешивать расплав; повышенная вредность для рабочих.
Через указанные недостатки плавильные котлы Михайлова в данное время почти полностью вытеснены с производства плавниками других типов.
Змеевиковый плавник беспрерывного действия (рис.3.2) представляет собой железный
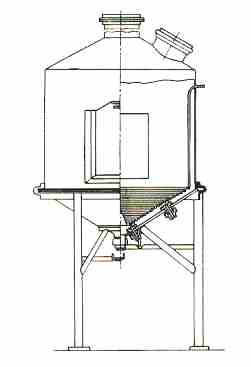 |
Рисунок 3.2 – Змеевиковый плавник беспрерывного действия
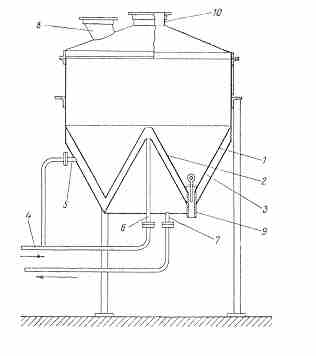 |
Рисунок 3.3 – Конический плавитель Комисарова
3.1.2 Изготовление расплава в лабораторных условиях
Изготовление расплава в лабораторных условиях предусматривает подготовительную работу, что связанная с переводом технологического потока из заводских условий на лабораторные. Поэтому рабочими веществами избираем парафин и петролатум, исходя из их свойств (есть наименее опасными и имеют температуру плавления меньшую чем 100 оС), и в качестве основного оборудования - водяную баню.
Водяная баня состоит из электрической плиты, на которую устанавливается емкость из цветного металла наполненную водой. В воду помещаем стеклянную емкость, в которую последовательно будут помещаться навески из веществ для их дальнейшего плавления. Рядом с плитой устанавливаем штатов с лапкой-держателем, в которую размещаем термометр, рассчитанный на измерение температуры до 100 оC.
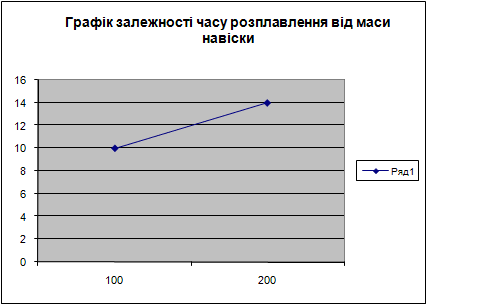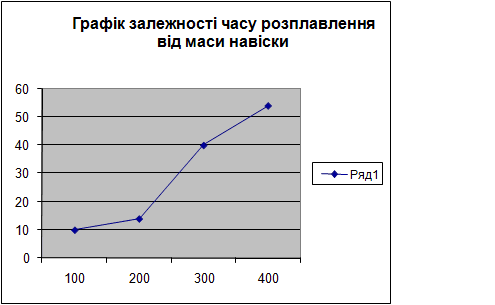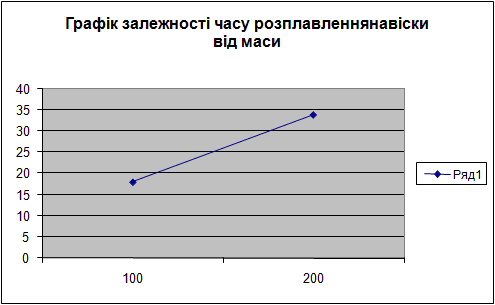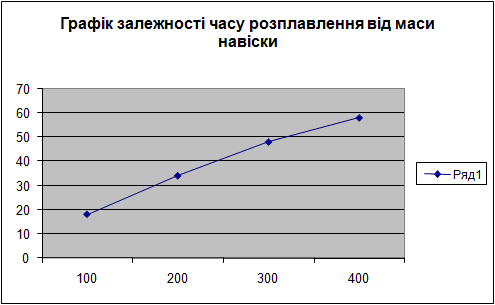
Порядок выполнения работы:
Начинаем процесс из разбивания парафина и взвешивание его на навіски 100 г, 200 г, 300 г,400 г на технических весах. В этот же время на нагретую электрическую плитку устанавливают емкость с водой и нагревают ее к температуре 1000С (температура кипения воды), после чего устанавливают в кипящую воду емкость с первой навеской 100 г. Ведя наблюдение за процессом плавления, фиксируем время полного расплавления навески и температуру расплава в этот момент. Таким же чином расплавляем навески, которые остались.
Повторяем весь процесс для вещества – петролатума.
 |
Количество кадров – 6, Количество повторов – 10
3.2 Кристаллизация расплава
3.2.1 Производство чешуек тротила
Утилизированный тротил привозят со склада или мастерской расснаряжения цеха №1 или №5 в витрачальний погребок автомашиной или трактором с прицепом. Мешки с тротилом разгружают на возки (не больше 12 мешков на возок по 30 кг).В погребке мешки с ТНТ кладут на деревянный лист в штабеле попартийно.
С витрачального погрибка мешки с тротилом транспортируют к мастерской изготовления ДПУ-830 Тл с помощью подвесной дороги. Подвесная дорога представляет собой монорельс , который смонтирован на стойках на высоте 2-3 м от грунта. Движение колыбели по монтажу осуществляется с помощью стального тросу, который приводится в движение с помощью электродвигателя. В погрибке мешки с тротилом нагружают на тележку, в процессе проверяют цельность мешков и наличие маркировки. Маркирование должно быть четким и содержать: обозначение продукта, номер партии, масса нетто, дату паковки. Тележки устанавливают на колыбель подвесной дороги фиксируют тормозным оборудованием и транспортируют к мастерской в отдел подготовки продукта к плавке. Транспортировка осуществляется пола автоматически , т.е. контролирование движения люльки осуществляется рабочим на конечной стойки подвесной дороги. В помещенные приготавления расплава каждый мешок с тротилом проходят входной контроль ( на цельность мешков, на внешний вид тротила ( на отсутствие инородных тел и следов загрязнения)). Из мешков тротил высыпаются в алюминиевый ковш. Загрузка ковша не более 80кг. Если будут выявлены признаки примочки тротила, тогда будет дополнительное рассмотрение мастера отдела технического контроля, и такой продукт не допускается.
Тротил из ковша с помощью пневматической тали загружают в плавитель Комисарова (250–300кг). По мере расплавления тротил из плавника по переходной трубе сливают в смеситель. Температура расплава в смесителе в момент начала ливень тротила должна быть 80–85 оС. Когда уровень расплава в смесителе достигнет 20–25 см от верхнего торца загрузочного люка, подачу расплава прекращают (уровень проверяют визуально через загрузочный люк), перекидную трубу устанавливают над люком пустого смесителя и процесс повторяют. В смесителе расплав тротила подогревают к температуре 82–90 оС при отключенной мешалки.
При достижении расплава необходимой температуры, люк смесителя затворяют крышкой с резиновой прокладкой, затягивают "барашки" крышки с помощью латунного прыткая, и подают краткий воздух ( Р= 0.11 Мпа). После отворения промежуточного клапану, расплав по массопроводу через фильтр передвигается в промежуточную емкость (уровень расплава в емкости равняется 15-25 см от крышки), после этого подачу воздуха в смеситель прекращают, снимают крышку из люка, затворяют промежуточный клапан. Смеситель готовый к приготовлению новой порции расплава.
Чешуирование тротила – особо опасная операция. Она происходит на барабане чешуирования путем его соскабливания из цилиндрических и торцевых поверхностей барабану, который оборачивается. Этот барабан нижней частью погружен в розплавленный тротил, залитый в корыто.
Включаем подачу холодной воды (температура не более 25 оС) в кожух барабана и горячей воды (температура 84-98 оС) – в кожух массопровода и корыта. Потом открываем клапан питательный, расплав тнт из емкости начнет поступать в корыто барабана чешуирования к уровню 20 см. Закрываем клапан. При дальнейшей работе барабана чешуирования питательный клапан приоткрывается и затворяется автоматически. Температура чешуйки не превышает 50 оС, если происходит спекания 40 оС, тогда нужно снизить скорость оборотов барабану. Температура тротила в корыте на 5-6 оС высшая температуры плавления тротила.
На течку барабана одеваем бумажный мешок и зажимаем его пневмоцилиндрами так, чтобы при наполнении мешка он стоял на платформе весов. При заполнении мешка тротилом, перекрываем течку заслонкою, отъединяем мешок от течки и взвешиваем(вес мешка должна быть 30 кг). Мешок прибираем с весов и ставим на платформу. мешки на машину нагружаем с помощью ленточного транспортеру.
3.2.2 Производство ДПУ
Приготавление заливочной массы, для изготовления литых зарядов и детонаторов ДПУ-830 Тл, производится в смесителе для изготовления ши- мазированного расплава, который расположен в отделе заливки. Шимазированный расплав состоит из расплава тротила и его чешуйки.
Завязшая чешуйка тротила в смеситель осуществляется по течки через сито (диаметр сетки составляет 10 мм). Перед началом работы проверяют температуру воды в рубашке смесителя (tв=84-98 оС), потом затворяют промежуточный клапан на массопроводе подачи розплава в барабан чешуирования и открывают промежуточный клапан на массопроводе подачи расплава в смеситель. При достижении уровня расплава в смесителе приблизительно 1/3-1/2 высоты баку (проверяют через загрузочний люк смесителя с помощью деревянного весла), перекрывают промежуточный клапан на массопроводе, включают мешалку и прибавляют чешуйки тротила через течку в смеситель (загрузка чешуйки осуществляется небольшими порциями приблизительно по 30-35кг ). При беспрерывном обращении мешалки происходит смешивание массы до однородности. Время приготавления заливочной массы составляет 30-40 минут, а температура заливочной массы должна быть 81-85 оС (допускается снижать температуру заливочной массы с помощью добавки новой порции чешуйки). Готовность массы определяется визуально, люк смесителя закрывают крышкой с резиновой прокладкой, закрывают клапан вытяжной вентиляции, надел на ручку рычага клапана противовес (5кг).В предотвращении ожогов рук, работу вырабатывают в варежках. По сигналу подают в смеситель краткий воздух (начальное давление краткого воздуха 0,15-0,20 МПа , потом снижается и остается постоянным 0,03-0,08 МПа). Краткий воздух в смеситель подается с помощью вентиля, который расположен на воздухопроводе. Заливочная масса поступает в разливной клапан по массопроводу.
Первые расплавленные порции массы сливают в ведро, и отправляют на кристаллизацию. Потом наливается масса заливки в специальное ведро, для определения ее готовности (готовность определяется по диаметру растекаемости, у которого допустимый придел густоты составляет 34-38 сантиметров). Отбирать пробу непосредственно из смесителя не допускается.
При получении удовлетворительного результата проверки густоты массы, делается заливка детонаторов. Заливка выполняется в заливочный инструмент, который состоит из верхнего и нижнего фланцев. На нижний фланец устанавливается оболочка для детонатора, потом на штырь нижнего фланца надевается прессованная шашка из A-IX-I, потом надевается верхний фланец на оболочку. После установления заливочного инструмента, приоткрывается кран заливочного клапану и выполняется заливка в футляр через окна центрующей втулки. Наполнил футляр к уровню приблизительно 40-60мм от среза, клапан закрывается. Время выдержки 3-5мин., после производится доливка. Все это осуществляется вместе с воспитанием розплава в оболочках. Наполнения выполняется к нижнему торцу фланца. Время выдержки залитого детонатора составляет 10-15 мин. После чего выполняется разборка заливочного инструмента, его чистка и чистка детонаторов от остатков тротила.
Детонаторы после заливки идут на контроль качества. Контроль делается по весу, по внешнему виду, по прохождению калибра. После контроля вместе с крышкой детонаторы отправляют на маркировку. Маркировка наносится отдельно на бумажный вкладыш. Вкладыши крепится к детонатору с помощью надевания крышки на оболочку. Маркировка детонатора должна содержать: номер партии, год изготов- ления, заводской номер детонатора. Также должна быть маркировка на крышке детонатора при ее изготовлении, и должны содержать: марку детонатора "ДПУ-830 Тл", товарный знак или условное обозначение предприятия-изготовителя [5].
После маркировки детонаторы идут на укупорку. Упаковываются где- тонатори в гафрированные ящики (по 24 шт.). Вес каждого ящика с дето- наторами не более 25 кг. Детонаторы вкладываются в ящик вертикально или горизонтально, плотно рядами (стенки ящику и промежуток между рядами заполняют макулатурой). После вложения детонаторов в ящик, ложится бумажная прокладка, закрывается ящик с помощью металлических клапанов и липкой ленты (ширина ленты 60-100 мм). Перед заклеиванием ящика по городу стыка ящика вставляют собственное клеймо упаковщика. На боковой стороне ящика наклеивают ярлыки: с одной стороны - маркировка, со второго – знак опасности [7].
Готовую продукцию отвозят на состав с помощью автомашины или трактора с прицепом. Загрузка в транспорт осуществляется с помощью ленточного конвейера [3].