Использование полиалюминий хлорида для обработки фильтрата полигонов по средствам когуляционых и флокуляционных процесов
Нур Айни Заинол, Хамиди Абдул Азиз, Мохд Суффиан Юсуфф, Мухаммад Умар
Источник: http://www.isca.in/rjcs/Archives/vol1/I3/05.pdf
Аннотация
Фильтрат является сложным комплексом и загрязняет сточные воды, он получается в результате просачивания воды через тело полигона. Очистка полигонного фильтрата необходима, поскольку он может поставить под угрозу окружающую экосистему. Целью этого исследования являлось определение эффективности полиалюминий хлорида (PACL) в устранении химической потребности в кислороде (ХПК), аммиачного азота (NH3–N) и цветности фильтрата с двух различных полигонов в Малайзии. Оптимальная дозировка в удалении этих параметров была определена и она оказалась ниже для полигона Kulim (KLS), в сравнении с полигоном Ampang Jajar (AJLS). При оптимальной дозе PACL в качестве коагулянта, степень уменьшения ХПК для KLS была выше, чем полученное значение для AJLS. Удаление цветности для обоих объектов были практически одинаковы. Устранение NH3–N был весьма умеренным для обеих свалок, однако у KLS более высокие темпы устанения этого составляющего.
Ключевые слова: Фильтрат, полигон, коагуляция и флокуляция, полиалюминий хлорид.
Вступление
Захоронение, как утилизация, на полигонах является одним из самых популярных методов для твердых бытовых отходов (ТБО), из-за его относительной простоты с точки зрения процедур удаления, низкой стоимости и ландшафтно-восстановительного влияния на выработки от минеральной добычи. Однако, есть серьезные опасения, связанные с этим методом утилизации, которое гинерирует высокоопасное загрязнение сточных вод, так называемый фильтрат. Фильтрат образуется при выщелачивании дождевой водой или воды неизбежно присутствующей в структуре отходов из тела полигона. Фильтрат может содержать большое количество органических веществ (биоразлагаемые и не поддающихся биохимическому разложению), аммиачного азота, взвешенных веществ (SS), неорганических солей и значительной концентрации тяжелых металлов. Таким образом, слив полигонного фильтрата без надлежащей очистки может оказывать вредное воздействие на поверхностные и подземные воды, поскольку он может просочиться через почвы и грунты.
Химический состав полигонного фильтрата зависит от нескольких факторов, включая состав отходов, гидрогеологического участка, конкретных климатических условий, прохождение влаги через полигон, возраст свалки, а также проектирования и эксплуатации полигона. В общем, молодой фильтрат имеет тенденцию быть кислотным, из-за присутствия жирных кислот. С другой стороны, стабильный или старый фильтрат преимущественно состоит из высокомолекулярных органических соединений, таких как гуминовые и фульвокислоты и относительно низкой химической потребности в кислороде (ХПК) в диапазоне 500–5000 промилле. Таким образом, биологические процессы значительно интенсивнее для молодого фильтрата, но менее интенсивны для старого ( стабильного) фильтрата.
Коагуляция-флоккуляция является относительно простой и часто применяемой техникой для воды и очистки сточных вод. Эта техника может быть с успехом использована для очистки старого фильтрата полигонов. Механизм очистки этого процесса состоит в основном из нейтрализации заряда отрицательно заряженных коллоидов по отношению к катионным продуктам гидролиза с последующим получением примесей в виде аморфного осадка гидроксида в процессе флокуляции.
Коагулянтом называют вещество или химическое соединение, которое добавляют в воду, чтобы начать (завершить) процесс коагуляции-флокуляции. Для исследования процесса коагуляции-флокуляции в качестве обработки фильтрата полигонов были проведены на несколько эксперементов. Сульфат алюминия (квасцы), хлорид железа и сульфат железа часто используются в качестве коагулянтов. Тем не менее, в последние годы большое внимание было уделено гидролизу солей металлов коагулянтов, а именно полиалюминий хлориду (PACL), из-за его более высокой эффективности в качестве коагулянта и относительно низкой стоимости по сравнению с обычными коагулянтами. Кроме того, PACI имеет хорошую структуру и высокую плотность заряда, что приводит к снижению требований дозировки и, следовательно, меньшему образованию осадка. Применение PACL в качестве коагулянта для удаления цветности, ХПК и аммиака из воды и сточных вод была рассмотрена в течении нескольких исследований, и был получен вывод, что PACL способен устранять цветность, уменьшать ХПК и содержание аммиака. Тем не менее, использование PACL качестве коагулянта по-прежнему редкость в очистке фильтрата.
Данное исследование сфокусировано на двух различных типах фильтрата, полученных на полигоне Kulim (KLS) и полигоне Ampang Jajar (AJLS). KLS находится в Kулим, штат Кедах, Малайзия. Это открытое для захоронения место, полигон начал использоваться в 1996 году, и был передан в для санитарной мусорной свалки в 2006 году. AJLS находится в Себеранг Пераи, штат Пенанг, Малайзия. Это место находится в ведении меджлиса Пербандаран Себеранг Пераи (MPSP) и полигон не работает уже более 10 лет.
Целью данного исследования было изучение эффективности коагуляции-флокуляции для удаления ХПК, NH3–N и цветности от KLS и AJLS фильтрата с использованием PACI. Таким образом, результаты были бы полезны в установлении качества очистки образца от заданных параметров в свалочном фильтрате.
Материалы и методы
Стоки: образцы фильтрата отбирали из KLS и AJLS в период с июня по декабрь 2010 года. Образцы были собраны в пластиковые контейнеры по 25 л, транспортированы в лабораторию и хранились при 4 °С. Образцы фильтрата доставали из холодильника и оставляли при комнатной температуре в сосуде в течении приблизительно 2 часов до проведения исследования. Затем образцы тщательно перемешивали до повторной взвеси оседлых твердых частиц, потом проводились разнообразные исследования. Образцы были охарактеризованы с точки зрения рН, NH3–N, ХПК, мутности и цветности. Таблица 1 и 2 показывают общие характеристики образцов, определенных в соответствии со стандартными методами для исследования воды и сточных вод.
Процесс очистки: гидролизованный раствор PACL с формулой Al(OH)xCly (где х находится в диапазоне 1,35–1,65, а у = 3 — х) и рН 2,3–2,9 (за счет присутствии соляной кислоты), поставляется Hasrat Bestari Sdn Bhd, штат Пенанг, Малайзия. 18%–ный раствор PACI был использован в качестве исходного раствора на протяжении эксперимента. Эксперименты проводились в обычной испытательной аппаратуре (VELP–Scientifica, Модель: J LT6, Италия), состоящий из шести лопастных роторов (2,5 см на 7,5 см), оснащенный 6 стаканами по 1 л каждый. Время и скорость для быстрого и медленного перемешивания были установлены с помощью автоматического контроллера. Для каждого эксперимента стакан использовался для тестирования, он был заполнен 500 мл образца. Перед быстрым перемешиванием, различные дозы PACL добавляли в каждую емкость, вместе с тем регулировали рН с использованием серной кислоты и гидроксида натрия. Для этого исследования, рабочие параметры были приняты: для быстрого перемешивания — скорость 80 оборотов в минуту, для медленного перемешивание — скорость 30 оборотов в минуту, быстрое перемешивание в течении 2–х мин, медленное перемешивание — 30 мин, а также время установления равновесия 30 мин.
Анализы: После выполнения тестов в емкостях, надосадочные образцы были изъяты для анализаиз стакана, с помощью пластикового шприца с точки, расположенной примерно на 2 см ниже уровня жидкости. Значение рН измеряли рН–метром (CyberScan 20), а мутность была измерена с помощью 2100N HACH лабораторного турбидиметра. Остаточное ХПК определяли с помощью закрытого рефлюкса и колориметрического метода (5220D). NH3–N определяли с использованием метода Nesslerization (4500 — NH3). ХПК был определен с использованием колориметрического метода (5220–D). Измерения цветности определяли как истинный цвет, образец фильтруют с помощью GC–50 фильтровальной бумаги (Advantec Toyo Kaisha, Япония) при 0,45 мкм размером пор, анализ проводится используя DR2800 HACH спектрофотометр при длине волны 455 нм. Метод № 2120C дает результат цветности в платиново-кобальтовой (PtCo) единице цветности, представляемой как 1 мг платины/л в виде хлороплатината иона. Эффект фильтрации по удалению цветности был корректирован с помощью контрольного образца. Эффективность удаления параметров было получено по следующей формуле.
извлечение (%) = [(Ci — Cf)/Ci]·100
где Ci и Cf начальные и конечные концентрации образца фильтрата в мг/л, соответственно.
Результаты и обсуждение
Дозировка коагулянта играет важную роль в удалении целевых загрязняющих веществ в исследований коагуляции-флокуляции. Оптимальная дозировка коагулянта определяется как значение, выше которого нет значительного увеличения эффективности удаления с последующим добавлением коагулянта.
Дозы коагулянта PACL для обоих фильтратов взяты в диапазоне от 0 мг/л до 9000 мг/л при различных приращениях. Влияние различных доз PACI на AJLS фильтрат показана на рис. 1, а рис. 2 показано влияние различных доз PACL на KLS фильтрат. Удаление ХПК увеличился изначально, но тенденция к снижению наблюдалась при дозировке PACL 2700 мг/л с последующим увеличением когда дозировка была (рис. 1) увеличена до 3600 мг/л. Однако, помимо этой дозировки, последовательное увеличение удаления ХПК наблюдалось и достигла максимума в дозировке PACL 7200 мг/л (рис. 1). Интересно, что картина очистки NH3–N была похожа на удаление ХПК первоначально, однако, для дозировки вне 3600 мг/л, шаблон удаления варьируется в широких пределах и достигает максимума при концентрации 5400 мг/л PACL, наблюдается последующие уменьшение при дальнейшим увеличением дозировки PACL (рис. 1). Как показано на рис. 1, удаление цветности было более последовательным с увеличением дозировки PACL и достигает максимума, когда содержание PACL увеличивается до 8100 мг/л.
Согласно рис. 2, для KLS фильтрата, тенденция удаление ХПК была иного рода, чем из AJLS. Плавное снижение ХПК наблюдалось с увеличением PACL-дозировки, и достигает максимума при 4500 мг/л, с последующим последовательным снижением при увеличении дозы PACL (рис. 2). Опять же, NH3–N показал своеобразную тенденцию очистки не соответствующую растущим дозах PACL, как показано на рис. 2. Хотя удаление цветности осталась практически одинакова для PACL дозах 900 и 1800 мг/л, было установлено, значительное уменьшение, если доза PACL была увеличена до 2700 мг/л. Тем не менее, он оставался почти на линейных дозах, превышающих 2700 мг/л (рис. 2).
На основании приведенных выше результатов, оптимальные дозировки PACI для AJLS и KLS были выбраны в 7200 мг/л и 4500 мг/л, соответственно. В нейтральном рН, эти оптимальные дозировки давали ХПК абсорбции от 50% до 67% для AJLS и KLS, соответственно. Хорошо известно, что ХПК-интенсивность зависит от гуминовых веществ в фильтрате. Таким образом, с проведением гидролиза коагулянта, таких как PACI, гуминовые вещества были успешно удалены из фильтрата. Настоящие результаты согласуются с описанными в других источниках. Разница в скорости удаления может быть связана с возрастом полигонного фильтрата. Следует отметить, что KLS в настоящее время действует и образует сильно загрязненный фильтрат в сравнении с AJLS, который был закрыт более чем 10 лет назад, следовательно, обрзуется старый, стабилизированный фильтрат с относительно высоким процентом стойких соединений, которые более трудно удалить.
Удаление цветности при оптимальных дозах было в среднем одинаково для обоих типов фильтрата с использованием оптимальной дозировки PACL, и колебалась в пределах 70–73% (рис. 1 и 2). Однако удаление содержания NH3–N была ниже на 26% и 45% для AJLS и KLS, соответственно. Это согласуется с предыдущими выводами в которых авторы используеют PACL в качестве коагулянта для обработки полу-аэробного свалочного фильтрата. В целом, удаление цветности был выше, чем ХПК и NH3–N для обоих полигонов, независимо от дозировки PACL (рис. 1, 2).
В общем, можно заметить, что очистка не увеличивается с повышением дозировки коагулянта до достижения оптимального значения. Это может быть связано с тем, что чрезмерное количество коагулянта, является причиной дестабилизации коллоидов и повторного диспергирования коллоидных частиц. Таким образом, процесс должен быть оптимизирован для снижения обеих операционных расходов и повышения эффективности удаления. Использование местных природных полимеров PACL, в качестве коагулянта, также может рассматриваться для дальнейшего снижения дозировки коагулянта, как сообщали в ранних работах.
Вывод
Итак, различные оптимальные дозы были получены для PACI в обоих полигонах. Оптимальная доза для PACI на KLS была ниже, чем AJLS, указанны низкие требования к коагулянту и, возможно, меньше осадкообразование. Можно сделать вывод, что обработка свалочного фильтрата от KLS и AJLS с помощью процесса коагуляции-флокуляции в присутствии PACI качестве коагулянта был эффективен в удалении цветности и ХПК, но не так действенен в случае удаления NH3–N. Таким образом, PACL может быть использован эффективно в качестве стадии предварительной обработки перед дальнейшей биологической очисткой.
Благодарность
Авторы хотели бы выразить признательность Universiti Sain Малайзии (USM), которые обеспечили получение гранта для проведения этого исследования. Авторы также хотели бы выразить признательность сотрудничеству в ходе этого исследования со стороны меджлиса Пербандаран Себеранг Пераи, Мажлиса Пербандаран Kулим и подрядчиком Idaman Bersih Sdn. Bhd. Penang.
Таблица1 — Общая характеристика фильтрата из Kulim полигона (KLS)
| Параметр | Единица измерения | Диапазон |
| pH | 7.85–8.28 | |
| NH3–N | (мг/л) | 600–720 |
| ХПК | (мг/л) | 110–300 |
| Мутность | (NTU) | 11.65–24.9 |
| Цветность(PtCo) | (мг/л) | 279–494 |
Таблица 2 — Общая характеристика фильтрата от Ampang Jajar полигона (AJLS)
| Параметр | Единица измерения | Диапазон |
| pH | (мг/л) | 7.13–8.25 |
| NH3–N | (мг/л) | 258–570 |
| ХПК | (мг/л) | 117–260 |
| Мутность | (NTU) | 15–20.3 |
| Цветность (PtCo) | (мг/л) | 134–287 |
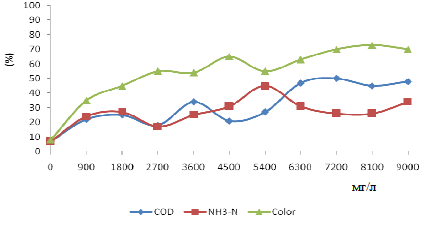
Рисунок 1 — Влияние в качестве коагулянта дозировки по удалению ХПК(COD), NH3–N и цветности (color) для AJLS фильтрата
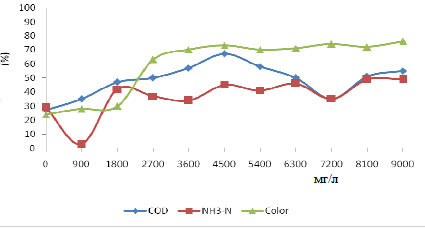
Рисунок 2 — Влияние в качестве коагулянта дозировки по удалению ХПК(COD), NH3–N и цветности (color) для KLS фильтрата
Список литературы
Bashir M.J.K., Aziz H.A., Yusoff M.S. and Adlan M.N., Application of response surface methodology (RSM) for optimization of ammoniacal nitrogen removal from semi– aerobic landfill leachate using ion exchange resin, Desalination, 254, 154–161 (2010)
Umar M., Aziz H.A. and Yusoff M.S., Trends in the use of Fenton, electro–Fenton and photo–Fenton for the treatment of landfill leachate, Waste Manage, 30, 2113–2121 (2010)
Umar M., Aziz H.A. and Yusoff M.S., Variability of parameters involved in leachate pollution index and determination of LPI from four landfills in Malaysia, Int. J. Chem. Eng., Article ID: 747953 (2010)
Aziz H.A., Daud Z., Adlan M.N. and Hung,Y.T., The use of polyaluminum chloride for removing colour, COD and ammonia from semi–aerobic leachate, IntJ.Environ.Eng., 1, 20–35 (2009)
Renou S., Givaudan J.G., Paulain S., Dirassouyan F. and Moulin P., Landfill leachate treatment: review and opportunity, J.Hazard. Mater., 150, 468–493 (2008)
Bashir M.J.K., Isa M.H., Kutty S.R.M. Awang Z.B., Aziz H.A., Mohajeri S. and Farooqi I.H., Landfill leachate treatment by electrochemical oxidation, Waste Manage., 29, 2534–2541 (2009)
Aziz H.A., Yusoff M.S., Adlan M.N., Adnan N.H. and Alias S., Physico–chemical removal of iron from semi–aerobic landfill leachate by limestone filter, Waste Manage, 24, 353–358 (2004)
Ghafari S., Aziz H.A., and Bashir M.J.K., The use of poly– aluminum chloride and alum for the treatment of partially stabilized leachate: a comparative study, Desalination, 257, 110–116 (2010)
Aziz H.A., Alias S., Adlan M.N. Asaari F.A.H. and Zahari M.S., Colour removal from landfill leachate by coagulation and flocculation processes, Bioresour. Technol., 98, 218–220 (2007)
Kulikowska D. and Klimiuk E., The effect of landfill age on municipal leachate composition, Bioresour. Technol., 99, 5981–5985 (2008)
Amokrane A., Comel A. and Verson, J., Landfill leachate pretreatment by coagulation–flocculation, Water Res., 31, 2775–2782 (1997)
Duan J.M. and Gregory J., Coagulation by hydrolyzing metal salts, Adv. Colloid Interface Sci., 100–102, 475–502 (2003)
Davis M.L. and Cornwell D.A., Introduction to Environmental Engineering, Fourth ed. Mc–Graw Hill, New York, (2008)14. Tatsi A.A., Zouboulis A.I., Matis K.A. and Samaras P., Coagulation–flocculation pretreatment of sanitary landfill leachates, Chemosphere, 53, 737–744 (2003)
Hu C., Liu H. and Qu J., Preparation and characterization of polyaluminum chloride containing high content of Al13 and active chlorine, Colloids and Surf. A: Physicochem. Eng. Asp. 260, 109–117 (2005).
McCurdy K., Carlson K. and Gregory D., Flocs morphology and cyclic shearing recovery: comparison of alum and polyaluminum chloride coagulants, Water Res., 38, 486–494 (2004)
Wang Y., Gao B.Y., Xu X.M., Xu W.Y. and Xu G., Characterization of floc size, strength and structure in various aluminum coagulants treatment, J. Colloid Interf. Sci., 332, 354–359 (2009)
Gao B., Hahn H.H. and Hoffmann E., Evaluation of aluminium –silicate polymer composite as a coagulant in water treatment, Water Res., 36, 3573–3581 (2002)
Tapas N., Vyras R.D., Shastry S. and Kaul S.N., Optimization of coagulants for pre–treatment of printing ink wastewater, Environ. Eng. Sci,. 19, 1–7 (2002)
Wang D., Sun W., Xu Y., Tang H. and John G., Speciation stability of inorganic polymer flocculant–PACI, Colloid Surf. Physicochem. Eng. Asp., 243, 1–10 (2004)
APHA, Standard Methods for the Examination of Water and Wastewater, Twenty first ed., American Public Health Association, Washington DC (2005)
Aguilar M.I., Saez J., Llorens M., Soler A., Ortuno J.F., Meseguer V. and Fuentes A., Improvement of coagulation– flocculation process using anionic polyacrylamide as coagulant aid, Chemosphere, 58, 47–56 (2005)
Ghafari S., Aziz H.A. and Zinatizadeh A.A., Application of response surface methodology (RSM) to optimize coagulation–flocculation treatment of leachate using poly–aluminum chloride (PAC) and alum, Hazard. Mater., 163, 650–656 (2009)
Aziz H.A., Adlan M.N., Mohamed A.M.D., Raghavan S., Koflly M., Isa M. and Abdullah M.H., Study on the anionic natural coagulant aid for heavy metals and turbidity removal in water at pH 7.5 and alum concentration 25 mg/L–laboratory scale, Ind. J. Eng. Mater. Sci., 7, 195–199 (2000)
Al–Hamadani Y.A.J., Yusoff M.S., Umar M., Bashir M.J.K. and Adlan M.N., Application of psyllium husk as coagulant and coagulant aid in semi–aerobic landfill leachate treatment, J. Hazard. Mater., doi:10.1016/j.jhazmat.2011.03.087 (2011).