Реферат за темою випускної роботи
Зміст
- Введення
- 1. Актуальність теми
- 2. Мета магістерської дисертації і завдання досліджень
- 3. Об'єкт і методи дослідження
- Висновок
- Перелік посилань
Введення
Біопаливо – паливо з рослинної або тваринної сировини, з продуктів життєдіяльності організмів або органічних промислових відходів. Різниться рідке біопаливо (для двигунів внутрішнього згоряння, наприклад, етанол, метанол, біодизель), тверде біопаливо (дрова, брикети, паливні гранули, тріска, солома, лузга) і газоподібне (синтез–газ, біогаз, водень). 54–60% біопалива складають його традиційні форми: дрова, рослинні залишки і сушений гній для опалення будинків і приготування їжі. Їх використовують 38% населення Землі [2].
Розширенню використання біопалива сприяють обов'язкові норми, що вимагають мати певний відсоток біопалива в енергоспоживанні. Життя людей неможливе без вживання палив. Розрізняють дві групи палив:
- палива, що видобуваються з земних надр (копалини палива);
- палива, одержувані з наземного сировини (їх прийнято називати біопаливо).
Основна відмінність між даними групами палив полягає в тому, що спалювання викопних палив призводить до збільшення вмісту вуглекислого (т. зв. Парникового) газу в атмосфері Землі (вуглецю в Землі стає менше, а в атмосфері – більше); спалювання ж палив другої групи не збільшує вмісту вуглекислого газу в атмосфері (наприклад, при спалюванні деревини в атмосферу вводиться рівно вуглекислого газу, скільки було вилучено з атмосфери в процесі росту деревини за рахунок фотосинтезу) [1].
Очевидно, що найперспективнішим видом сировини для виробництва біопалива є водорості. Водорості є найшвидше рослинами на землі (маса за добу подвоюється), для їх росту потрібно легкодоступний сировину: сонячне світло, вода і діоксид вуглецю.
Мікроводорості можуть вирощуватися як в прісній воді, так і в солоній. Також для виробництва мікроводоростей не потрібно використання шкідливих пестицидів і гербіцидів. Одне з основних переваг мікроводоростей полягає в тому, що вони ефективно перетворюють енергію сонячного світла в біомасу
Приставка біо
у назві говорить, що в процесі отримання біопалива ми використовували вуглекислий газ. Потрібно звернути увагу, що біопаливо — це CO2–нейтральне паливо: при спалюванні біопалива утворюється вуглекислий газ, але і при його отриманні стільки ж вуглекислого газу знову перетвориться в біомасу.
За останні 20 років викиди вуглекислого газу в атмосферу збільшилися в півтора рази, і концентрація газу в атмосфері з кожним роком підвищується. Можна припустити, що наявний на Землі фотосинтезуючих потенціал вже не справляється з тими викидами вуглекислого газу, які людство виробляє. Вуглекислий газ, вода і енергія сонячного світла в процесі фотосинтезу перетворюються в енергію зв'язків хімічних сполук органічної речовини і кисень.
Процес фотосинтезу — це реакція, яка обумовлює круговорот вуглецю і кисню в природі. За оцінками фахівців, до 80% всього кисню на нашій планеті виробляє в морях і океанах фітопланктон, тобто водорості і ціанобактерії, а що залишилися 20% – наземні рослини. Сьогодні в науковому співтоваристві є великий інтерес до мікроводоростей як засобу захоплення вуглекислого газу і поновлюваному джерелу біопалива.
Сама распространенная — це мікроводорость Chlorella vulgaris.
Chlorella vulgaris – одноклітинна водорість, що мешкає в прісних і солоних водоймах, на вологому грунті, Скаллі. Клітини мають вигляд зелених кульок діаметром до 15 мкм. Джгутиків, вічок і скорочувальних вакуолей не має. У клітинах є чашоподібний хроматофор з піреноїдом або без нього і дрібне ядро. Статевий процес для цієї водорості не відомий. Безстатеве розмноження відбувається шляхом мітотичного поділу вмісту материнської клітини двічі або тричі.
В результаті поділу формується чотири або вісім дочірніх клітин. Після розриву материнської оболонки клітини виходять назовні, збільшуються в розмірах і діляться знову.
Хлорела цікава тим, що її клітини містять велику кількість поживних речовин – 50 повноцінних білків, жирні олії, вуглеводи, вітаміни В, С і К і навіть антибіотики. Вона розмножується так інтенсивно, що за добу відбувається тисячократно збільшення числа її клітин. Хлорела стала першою водорістю, яку людина стала вирощувати в культурі. Вона використовувалася в якості експериментального об'єкта для вивчення деяких етапів фотосинтезу.
1. Актуальність теми
Одна з актуальних проблем сучасності є пошук альтернативних видів джерел енергії. Одним з них є рідке паливо, серед них можна виділити різні види біопалива, в тому числі найбільш актуальним є біопаливо одержуване з мікроводоростей. Позитивним моментом є, то що мікроводорость можна інтенсивно вирощувати у великому обсязі, при чому технологія цього процесу досить проста [3].
2. Мета магістерської дисертації і завдання досліджень
Метою даної роботи є: вивчення процесу генезису мікроводоростей з визначенням його якісних показників на експериментальній установці.
Завдання:
- Визначення показників якості зростання мікроводоростей різними інструментальними методами.
- Порівняння і вибір кращого інструментального методу.
3. Об'єкт і методи дослідження
Як об'єкт дослідження застосовувалася культуральне середовище мікроводоростей на різних стадіях. Головною відмінністю суспензії було інтенсивність її забарвлення, і тому на першому етапі необхідно визначити реальне число клітин в одиниці об'єму (млн/мл).
Оцінка продуктивності мікроводорості здійснюється за стандартною методикою в якості, якої застосовується традиційна для світлової мікроскопії методика підрахунку клітин культури за допомогою рахункових камер (Горяєва, Тома – Цейса) [5].
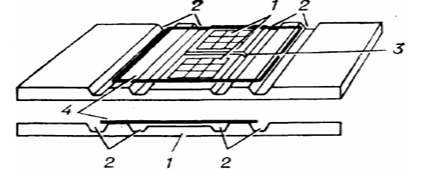
Рисунок 1 — Пристрій двухсеточной камери Горяєва
1 – пластинки з вигравіруваними сітками; 2 – поздовжні жолобки; середня частина платівки нижче бічних на 0,1 мм (глибина камери) і розділена поперечним желобком (3); 4 – покривне скло.
Після ретельного перемішування досліджуваної рідини беруть її зразок і наносять на сітку лічильної камери, накривають покривним склом розміром 18 х 18 мм завтовшки 0,25–0,35 мм і притирають покривне скло до бічних пластинках камери до освіти кілець Ньютона. Притирають покривне скло для того, щоб висота шару досліджуваної рідини в камері була 0,1 мм.
Після заповнення камери досліджуваним зразком, її поміщають на столик мікроскопа і знаходять в його поле зору сітку. Підраховують все клітини мікроорганізмів, що знаходяться всередині великого квадрата, а також на прикордонних лініях, якщо клітини здебільшого знаходяться в даному квадраті. Якщо клітини перетинаються прикордонної лінією навпіл, то клітини вважають тільки на двох суміжних сторонах квадратом. У кожному препараті підраховують клітини в п'яти великих квадратах, наприклад, по кутах і в центрі сітки.
Біореактор
Отримання біопалива з ліпідів містяться в мікроводоростей, є високоефективної біотехнологією і має значний потенціал.
Біореактор – апарат, в якому здійснюється ріст і розвиток генезису, а також перемішування культурального середовища в процесі мікробіологічного синтезу.
Біореактор хлорели на вході з ємністю готової суспензії забезпечує виконання оптимальної технології вирощування мікроводоростей з отриманням якісного цільового продукту.
Установка має в своєму складі блок визначень кількісних показників з використанням приладів визначення інтенсивності кольору культурного середовища (суспензії хлорели).
Висока продуктивність мікроводоростей залежить від наступних умов культивування: світловий режим, склад живильного середовища, концентрація CO2, конструкції фотобіореактори. Оптимальне поєднання все цих параметрів дозволить отримати максимальний вихід біомаси. CO2 – основне джерело харчування.
Значення необхідної концентрації вуглекислого газу в газоповітряної суміші залежить від використовуваного штаму, конструкції фотобіореактор і режиму культивування. Вуглекислий газ вводиться в фотобіореактори з повітрям або в чистому вигляді з балонів.
Концентрація вуглекислого газу залежить від щільності клітин мікроводоростей в суспензії. Так, при щільності клітин хлорели 100–150 млн / мл вуглекислотне насичення фотосинтезу відбувається при концентрації CO2 в газовій суміші 0,2%, а при 4–5 млрд. – 4,5–5,5%.
Найбільш впливає на зростання мікроводоростей фактор – освітленість. Відомо, що нестача або надлишок освітленості уповільнює процес фотосинтезу, що негативно позначається на прирості біомаси.
Одним з найбільш перспективних напрямків є використання закритих фотобіореактори з використанням штучного світла для освітлення біомаси в темний час доби.
В даний час в якості штучних джерел світла застосовуються люмінесцентні, натрієві, світлодіодні (фіто або біколор), галогенові лампи, а також лампи розжарювання [4].

Рисунок 2 — Культивування мікроводоростей
(анімація: 5 кадрів, 5 циклів повторення, 326 кілобайт)
Фотографічний метод
Значною перевагою фотографічного методу є його документальність, так як фотографічна пластинка зі спектром може бути збережена. Крім того, метод відрізняється високою абсолютною чутливістю і достатньою при визначенні низьких концентрацій відтворюваністю [4].
Фотографічний метод – метод вивчення різних явищ, що відбуваються в природі, що полягає в фіксації явища на фотографії або серії фотографій, які в подальшому піддаються аналізу з боку фахівців. Проведемо імітацію процесу генезису, щоб визначити залежність барвника, як кількість барвника впливає на інтенсивність і колірну інтенсивність досліджуваної суспензії. В одну наливаємо 1 мл і отримуємо 20 млн клітин; в другу 3мл – 60 млн клітин, в третю 5мл – 100 млн клітин. Далі будемо працювати з графічним редактором. Потрібно залити фото з пробірками, навести на центр фото і отримаємо результат значення трьох складових кольору R (червоний), G (зелений), B (синій). Використовується значення G для побудови графіків.

Рисунок 3 — Пробірки з різною кількістю барвника
Фотоколориметричний метод
Фотоколориметричний метод заснований на визначенні змісту речовин в розчинах по поглинанню немонохроматичного випромінювання світла у видимій області спектра. Цим методом можна за інтенсивністю забарвлення розчину встановити концентрацію визначається речовини в розчині [4].
Для цього нам знадобиться: три пробірки з речовиною, датчик кольору TCS230, Arduino UNO, програмне забезпечення для Arduino UNO.
З'єднаємо схему, зверху на датчик потрібно по черзі піднести, кожну з пробірок, на екрані в програмі Arduino, ми побачимо значення RGB. Далі потрібно побудувати графік і зробити висновок.
Датчик TCS230, розташований в центрі плати, складається з фотодіодів чотирьох типів: 16 фотодіодів з червоним фільтром, 16 фотодіодів з зеленим фільтром, 16 фотодіодів з синім фільтром і 16 фотодіодів без світлофільтра. До датчику підносять зразок одного з трьох кольорів – червоного, зеленого або синього. Зразок висвітлюється світлодіодами на платі навколо датчика. Датчик має перетворювач струму в частоту, він перетворює свідчення фотодіодів в квадратну хвилю з частотою, пропорційною інтенсивності світла обраного кольору. Ця частота потім зчитується Arduino.

Рисунок 4 — Робочий варіант схеми люксметра
G1 – Фотографічний метод, G2 – Фотоколориметричний метод.
Таблиця 1 — Дані для фотографічного і фотоколориметричного методу.
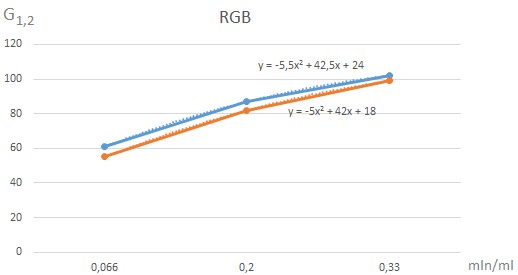
Рисунок 5 — Графіки залежності G1, G2 від кількості барвника
Заключение
Таким чином, біодизель — паливо на основі жирів тваринного, рослинного і мікробного походження, а також продуктів їх етерифікації.
Для отримання біодизельного палива використовуються рослинні або тваринні жири. Сировиною можуть бути рапсове, соєве, пальмове, кокосове масло, або будь–якого іншого, а також відходи харчової промисловості. Розробляються технології виробництва біодизеля з водоростей.
Вибір підходящої середовища є важливою умовою для успішного культивування мікроводоростей. Тому перед початком виділення найпильнішу увагу слід приділити вибору середовища для культивування.
Визначення інтенсивності колірної компоненти (G1, G2), різними методами, показав, що характер залежності мають подібний характер.
Для фотографічного і колориметрического методу, важливим завданням даного дослідження є визначення кількості мікроводорості для отримання біопалива.
Перелік посилань
- Основные тенденции развития рынка биотоплива в мире и России за период 2000–2012 годов. [Электронный ресурс]. URL: http://portal-energo.ru/files/...
- Биодизельное топливо. Производство биодизеля. [Электронный ресурс]. URL: http://amastercar.ru/articles/...
- Кулманаков, С. С. Перспективные смесевые кислородсодержащие топлива / С. С. Кулманаков, Д. Д. Матиевский, А. И. Балашев, С. В. Лебедевас // Ползуновский Вестник. – 2009 г. – №1–2. – С. 17–21.
- Попова, И. Ю. Методы биотоплива / И. Ю. Попова // Сверхкритические Флюиды: Теория и Практика. – 2007 г. Т. 2. – № 4. – C. 85–95.
- Иманкулов, Н. Н. Фотокалориметрический метод / Н. Н. Иманкулов, О. С. Балабеков // Материалы научно–практической конференции Нефтехимия и нефтепереработка. Уфа, 2008 г.
- Виноградова, А. В., Биотехнология топлива: учеб. пособие / А. В. Виноградова, Г. А. Козлова, Л. В. Аникина. – Пермь: Изд–во Перм. гос. техн. ун–та, 2008. – 212 с.
- Особенности производства биодизеля. [Эдектронный ресурс]. – Режим доступа: http://www.cleandex.ru/articles/...
