Реферат за темою випускної роботи
Зміст
ВВЕДЕННЯ
Водне господарство є складовою частиною економіки. Головне його завдання-забезпечити споживачів водою в необхідній кількості і необхідної якості. В умовах маловодного клімату Донецького степу стратегічно важливе значення має водопостачання населення і підприємств. Основою водного господарства є ресурси поверхневих і підземних вод. Їх раціональне використання і охорона від забруднення і виснаження регулюється законодавством і обумовлює управління водними ресурсами як єдиним механізмом. Особливе значення має проблема раціонального використання та охорони водних ресурсів в умовах маловодного регіону Донецької Народної Республіки. Всі води (водні об'єкти) на території ДНР є надбанням народу і можуть передаватися тільки в користування. Водойми мають велике значення не тільки для життєзабезпечення населення, промисловості, сільського господарства, а й для відпочинку, туризму, спорту. В умовах антропогенних навантажень на природне середовище існує необхідність розробки та дотримання правил користування водними ресурсами, раціонального їх використання та екологічно спрямованого захисту. Предметом даної роботи є поверхневі води м. Донецька. Метою роботи є: дослідити стан і проблеми поверхневих вод, розглянути перспективи вирішення даних проблем. Завдання роботи: - про характеризувати особливості водних ресурсів регіону; - вивчити використання водних ресурсів в м. Донецьку; - вивчити проблему забруднення води; - розглянути основні напрямки щодо поліпшення стану водних ресурсів. Для написання роботи використовувалися такі методи: літературний; картографічний; статистичний; порівняльний; програмно-цільовий. У даній роботі використовувалися численні джерела: підручники та навчальні посібники; статистичні матеріали; книги-довідники; буклети; Інтернет - сайти.
1. Стан і раціональне використання водних ресурсів на території м. Донецька
Всі водні об'єкти м. Донецька та тимчасово приєднаних територій є об'єктами загальнодержавного значення. Територією міста Донецька та тимчасово приєднаними територіями проходить вододіл басейну Дніпра та басейну річок приазов'я. З 120 водних об'єктів міста та тимчасово приєднаних територій слід виділити 8 водосховищ та 112 ставків. Загальна площа водойм становить 864,7 га, обсяг водних ресурсів - 28,1 млн. куб. м. Кальміус-основна річка, яка протікає через центр міста по п'яти районах: Київському, Ворошиловському, Калінінському, Ленінському і Будьонівському. Її притоками в межах міської межі є балки широка, Богодухова, дурна, Гнатіївська, балки без назви. На річці Кальміус в межах Київського і Ворошиловського районів розташовується два водосховища – Кальміуське і Нижньо-Кальміуське. У межах Моспіно в Пролетарському районі протікає р. Грузька-ліва притока р. Кальміус. Північно-західна частина міста розсічена балками і річками осикова і Лозова (басейн р.Вовча). Водні ресурси річок і балок м. Донецька представлені: природним, незареєстрованим поверхневим стоком, що формується за рахунок атмосферних опадів і дренування підземних вод; стічними і шахтними водами; зарегульованим стоком-ставками і водосховищами. Основними споживачами водних ресурсів є шахти і підприємства М. Донецька. На державному обліку в м. Донецьку в поточному році зареєстровано 104 спеціальних водокористувача. У 2019 році загальний обсяг скинутих у поверхневі водні об'єкти стічних вод склав 103,5 млн.куб. м, з них недостатньо очищених – 41,1 млн. куб. м або 40% валового скидання. Через високу антропогенного і техногенного навантаження протягом тривалого часу багато водні об'єкти міста гранично обміліли, мають значний рівень бактеріального і хімічного забруднення. Контроль якості води в них показує, що при різних фазах гідрологічного режиму концентрації забруднюючих речовин практично не змінюються, що говорить про втрату самоочищаючої здатності водних об'єктів. Основними суб'єктами скидання недостатньо очищених стічних вод у водні об'єкти на території м. Донецька є діючі підприємства вугільної промисловості: ДП " Донецька вугільна енергетична компанія "(шахта ім. Челюскінців, шахта ім. Скочинського-працюють на видобуток вугілля, шахта 17-17 біс, шахта Абакумова, шахта Лідіївка – працюють у режимі водовідливу) та ДП " Шахта ім. Засядько", а також РП "Донбасвуглереструктуризація" , в яку входить в тому числі і " Донецька дирекція з виконання проектів ліквідації та підготовки шахт до ліквідації» (шахта ім. М. Горького, шахта № 9 Капітальна, шахта Заперевальна № 2). Результати дослідження якості води, виконані суб'єктами екологічного моніторингу, вказують на відхилення показників якості води від прийнятих санітарних нормативів охорони поверхневих вод від забруднення по сульфатам, зваженим речовинам, солевмісту і нафтопродуктам. У літній період спостерігається перевищення діючих норм по біохімічному споживанню кисню і збагачення вод мінеральними формами азоту, що вказує на підвищений вміст легкоокісляемих органічних речовин у воді поверхневих водойм і значну частку скидів шахтних вод. Якість скидаються шахтних вод оцінюється згідно з нормативами складу і властивостей води, передбаченим санітарними правилами і нормами охорони поверхневих вод від забруднення СанПіН 4630-88 для поверхневих водних об'єктів культурно-побутового водокористування. Відхилення показників якості шахтної води, що скидається у водні об'єкти, в основному, відзначаються по сухому залишку, хлоридів, сульфатів. Дані речовини, згідно санітарної класифікації, віднесені до 4 класу небезпеки – помірно небезпечні речовини. Вода в поверхневих водних об'єктах, розташованих на території м.Донецька, не відповідає нормативам якості води для водних об'єктів господарсько-питного призначення, і відповідно, не використовується для питного водопостачання. За результатами лабораторних досліджень, якість води водойм не відповідає санітарним нормам для купання. Однак в місті є водойми, які в літній період стихійно використовуються населенням для відпочинку і купання. Основні джерела забруднення водойм м. Донецька: скидання стічних вод від промислових підприємств з наявністю неефективної системи очищення; скидання шахтних вод; витоку каналізаційних колекторів; стихійні звалища твердих побутових відходів, влаштування городів в межах прибережних захисних смуг водойм; зливові / поверхневі стоки з міських територій.
2. Вміст ртуті у водних Об'єктах м. Донецька
Ртуть в дуже малих кількостях присутній в поверхневих природних водах, основним її сховищем у водних системах є донні відкладення. На знаходження у водному середовищі тієї чи іншої форми ртуті впливають кислотність водного середовища і її окислювальний потенціал. У водах ртуть мігрує в двох основних фазових станах-в розчині вод (розчинені форми) і в складі суспензії (Зважені форми). У свою чергу, в розчині вод вона може перебувати у вигляді двовалентного іона, гідроксиду ртуті, комплексних сполук (з хлором, органічною речовиною та ін.). Серед сполук Hg (II), за своїм екологічним і токсикологічним значенням особлива роль належить ртутьорганічним сполукам. Найважливішими акумуляторами ртуті, особливо в умовах забруднення, є суспензія і донні відкладення водних об'єктів. Найбільш високими концентраціями ртуті характеризуються техногенні мули, активно накопичуються в річках і водоймах, куди надходять стічні води промисловості. Рівні вмісту ртуті в них досягають 100-300 мг/кг і більше (при фоні до 0,1 мг/кг). Відомі випадки, коли кількість ртуті, що надійшла зі стічними водами і накопичилася в таких мулах, становила десятки і сотні тонн. Нормальне функціонування таких річок і водойм, їх практичне використання можливе тільки при видаленні забруднених відкладень. Використання забруднених ртуттю вод для зрошення сільськогосподарських угідь призводило до її накопичення в сільгосппродукції до рівнів, що перевищують ГДК. Наявність ртуті в поверхневих водних об'єктах м. Донецька обумовлено більшою мірою техногенним надходженням цього елемента. Хімічний склад річкових вод знаходиться в прямій залежності не тільки від хімічного складу поверхневого стоку і підземних вод, а й від хімічного складу і кількості скидаються вод. Значний внесок вносять стічні води вугільних підприємств (шахтні води). Вміст ртуті в шахтних водах обумовлено їх кількістю в підземних водах вугленосних відкладень і процесами, пов'язаними з міграцією цього елемента з гірських порід в шахтні води. При певних умовах ртуть може накопичуватися в поверхневих і грунтових водах в кількостях, що не дозволяють використовувати їх в народному господарстві, часто негативно впливаючи на водойми господарсько-питного і рибогосподарського призначення.
3. МЕТОДИ ХІМІЧНОГО АНАЛІЗУ
3.1 Визначення вмісту розчинених газів у воді
Кількість кисню, розчиненого у воді, має велике значення для оцінки стану водойми. На його вміст у воді впливають дві групи протилежно спрямованих процесів: одні збільшують концентрацію кисню, інші зменшують її. До першої групи процесів, що збагачують воду киснем, слід віднести: процес абсорбції кисню з атмосфери; виділення кисню водною рослинністю в процесі фотосинтезу; надходження у водойми з дощовими і сніговими водами, які зазвичай пересичені киснем. Абсорбція кисню з атмосфери відбувається на поверхні водного об'єкта, її швидкість підвищується зі зниженням температури, з підвищенням тиску і зниженням мінералізації. Фотосинтетичне виділення кисню прикріпленими, плаваючими рослинами і фітопланктоном відбувається тим сильніше, чим вище температура води, інтенсивність сонячного освітлення і більше поживних речовин у воді. Вміст розчиненого кисню схильне сезонним і добовим коливанням. Його зниження вказує на різку зміну біологічних процесів у водоймах, а також на забруднення водойм. Метод заснований на здатності гідрату закису марганцю окислюватися в лужному середовищі в з'єднання вищої валентності, кількісно пов'язуючи розчинений у воді кисень, і потім знову переходити в кислому середовищі в двовалентні з'єднання, окислюючи при цьому еквівалентну (пов'язаному кисню) кількість йоду. Виділився при цьому йод визначається титруванням тіосульфатом.
3.2 Визначення заліза в поверхневих водах
Залізо постійно присутній в поверхневих і підземних водах; концентрація його в цих водах залежить від геологічної будови і гідрологічних умов басейну. Високий вміст заліза в поверхневих водах вказує на забруднення їх шахтними або промисловими стічними водами, особливо водами підприємств металургійної, металообробної, текстильної, лакофарбової промисловості, з сільськогосподарськими стоками. Сполуки заліза не володіють вираженими токсичними властивостями, але погіршують якість води, надаючи їй при концентрації більше 0,3 мг/дм3 неприємний залозистий присмак. Після прання в такій воді на тканинах з'являються іржаві плями. Такі ж плями з'являються на посуді, в раковині і в ваннах. Допустима концентрація заліза в питній воді становить 0,3 мг / дм3. Вміст загального заліза у воді визначають фотоколориметрично на підставі реакції іонів Fe3+ з роданід-іоном, сульфосаліциловою кислотою або о-фенантроліном. Колориметричний аналіз заліза з сульфосаліциловою кислотою заснований на реакції сульфосаліцилової кислоти з солями заліза в лужному середовищі з утворенням жовтого комплексу заліза. Цим способом можна встановити 0,1-10 мг/дм3, заліза з точністю 0,1 мг/дм3. При реакції о-фенантроліну з іонами заліза (III) в області рН від 3 до 9 утворюється червоно-фіолетове Комплексне з'єднання. Пряме визначення можливе при вмісті заліза 0,05-2 мг в 1 дм3 води, при цьому не потрібно попереднього консервування проби
3.3 Визначення концентрації іонів водню (рН)
Потенціометричний (електрометричний) метод визначення величини pH води зі скляним електродом більш універсальний і точний. Більшість серійних рН-метрів дозволяє проводити вимірювання з точністю 0,05-0,02 одиниці pH. Він придатний для аналізу вод з широким діапазоном мінералізації і містять пофарбовані і зважені речовини. Метод заснований на вимірюванні різниці потенціалів, що виникають на кордонах між зовнішньою поверхнею скляної мембрани електрода і досліджуваним розчином, з одного боку, і 27 внутрішньою поверхнею мембрани і стандартним розчином кислоти, з іншого. Так як внутрішній стандартний розчин скляного електрода має постійну активність іонів водню, потенціал на внутрішній поверхні мембрани не змінюється і вимірювана різниця потенціалів визначається потенціалом, що виникає на межі зовнішньої поверхні електрода і досліджуваного розчину. Вимірювання виробляють щодо потенціалу іншого, електрода, званого електродом порівняння. В якості останнього. вибирають такий електрод, потенціал якого практично не залежить від активності іонів водню, наприклад, каломельний, хлорсеребряний. Електрорушійна сила, що виникає в вимірювальних осередках, складених з індикаторного (скляного) електрода, електродів порівняння (каломельного, хлорсеребряного) - досліджуваного розчину і розчинів з постійною активністю водневих іонів є функцією активності іонів водню (pH) в досліджуваному розчині (і температури). Вміст у поверхневих водах. Величина концентрації іонів водню (рН) в річкових водах зазвичай коливається в межах 6,5-6,0, океані 7,9-8,3 рН. рН води шахт і рудників досягає іноді одиниці, а содових озер і термальних джерел десяти. Концентрація іонів водню схильна до сезонних коливань. Взимку величина рН для більшості річкових вод становить 6,8-7,4, влітку 7,4-8,2.
3.4 Визначення фізичних показників якості води
Фізичними показниками якості води є її температура, запах і смак, каламутність, прозорість, кольоровість. Температура води Температура води залежить від місця розташування джерела, пори року, температури тих грунтів, з якими вона стикається. Температура поверхневих вод схильна до істотних коливань, в той час як на водах підземних джерел сезонні коливання температур відображаються мало. Найбільш сприятлива температура питної води знаходиться в інтервалі 7-12°С, вона має найбільш приємний і освіжаючий смак. Вода з високою температурою містить в собі мало розчинених газів, тому вона погано втамовує спрагу і неприємна на смак. Температура визначається виключно в момент відбору проб ртутним термометром з ціною поділки 0,1-0,5°С, який опускають на задану глибину і витримують протягом 3-10 хв. Запах і смак Запах і смак природних вод залежать від температури води, розчинних у воді газів і хімічного складу домішок. Запах води визначається летючими пахнуть речовинами. Велику роль у формуванні запаху і присмаку природних вод грає життєдіяльність гідробіонтів, особливо біохімічне розкладання органічних речовин мікроорганізмами, виділення різних специфічних органічних сполук деякими водоростями і мікроорганізмами, особливо при масовому їх розвитку, наприклад, при цвітінні водойми, природа хімічних компонентів, що надходять в даний водойма в результаті природних причин або зі стічними водами підприємств. За характером запахи діляться на дві групи: запахи природного походження, причиною яких є живуть і відмерлі у воді організми, що оточують грунти, загнивають рослинні залишки і т. д. визначення таким запахам дають відповідно до класифікації запахи штучного походження, що викликаються домішками деяких промислових стічних вод, реагентами для обробки водопровідної води і т. д. ці запахи отримують назву за відповідною речовиною: фенольний, бензиновий, хлорний і ін. Розрізняють чотири види смаку води: солоний, гіркий, солодкий і кислий. Інші види смакових відчуттів називають присмаками. Причиною присмаку води може бути присутність в ній сірководню, нафтопродуктів, зокрема, фенолу, деяких солей. Так, солі заліза (II) і марганцю (II) надають воді залозистий смак, сульфат кальцію –терпкий, сульфат магнію – гіркий, хлорид натрію – солоний смак. Характер і інтенсивність запаху і смаку води визначають органолептично: дають експертну якісну характеристику і оцінюють інтенсивність в балах за п'ятибальною системою. Кольоровість води Чиста вода в тонких шарах безбарвна. У товстому шарі вона має блакитний відтінок. Інші відтінки свідчать про наявність у воді різних розчинених і зважених домішок. Колір природних вод відкритих водойм найчастіше обумовлюється наявністю гумінових речовин, що забарвлюють воду в різні відтінки жовтого і бурого кольору. Кількість цих речовин залежить від геологічних умов, характеру грунтів, наявності боліт і торфовищ в басейні річки і т.п. колоїдні залізисті сполуки надають воді відтінки від жовтуватих до зелених. При попаданні у воду відходів різних виробництв її колір може змінюватися в залежності від кольору забруднюючих речовин. Кольоровість визначають колориметрично або фотометрично, порівнюючи колір досліджуваної води з еталонною шкалою, що імітує забарвлення природних вод. Для цього використовують платино-кобальтову або дихромато-кобальтову шкалу. Результати виражають в умовних одиницях-градусах кольоровості. Кольоровість природних вод варіює від декількох одиниць до декількох тисяч градусів. Прозорість і каламутність Прозорість (або світлопропускання) і каламутність води є фізичною характеристикою води, що залежить від присутності у воді забарвлених і зважених органічних і мінеральних речовин. Мірою прозорості служить висота стовпа води, при якій можна спостерігати опускається в водойму білу пластину певних розмірів (диск Секкі) або розрізнити на білому папері стандартний шрифт певного розміру і типу (як правило, шрифт середньої жирності висотою 3,5 мм). При регулярному контролі роботи водопідготовчих станцій і при визначенні якості води у водопровідній мережі прозорість води визначається за методом Хреста. Результати виражають в сантиметрах із зазначенням способу вимірювання. При вмісті у воді зважених речовин більше 3 мг / дм3 знаходять величину, зворотну прозорості – - каламутність води. Каламутність води встановлюють, порівнюючи каламутність досліджуваної води зі стандартами, і висловлюють в мг / дм3. Визначення прозорості (каламутності) води – обов'язковий компонент програм спостережень за станом водних об'єктів. Підвищення каламутності води може бути обумовлено наявністю в ній гумінових речовин, колоїдних сполук заліза, зважених і забарвлених речовин, що є відходами виробництва, а також масовим розвитком водоростей, що характерно для забруднених і атрофованих водойм.
3.5 Визначення важких металів
Важкі метали виділяються із загальної групи металів за специфічною шкідливістю для живих організмів. Поняття "важкі метали" не відноситься до строго визначених. Різні автори в складі групи важких металів вказують різні хімічні елементи. В екологічних публікаціях в цю групу включають близько 40 елементів з атомною масою понад 50 атомних одиниць. Н. Ф. Реймерс відносить до важких метали з щільністю більше 8 г/см3, виділяючи при цьому підгрупу благородних металів. Таким чином, до власне "важких" віднесені мідь, нікель, кадмій, кобальт, вісмут, ртуть, свинець. Група фахівців, що працює під патронажем Європейської Економічної Комісії ООН і займається моніторингом викидів в навколишнє природне середовище важких металів, включає в цю групу також цинк, миш'як, селен, сурму.
3.6 Визначення хлоридів і сульфатів
Концентрація хлоридів у водоймах-джерелах водопостачання допускається до 350 мг/л. У поверхневих водах кількість хлоридів залежить від характеру порід, що складають басейни, і варіює в значних межах - від десятих часток до 1000 міліграмів на літр. Концентрація хлоридів у поверхневих водах схильна до помітних сезонних коливань, що корелює зі зміною загальної мінералізації води. Принцип методу. Хлориди визначають титруванням проби аналізованої води нітратом срібла в присутності хромату калію як індикатора. Нітрат срібла дає з хлорид-іонами білий осад, а з хроматом калію - кирпичнокрасный осад хромату срібла. З утворилися опадів меншою розчинністю володіє хлорид срібла. Тому, лише після того, як хлорид - іони будуть пов'язані, починається утворення червоного хромату срібла. Поява оранжево-бурого забарвлення свідчить про кінець реакції. Титрування можна проводити в нейтральному або слаболужному середовищі. Якщо pH досліджуваної проби менше 7, аналізовану воду нейтралізують 0,01 М розчином гідрокарбонату натрію, а якщо більше - 0,01 М розчином сірчаної кислоти. Контроль за pH ведуть за допомогою універсальної лакмусового папірця. Виконання вимірювань масової концентрації сульфатів титриметричним методом засноване на утворенні важкорозчинного сульфату барію при додаванні розчину хлориду барію до аналізованої воді. Після практично повного осадження сульфатів надлишок іонів барію реагує з індикатором з утворенням комплексної сполуки. При цьому забарвлення розчину змінюється від синьо-фіолетового (фіолетового) до блакитного. Для зменшення розчинності осаду сульфату барію титрування проводять у водно-спиртовому або водно-ацетоновому середовищі. Рівняння реакцій напишіть самостійно. Діапазон вимірювань 30-300 мг
4. РЕЗУЛЬТАТИ ГІДРОХІМІЧНОГО АНАЛІЗУ ВОДИ
Гідрохімічний контроль за якістю води складається з системи контролю і спостережень: за хімічним складом води водойм і водотоків басейну; вступниками атмосферними опадами; антропогенними джерелами забруднення. Мережа гідрохімічних спостережень створюється з урахуванням скидів стічних вод, а також видів водокористування. Склад і обсяг гідрохімічних спостережень визначається вимогами, що пред'являються органами державного управління і нагляду і основними водокористувачами. При цьому зазвичай визначаються: мінералізація; вміст кисню; біологічне споживання кисню (БПК); хімічне споживання кисню (ГПК); вміст основних іонів, біогенних речовин, нафтопродуктів, детергентів, фенолів, пестицидів, важких металів. Визначаються також фізичні параметри: кольоровість, температура.
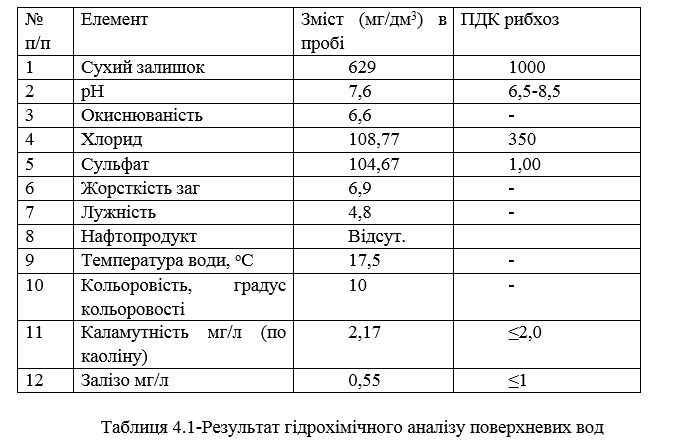
4.1 Результат гідрохімічного аналізу поверхневих вод
ВИСНОВОК
В результаті хімічного аналізу ми з'ясували, що показник сульфатів перевищує допустиму концентрацію. Є показником забруднення поверхневих вод виробничими стічними водами і підземних вод водами вищерозміщених водоносних горизонтів. Атмосферний двоокис сірки (SO2), що утворюється при згорянні палива і виділяється в процесах випалу в металургії, може робити внесок у вміст сульфатів в поверхневих водах.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
1. Другов, Ю. С. Анализ загрязненной воды: практическое руководство / Ю. С. Другов, А. А. Родин. — Москва: БИНОМ. Лаборатория знаний, 2012. — 678 с.
2. Алекин О.А., Семенов А.Д., Скопинцев Б.А. Руководство по химическому анализу вод суши.- Л.,Гидрометеоиздат, 1973.- 268с.
3. Семенов А.Д. Руководство по химическому анализу поверхностных вод суши.- Л., Гидрометеоиздат, 1977.- 541с.
4. Евдокимов, С.А. Обобщающие показатели качества поверхностных вод/ С.А. Евдокимов // Водные ресурсы, №2, 1990. С. 109-115.
5. Методические основы оценки антропогенного влияния на качество поверхностных вод / Под ред. А.В. Караушева. Л.:Гидрометеоиздат. - 1981. - 176 с.
6. СанПиН 2.1.5.980-00 Гигиенические требования к охране поверхностных вод. Дата введения 2001-01-01.
7. Петросян В. С. Загрязнение ртутью: причины и последствия / В. С. Петросян // Экология и промышленность, 1999, № 12. C. 34–38
8. Рамамурти, С. Е. Тяжелые металлы в природных водах / С. Е. Рамамурти. – М.: Мир, 1987. – 286 с.


