Аннотация
В этой работе было исследовано борирование сталей электролизом расплавленной соли в электролите на основе буры при различных плотностях тока (50–700 мА/см2),температурах (800–1000°C) и времени (0–2 ч). Оптимальные условия были определены с учетом толщины, твердости и морфологии боридного слоя. В зависимости от количества рассеянного бора с поверхности на матрицу могут образовываться различные борированные фазы следующим образом: FeBх (x>1)→FeB→Fe2B→Fe3B, FeyB (y>3)→Fe. Определены оптимальные условия для проведения борирование низкоуглеродистой стали DIN EN10130-99: 10% Na2CO3 + 90% Na2B4O7, 900°C, 1 час и 200 мА/см2. Коррозионные испытания данного материала проводились в различных средах: HCl, H2SO4, HNO3, H3PO4 и HClO4 (10% об.). Электрохимически борированная низкоуглеродистая сталь показала скорость коррозии 0,66 г/см2/сут в HCl, 1,13 г/см2/сут в H2SO4, 1,59 г/см2/сут в HClO4 и 3,37 г/см2/сут в H3PO4. Однако она не была устойчив к воздействию HNO3 со значительной скоростью коррозии 0,3 г/см2/сут.
1. Введение
Процесс борирования улучшает свойства поверхности по твердости, износу, усталости, окислению и коррозии (по отношению к неокисляющимся разбавленным кислотным растворам, щелочным средам и расплавленным металлам). Промышленные процессы борирования могут быть применены к большинству черных материалов, таких как конструкционные стали; корпусные закаленные, отпущенные, инструментальные и нержавеющие стали; литые стали; чугун Armco; серый и ковкий чугун; а также спеченный чугуни сталь [1, 2].
Термохимическое борирование, как правило, предпочтительнее в промышленности, поскольку оно технологически проще и позволяет наносить покрытие равномерно на сложные поверхности, однако продолжительность обработки большая (около 5 часов). Однако электролитический процесс обеспечивает более высокую скорость роста боридного слоя для придания материалу более простой формы за короткое время (около 30 мин) [3, 4].
Муассан [1] еще в 1895 году предложил борировать сталь. В то время промышленное применение электрохимических процессов было ограничено, поэтому исследования в этой области больше не проводились. В ограниченных исследованиях Сегерс, Фонтана и Винанд [3] изучалось влияние плотности тока и времени на толщину покрытия и морфологию поверхности в расплавленном Na2B4O7 при различных температурах (900–1050°C). Исследования показали, что Fe2B или FeB + Fe2B фазы формировались в зависимости от приложенной плотности тока и температуры. Матиасовский и его группа [4] обнаружили, что образование боридного слоя контролировалось диффузией бора на поверхность. Кроме того, Ткачев, Григоров и Катханов [5] исследовали возможный механизм реакции при электрохимическом борировании. Другое исследование было проведено Ханом и Чуном [6], которые исследовали влияние компонентов смеси на структуру слоя.
Борирование, которое может значительно повысить коррозионно-эрозионную стойкость железистых материалов в неокисляющихся разбавленных кислотах и щелочных средах, все чаще используется с этой целью во многих отраслях промышленности. Также поверхность обладает высокой твердостью, умеренной стойкостью к окислению (до 850°C) и достаточно устойчива к расплавленным металлам, таким как цинк [1, 2].
Коррозионное поведение и свойства электрохимически полученного боридного слоя еще не изучались, в то время как коррозионные свойства боридного слоя, полученного другими методами (термохимический, реактор с псевдоожиженным слоем и т.д.), были проведены лишь в нескольких исследованиях [1, 2, 7, 8].
Было изучено борирование сталей электрохимическим восстановлением из расплавленных солей и условия электролиза (состав электролита, плотность тока, температура и время) фиксировали с учетом твердости, морфологии и толщины полученного боридного слоя. Кроме того, была исследована коррозионная стойкость слоев, которые были изготовлены при оптимальных условиях, в разбавленных кислых растворах.
2. Экспериментальные исследования
2.1 Ячейки и печь
Эксперименты по борированию электролизом в расплавленной соли проводились в высокочастотной печи, содержащей графитовый тигель с платиновыми анодами и стальной катодный материал. Ток подавался в цифровом виде от источника постоянного тока источник (0,001 мА). Во время электролиза температура внутренней стороны электролита контролировалась с помощью термопары изнутри и лазерного термометра с внешней поверхности, чтобы исключить риск воздействия электрического тока на измерения термопары.
2.2 Экспериментальная процедура
На протяжении всех экспериментов, прежде чем поместить катодный материал в электролит, катод полировался, чтобы обезжирить поверхность и получить определенную шероховатость. В конце каждого эксперимента, катод извлекали из электролита и оставляли на воздухе, после чего отключали ток. Затвердевший электролит на поверхности катода удаляли кипящей водой.
Для подготовки борированной поверхности были применены обычные методы полировки, чтобы измерить толщину слоя в восьми различных точках, которые были определены ранее. Толщины слоев FeB и Fe2B измерялись поочередно и вычислялось среднее значение. Контраст фазовой составляющей слоя был легко различим, поэтому травление не всегда было необходимым. Состав боридного слоя был охарактеризован с поверхности методом тонкопленочного рентгеноструктурного анализа (XRD) с использованием излучения Cu–Ka (10 кВ, 10 мА). Кроме того, значения твердости были измерены все фазы. Полученный боридный слой при оптимальных условиях подвергали коррозионным испытаниям с содержанием 10%-ных растворов HCl, H2SO4, HNO3, H3PO4 и HClO4 на 48 часов.
3. Результаты и обсуждениее
Эксперименты по электролизу были проведены в различных условиях с целью определения оптимальных параметров электрохимического борирования низкоуглеродистой стали, состав которой приведен в таблице 1.
Таблица 1 — Химический состав стали , % масс.

Была установлена приемлемая твердость поверхности и однородный толстый слой. Эксперименты показали, что оптимальными условиями для борирования низкоуглеродистой стали DIN EN10130-99 являются 10% Na2CO3 + 90% Na2B4O7, 900°C, 1 час и 200 мА/см2.
Рентгеноструктурный анализ борированного слоя (рис. 1) показывает, что на поверхности образовались фазы FeB, Fe2B и Fe3B. Фазы FeB и Fe2B, образовавшиеся на поверхности, также упоминались другими исследователями. При электролитическом борировании была обнаружена фаза Fe3B и определено ее возможное положение (рис. 2).
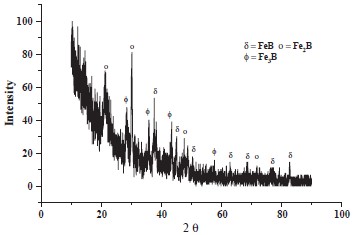
Рисунок 1 — Рентгенограмма борированного слоя стали

Рисунок 2 — Микроструктура борированного слоя стали
На рентгенограмме, приведенной на рис. 1, и снимке микроструктуры, приведенной на рис. 2 показан боридный слой, состоящий из различных соединений FeB–FeBх (x>1) и могут быть образованы в соответствующем электролите путем поляризации. В ходе экспериментов по борированию могут образовываться различные борированные фазы в зависимости от количества рассеянного бора от поверхности к матрице следующим образом: FeBх (x>1)→FeB→Fe2B→Fe3B, FeyB (y>3)→Fe. Типичная микрофотография борированного слоя (рис. 3а) и профиль твердости (рис. 3b) слоя, полученного при оптимальных экспериментальных условиях, приведены ниже. При исследовании микроструктуры рост слоя происходил в виде зубев, и известно, что эффективный параметры этой структуры зависят от морфологии роста, состава и структурных дефектов.
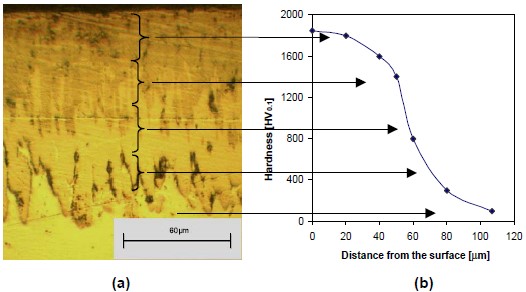
Рисунок 3 — Типичная микрофотография боридного слоя (а) и профиль твердости на слое (b)
Длина пиков
и впадин
слоя была измерена в восьми различных точках, и средние значения этих измерений рассчитаны для определения общей толщины
слоя. Было обнаружено, что общая толщина слоя составляет 120 мкм для идеального боридного слоя и 75 мкм для идеального слоя FeB.
На рис. 3 показана разница между слоями FeB и Fe2B, поэтому моделирование профиля твердости фаз, которое произошло в результате диффузии бора, может быть легко получено.
Профили твердости определялись по методу Виккерса (100 г). Типичный пример двухслойного покрытия приведен на рис. 3b. Самые высокие значения твердости получены для FeB (1890 HV), но слои Fe2B также очень твердые (1572 HV) по сравнению со стальной подложкой (100 HV).
Известно, что одной из целей процесса борирования является повышение коррозионной стойкости материалов путем обработки поверхности. Для определения коррозионных свойств электрохимически сформированного боридного слоя проводились испытания по выдержке в 10%-ных растворах H2SO4, HNO3, H3PO4 и HClO4 на протяжении 48 ч.
В конце этих испытаний были получены изменения массы образцов в зависимости от времени выдержки, результаты приведены на рис. 4а для растворов HCl, H2SO4, H3PO4 и на рис. 4b для растворов HClO4, HNO3.
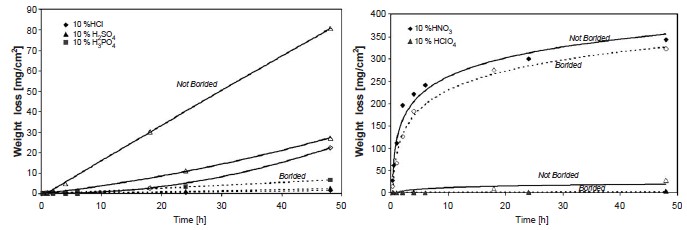
Рисунок 4 — Потеря массы образца в неокисляющем (а) и окисляющем (b) кислотном растворе
4. Выводы
- Определены оптимальные условия для борирования низкоуглеродистой стали: 10% Na2CO3 + 90% Na2B4O7, 900°C, 1 час и 200 мА/см2.
- В конце процесса борирования могут образовываться различные борированные фазы в зависимости от количества рассеянного атома бора от поверхности к матрице следующим образом: FeBх (x>1)→FeB→Fe2B→Fe3B, Fey (y>3)→Fe.
- Рост слоя происходил в виде зубьев, и известно, что эффективные параметры этой структуры зависят от морфологии роста, состава и структурных дефектов. Было установлено, что общая толщина слоя составляет должно быть 120 мкм для идеального боридного слоя и 75 мкм для идеального слоя FeB.
- Твердость слоя, в соответствии с диффузионным количеством бора и образованием фазы FeBх, уменьшалась от поверхности (1900 HV) к матрице (100 HV).
- Испытания на коррозию данного материала проводились в различных средах, таких как; HCl, H2SO4, HNO3, H3PO4 и HClO4 (10% об.). Электрохимически борированная низкоуглеродистая сталь показала скорость коррозии в 0,66 г/см2/сутки в HCl, 1,13 г/см2/сутки в H2SO4, 1,59 г/см2/сутки в HClO4, 3,37 г/см2/сутки в H3PO4. Однако она не была устойчива к воздействию HNO3 со значительной скоростью коррозии 0,3 г/см2/сут. и 200 мА/см2.
Список использованной литературы
1. A.G. Von Matuschka, Boronizing, Heyden and Son Inc., Philadelphia,1980.
2. A.K. Sinha, Heat Treat. 4 (1991) 437.
3. L. Segers, A. Fontana, R. Winand, Electrochim. Acta 36 (1991) 41.
4. K. Matiasovsky, M. Chrenkova-Paucirova, P. Fellner, M. Makyta, Surf. Coat. Technol. 35 (1988) 133.
5. V.N. Tkachev, P.K. Grigorov, B.B. Katkhanov, Met. Sci. Heat Treat. 17 (1975) 348.
6. S.H. Han, J.S. Chun, J. Mater. Sci. 15 (1980) 1379.
7. E. AtNk, U. Yunker, C. Meric, Tribol. Int. 36 (2003) 155.
8. T. Wierzchon, P. Bielinski, K. Sikorski, Surf. Coat. Technol. 73 (1995) 121.