| на главную | |
Массоперенос кислорода в системе шлак-металл
Дымнич А.Х., Троянский А.А. Разинов А.Н
(кафедра ЭМиКПС)
Производительность сталеплавильных агрегатов в значимой степени определяется интенсивностью удаления примесей металла. В свою очередь скорость рафинировочных процессов определяется интенсивностью поступления кислорода в металл.
В работе рассматривается случай массопередачи кислорода из шлака в металл, когда эти фазы периодически возмущаются газовыми потоками.
В основу решения задачи была положена модель Хигби, согласно которой предполагается, что при пересечении поверхности раздела шлак-металл пузырьками оксида углерода мгновенно нарушаются градиенты концентраций диффундирующих компонентов в каждой из фаз. Это приводит к нестационарному переносу масс от одной фазы к другой, с восстановлением концентрационных градиентов в них до появления следующего пузырька. Следовательно, рассматриваемая задача сводится к определению количества вещества, перешедшего из одной фазы в другую за время, определяемой частотой образования пузырьков оксида углерода. Следует сразу же отметить, что границы применимости такой модели массопередачи ограничены прежде всего самой гидродинамикой. Увеличение скорости движения жидких фаз способствует развитию межфазной турбулентности (образование шлаковой эмульсии в металле и наоборот), где массоперенос становится микрогетерогенным. Поэтому предложенная модель наиболее оправдана при низкой и умеренной скоростях окисления углерода.
Рассматривается следующий механизм массопереноса кислорода. Кислород газовой фазы адсорбируется на поверхности шлака по реакции
![]() .(1)
.(1)
Образовавшийся в результате этой реакции диоксид железа (Fe2O3) конвективной диффузией доставляется к границе шлак-металл, где протекает следующая реакция
![]() .(2)
.(2)
Таким образом, поверхность шлак-металл является источником образования оксида железа (FeO), который распределяется между шлаком и металлом.
Применительно к этой задаче для 3-х компонентной системы можно записать следующую систему дифференциальных уравнений:
 (3)
(3)
 ,(4) ,
,(4) , .(5)
.(5)
где ![]() ,
, ![]() ,
, ![]() – концентрация закиси
и окиси железа в шлаке, и кислорода в металле;
– концентрация закиси
и окиси железа в шлаке, и кислорода в металле;
![]() ,
, ![]() ,
, ![]() – коэффициенты
диффузии FeO Fe2O3 в шлаке, и кислорода в металле;
– коэффициенты
диффузии FeO Fe2O3 в шлаке, и кислорода в металле;
х – координата, в направлении которой происходит диффузия.
Согласно принятой модели
в момент пересечения границы раздела шлак-металл пузырьками СО поверхностные
концентрации ![]() и
и
![]() в шлаке и
в шлаке и
![]() в металле равны
объемным. Следовательно начальные условия можно записать:
в металле равны
объемным. Следовательно начальные условия можно записать:
![]() , (5)
, (5)
![]() ,
, ![]() ,
, ![]() – среднемассовые
концентрации компонентов в шлаке и металле.
– среднемассовые
концентрации компонентов в шлаке и металле.
Так как концентрация железа
(CFe) на межфазной границе высока, можно принять, что скорость
образования закиси железа на ней (WFeO) пропорциональна концентрации
![]() (реакция первого порядка)
(реакция первого порядка)
![]() , (7)
, (7)
где k1 – константа скорости химической реакции (2).
Тогда скоростьрасходования Fe2O3 у этой границы можно представить как
![]() , (8)
, (8)
В выражении (8) коэффициент пересчета определяется следующим соотношением:
 ,
,
где ![]() и
и ![]() – молекулярный вес
диоксида железа и чистого железа.
– молекулярный вес
диоксида железа и чистого железа.
Выбрав границу раздела
фаз, где выполняется условие фазового равновесия, за начало отсчета, можно
записать следующие граничные условия: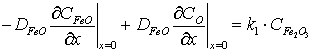 ; (9)
; (9)
 ; (10)
; (10)где f – коэффициент активности железа в шлаке;
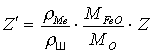 – константа распределения кислорода между металлом и шлаком;
– константа распределения кислорода между металлом и шлаком;
![]() ,
,![]() – плотность металла и шлака соответственно, г/см3.
– плотность металла и шлака соответственно, г/см3.
Вдали от поверхности раздела фаз концентрации диффундирующих компонентов равны объемным, т.е.:
![]() .(12)
.(12)
Система дифференциальных уравнений (3 – 5) совместно с начальными (6) и граничными (9 – 12) условиями была решена операционным методом.
Из решения задачи был определен среднеинтегральный диффузионный поток кислорода из шлака в металл. Для случая, когда химические реакции (1) и (2) протекают с большой скоростью (k1→ ∞,k2 → ∞) диффузионный поток кислорода из шлака в металл определяется уравнением
 (13)
(13)
где j0ш-м – плотность диффузионного потока кислорода из шлака в металл, кг∙моль/(м2∙с).
τе – время между появлением последующего пузырька, с.
В уравнении (13) выражение  определяет
окислительный потенциал шлаковой фазы.
определяет
окислительный потенциал шлаковой фазы.
Запишем выражение
 ,
,
где k – коэффициент массопередачи кислорода из шлаковой в металлическую фазу.
Коэффициент массопередачи k можно записать в другой форме
![]() ,
,
где  – коэффициент массоотдачи оксида железа в шлаковой фазе,
м/с;
– коэффициент массоотдачи оксида железа в шлаковой фазе,
м/с;
 – коэффициент массоотдачи кислорода в металле, м/с.
– коэффициент массоотдачи кислорода в металле, м/с.
Следовательно
коэффициенты массоотдачи (βш и βм) и
массопередачи зависят о коэффициентов диффузии компонентов в соответствующих
фазах и частоты «бомбардировки»  поверхности раздела фаз пузырьками оксида углерода.
поверхности раздела фаз пузырьками оксида углерода.
Время между появлением двух смежных пузырьков СО в одном и том же участке металлической ванны (τе) определяется из следующего соотношения:
![]() ,(15)
,(15)
где V – объем пузырька на выходе из металлической ванны;
T – температура жидкого металла;
vc – скорость окисления углерода;
G – вес металлической ванны.
Параметр Fп зависит от радиуса пузырька СО и определяется как
![]() ,
,
где rп – радиус пузырька СО на выходе из ванны.
Размер лопающихся на поверхности шлака пузырьков окиси углерода в период доводки плавки определили с помощью фотосъемки. На основании этих исследований было установлено, что при скорости окисления углерода металлической ванны емкостью 300т равнойvc=0,30 %С/час объем пузырьков на выходе из ванны составляет 100 – 700 см3.
Для этих значений время между появлением пузырьков (τе) составляет
τе = 0,15 – 0,26сек.
Подставляя значение τе в уравнение (14) определяем величину коэффициента массопередачи кислорода в металл. Расчеты показали, что коэффициент массоопередачи k колеблется в пределах k =(0,16 – 0,24)10-2м/с, что удовлетворительно согласуется с экспериментальными данными А. Даркена k=2∙10-2м/с).
Выводы. Используя диффузионную модель Хигби были определены диффузионный поток и коэффициент массопередачи кислорода из шлака в металл при барботаже фаз пузырьками оксида углерода. Полученные значения коэффициента массоопередачи удовлетворительно согласуется с экспериментальными данными.