Реферат по теме выпускной работы
План
- 1. Актуальность, цель и задачи работы
- 2. Твёрдый остаток низкотемпературного пиролиза автомобильных шин и его технический анализ
- 3. Общая характеристика процессов адсорбции
- 4. Методики экспериментальных исследований и полученные результаты
- Выводы
- Список источников
1. Актуальность, цель и задачи работы
Сорбция является одним из универсальных методов очистки и доочистки сточных вод от растворённых органических соединений природного и неприродного происхождения таких производств, как коксохимические, сульфат-целлюлозные, хлорорганические, синтеза полупродуктов, красителей и др.
В качестве сорбентов применяют различные искусственные и природные пористые материалы: активированные угли, золу, коксовую мелочь, силикагели, алюмогели, активные глины и земли. Наиболее распространенным сорбентом в отечественной и зарубежной практике является активированный уголь, гранулированный и порошкообразный. Вместе с тем, сорбционные свойства активированных углей проявляются только в отношении органических загрязнений, а их широкое использование на практике сдерживается высокой стоимостью и дефицитностью [1]. Поэтому актуальным является поиск новых сорбентов, которые по своим характеристикам не будут уступать известным маркам активированных углей, а их использование будет экономически целесообразно.
В последнее время наметилась тенденция поиска новых углесодержащих веществ для производства сорбентов, потребность в которых в Украине велика, как для очистки сточных вод, так и для обезвреживания отходящих газов. Известны методы получения сорбентов из лингина (твёрдый отход переработки древесины), нефтяных отходов, изношенных автомобильных шин, сельскохозяйственных и других отходов [2]. Например, такой метод как низкотемпературный пиролиз, позволяет получить из автошин до 45 % твёрдого остатка, содержащего около 90 % масс. углерода, который по своим свойствам является хорошим сорбирующим материалом. С другой стороны, этот метод позволяет рекуперировать значительное количество отработанных шин, которые трудно обезвредить другими экологичными методами.
Целью магистерской работы является экспериментальное изучение сорбционных свойств, качественных и количественных характеристик твёрдого продукта пиролиза изношенных автомобильных шин.
Поставленные задачи: 1. Проведение технического анализа твёрдого остатка. 2. Экспериментальное определение сорбционной ёмкости твёрдого остатка относительно йода и органических красителей: метиленового синего, метилового красного и оранжевого в статических условиях по стандартным методикам. 3. Исследование сорбционных свойств твёрдого остатка относительно некоторых органических загрязнителей и ионов тяжелых металлов.
2. Твёрдый остаток низкотемпературного пиролиза автомобильных шин и его технический анализ
Проблема утилизации отходов, в том числе изношенных автомобильных шин, в современном обществе остается важной, несмотря на развитие технологии производства новой экологически безопасной продукции. Складирование, утилизация и захоронение отходов экономически неэффективно и экологически небезопасно, так как при длительном хранении они могут выделять в окружающую среду вещества, способные привести к нарушению экологического равновесия[3]. Одним из перспективных методов утилизации является низкотемпературный пиролиз – термическое разложение органических веществ без доступа воздуха при температуре (400?500) °С. В настоящее время прошла испытание опытная установка низкотемпературного пиролиза по переработке изношенных автомобильных шин [4]. В результате пиролиза помимо жидких и газообразных продуктов образуется твёрдый остаток, который может быть использован в качестве сорбента.
Показатели качества твёрдого остатка, полученные в результате технического анализа, представлены в таблице 2.1.
Таблица 2.1 – Показатели качества твёрдого остатка
| Параметр | Твердый остаток |
| Массовая доля углерода,% | 83,8 |
| Зольность,% | 16,2 |
| Массовая доля серы,% | 2,31 |
| Массовая доля водорода,% | 0,88 |
| Выход летучих веществ,% | 2,3 |
| Массовая доля влаги,% | 1,13 |
Результаты выполненного анализа свидетельствуют о том, что по основному показателю – содержание углерода 83,8 %, твёрдый остаток возможно использовать в качестве сорбента.
3. Общая характеристика процессов адсорбции
В настоящее время нет общей теории, которая достаточно корректно описывала бы все виды адсорбции на различных адсорбентах и разных поверхностях раздела фаз. Поэтому рассматривают наиболее распространенные теории, которые (несмотря на большое число допущений) позволяют на качественном уровне получить представление о таком сложном процессе, как адсорбция. Это Теория молекулярной адсорбции Ленгмюра, Теория полимолекулярной адсорбции и Обобщенная теория Брунауэла, Эммета и Теллера. Взаимодействие молекул компонентов раствора с атомами или молекулами поверхности твердого тела приводит к тому, что молекулы этих компонентов удерживаются в течение некоторого времени на границе раздела фаз. Чем больше энергия взаимодействия молекул вещества с поверхностью адсорбента, тем больше времени молекула находится на поверхности раздела фаз, т.е. существует в адсорбированном состоянии. Виды изотермы адсорбции представлены на рисунке 4.1.
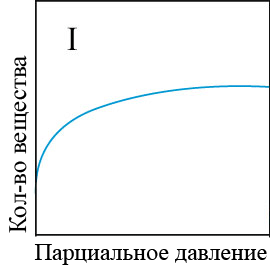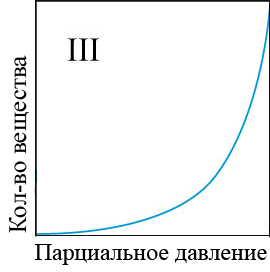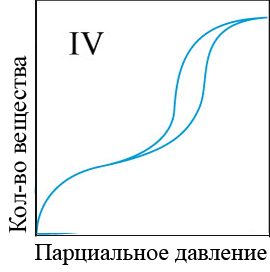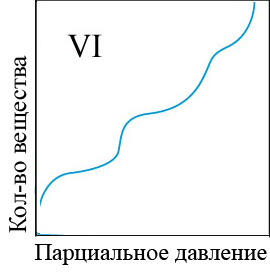
Рисунок 4.1 – Виды изотерм адсорбции
В большинстве случаев равновесие между молекулами в газовой фазе или растворе и молекулами, связанными поверхностью адсорбента, в условиях постоянства температуры выражается уравнением изотермы адсорбции, предложенным Ленгмюром [5] :
Г = Г∞(ВС/(1+ВС)), (3.1)
где Г - количество вещества, адсорбированного 1 м2 поверхности (или 1 г) адсорбента (удельная адсорбция вещества) , г/м2 или г/г ;
Г∞- количество вещества, адсорбированного 1 м2 поверхности (или 1г) адсорбента при максимальном ее заполнении , г/ м2 или г/г ;
С - равновесная концентрация вещества в газовой фазе или растворе;
В - постоянная величина, зависящая от строения молекул.
При адсорбции из водных растворов уравнение Ленгмюра наиболее пригодно в тех случаях, когда адсорбируются большие молекулы, например, молекулы гумусовых веществ, обусловливающие окраску природных вод. При адсорбции меньших молекул, обычно даже при больших равновесных концентрациях, удельная адсорбция не достигает предела, а постепенно, хотя и медленно, продолжает изменяться. При этом условия адсорбционного равновесия хорошо выражаются эмпирическим уравнением Фрейндлиха (уравнение параболы) [6]:
Г = αС1/k, (3.2)
где α и 1/k - константы, определяющие кривизну параболы.
При равновесной концентрации, равной единице, величина удельной адсорбции Г становится равной константе α. Чем больше α, тем больше удельная адсорбция вещества. Следовательно, величина ? может быть условной мерой активности адсорбента при небольших концентрациях поглощаемых из раствора веществ. Для определения адсорбционных констант α, k строят адсорбционные кривые в явных и логарифмических координатах и выполняют соответствующие расчёты [7].
4 Методики экспериментальных исследований и полученные результаты
Для подтверждения возможности использования твёрдого остатка в качестве сорбента, были проведены его испытания по стандартным методикам [8]. Согласно [8] определили адсорбционную активность относительно метиленового синего, метилового оранжевого и метилового красного.
Для этого навеску угля массой 0,1000 г помещали в коническую колбу ёмкостью 200 см3, добавляли 25 см3 раствора красителя, закрывали крышкой и взбалтывали на протяжении 20 мин. После этого определяли оптическую плотность на фотоэлектроколориметре с синим светофильтром и длиной волны 400 нм в кюветах, с расстоянием между рабочими гранями 10 мм.
В качестве контрольного раствора использовали дистиллированную воду. По полученным оптическим плотностям на основании градуировочного графика определяли остаточную концентрацию красителя.
Адсорбционную активность рассчитывали по формуле:
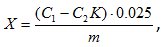
где С1 – концентрация исходного раствора красителя, мг/дм3;
С2 – концентрация раствора красителя после контакта с активированным углем, мг/дм3;
К – коэффициент разбавления;
m – масса навески активного угля, г;
0,025 – объём раствора красителя, участвующий в исследовании, дм3.
Исследование проводили в статических условиях – сорбент помещали в замкнутую систему. Результаты исследования адсорбционной ёмкости приведены в таблицах 4.1-4.3.
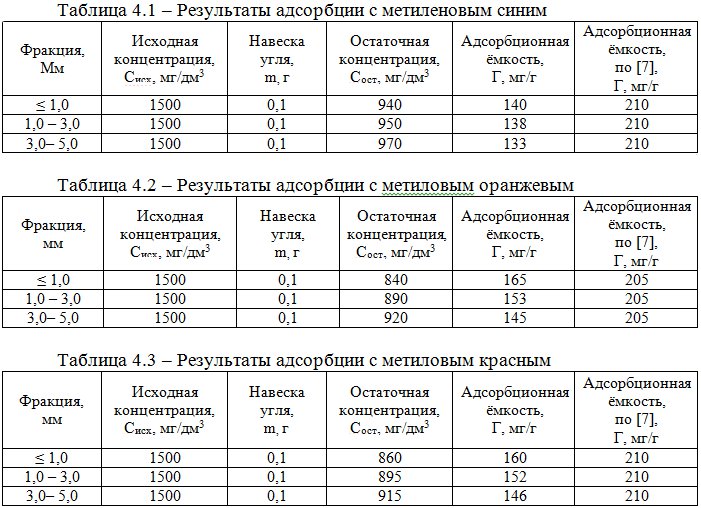
Как следует из данных таблиц 4.1-4.3, величина адсорбционной ёмкости твёрдого остатка пиролиза автошин составляет 60-80 % от величины адсорбционной ёмкости активированных углей, заданной стандартом [8].
Для определения вида изотерм адсорбции были проведены исследования сорбционных свойств твёрдого остатка и определены константы в уравнении Фрейндлиха. Для этого выполнили серию опытов, в которых варьировали исходные концентрации красителей в диапазонах, приведённых в таблицах 4.4-4.6. Значения величин сорбционной ёмкости рассчитывали по формуле (3.2), без учёта коэффициента разбавления и объём анализируемого раствора составил 50 см3.
Полученные результаты представлены в таблицах 4.4-4.6.
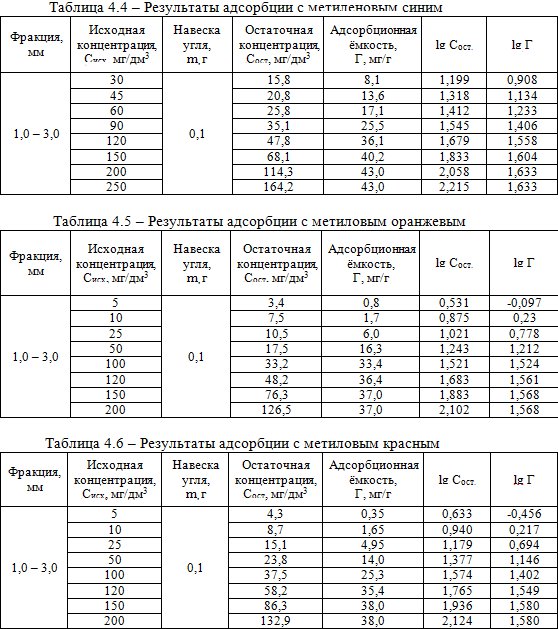
По полученным данным построили адсорбционные кривые в натуральных и логарифмических координатах (рис. 4.2 – 4.4).
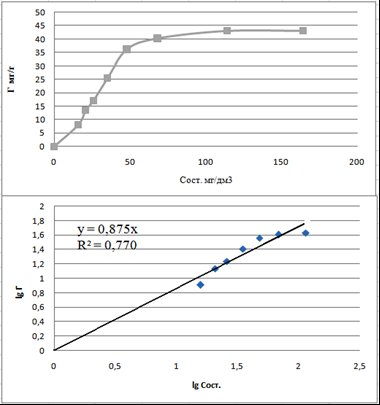
Рисунок 4.2 – Адсорбционные кривые относительно метиленового синего
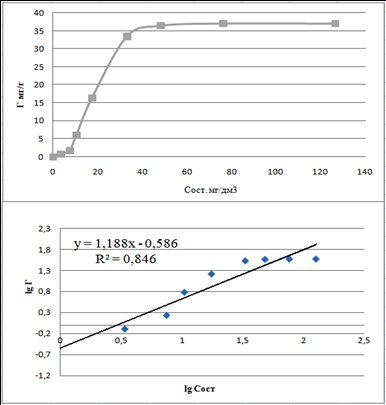
Рисунок 4.3 – Адсорбционные кривые относительно метилового оранжевого
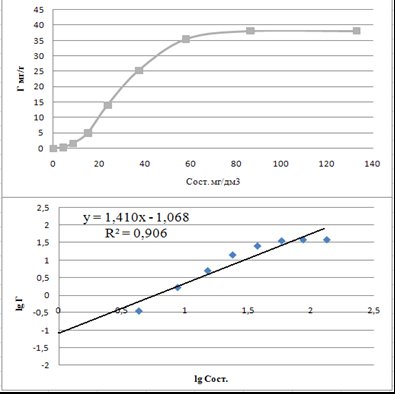
Рисунок 4.4 – Адсорбционные кривые относительно метилового красного
В результате выполненных расчётов на основании данных рис. 4.2-4.4 были определены адсорбционные константы и полученные следующин уравнения:
а) для метиленового синего – Г = 1,000 С0,466;
б) для метилового оранжевого – Г = 0,282 С0,424;
в) для метилового красного – Г = 0,089 С0,364.
Полученные коэффициенты в уравнениях свидетельствуют о достаточных сорбционных свойствах твёрдого остатка [9].
Важной характеристикой углесодержащих сорбентов является сорбционная ёмкость по йоду, которая согласно [10] должна составлять для углей марки ОУ – 30 %, для БАУ – 60 %.
Для определения сорбционной ёмкости взяли навеску твёрдого остатка массой 1,0000 г после высушивания в сушильном шкафу до постоянной массы, помещали в коническую колбу емкостью 250 см3. Добавляли туда 100 см3 0,1 н раствора йода в йодном калии, закрывали пробками и взбалтывали на аппарате для встряхивания жидкости в течение 15 мин. Потом раствору давали отстояться, осторожно отбирали 10 см3 раствора в коническую колбу емкостью 50 см3 и титровали 0,1 н раствором тиосульфата натрия в присутствии крахмала. Одновременно проводили определение исходного содержимого йода в растворе.
Обработку результатов проводили по формуле:
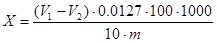
где V1 – объём раствора тиосульфата натрия (0,1 н), который пошёл на титрование 10 см3 раствора йода в йодистом калии, см3;
V2 – объём раствора тиосульфата натрия (0,1 н), который пошёл на титрование 10 см3 раствора йода в йодистом калии, после обработки его углём, см3;
0,0127 – масса йода, которая соответствует 1 см3 раствора тиосульфата натрия, г;
100 – объём раствора йода в йодистом калии, который брали на осветление углём, см3;
m – масса навески угля, 1,0000 г.
Адсорбционная активность исследуемого остатка по йоду составила 73 %, что соответствует адсорбционной активности угля марки БАУ-МФ, и не ниже аналогичной величины для отдельных марок АУ.
Выводы
В технологии водоочистки наряду с известными сорбентами, такими как активированный уголь, силикагель, можно использовать сорбенты, полученные из отходов производств. Одним из таких отходов является твёрдый остаток пиролиза изношенных автомобильных шин, который по своим характеристикам и свойствам не уступает активированным углям марки ОУ-А(Б,В,Г), БАУ и других АУ.
В ходе экспериментального исследования были получены данные, на основе которых можно говорить о целесообразности использования продукта пиролиза для очистки сточных вод от органических загрязнителей.
В дальнейшем планируется исследование сорбционных свойств твёрдого вещества в динамических условиях, а именно извлечение из сточных вод органических загрязнителей и ионов тяжёлых металлов. Будут проведены исследования возможности очистки сточных вод коксохимического завода на модельной установке.
Список использованной литературы
- Электронная статья. Активированный уголь, очистка воды и воздуха [Электронный ресурс]: http://www.activcarbon.com.ua
- Шендрик, Т.Г. Утилизация нефтяных отходов с получением активированных углей / Т.Г. Шендрик, Л.В. Пащенко, В.А. Кучеренко. В.В. Симонов // Углехимический журнал. – 2005. № 5. – с. 27-31.
- Миллер Р. Теория переключательных схем / Р. Миллер. – М.: Наука, 1971. – Том 2: Последовательностные схемы и машины. – 304 с.
- Электронная статья. Утилизация шин и экология [Электронный ресурс]: http://www.utilrti.ru
- Булавин А.В., Пашкевич В.Н. Переработка отработанных автомобильных шин методом низкотемпераьурного пиролиза. / Научные труды Донецкого национального технического университета. // Химия и химическая технология. Выпуск 95. – Д:Лебедь, 2005. – с. 98 – 102.
- Когановский А.М. Адсорбция и ионный обмен в процессах водоподготовки и очистки сточных вод. / А.М. Когановский. – К.: Наукова думка, 1983. – 240 с.
- Смирнов А.Д. Сорбционная очистка воды./ А.Д. Смирнов. – Л.: Химия, 1982. – 168 с.
- Адсорбционная технология очистки сточных вод / А.М. Когановский, Т.М. Левченко, И.Г. Рода. – К.: Техніка, 1981. – 176 с.
- ГОСТ 4453 – 74. Уголь активный осветляющий древесный порошкообразный. М.: Государственный комитет стандартов, 1974. –11 с.
- Цыбульская К.В., Трошина Е.А. Изучение возможности использования твёрдого продукта пиролиза автомобильных шин. / Сборник докладов Международной научно-практической конференции молодых ученых и студентов «Современные экологически безопасные и энергосберегающих технологи в природопользовании» . – ч. 2. – К: КНУБА, 2011. – с. 53 – 55.
- ГОСТ 6217 – 74. Уголь активный древесный дробленый. – М.: Государственный комитет стандартов, 1974. – 6 с.


