Аннотация
Пупкова В.И. В данной брошюре приводятся основные сведения по строению, свойствам и методам определения гемоглобина. В работе рассматриваются наиболее используемые колориметрические методы – гемиглобинцианидный и гемихромный. Несмотря на кажущуюся простоту анализа, правильность определения гемоглобина невелика, поэтому подробно изложены методики и способы проведения анализа, позволяющие избежать различных погрешностей и получать правильные результаты; указаны источники возможных погрешностей.
ОСНОВНЫЕ ФУНКЦИИ. СТРОЕНИЕ. СВОЙСТВА
Гемоглобин – основной дыхательный пигмент и главный компонент эритроцита, выполняющий важные функции в организме человека: перенос кислорода из легких в ткани и углекислого газа из тканей в легкие. Он также играет существенную роль в поддержании кислотно-основного равновесия крови. Буферная система, создаваемая гемоглобином, способствует сохранению рН крови в определенных пределах.
Гемоглобин – красный пигмент крови человека и животных. Подсчитано, что в одном эритроците содержится около ~ 340000000 молекул гемоглобина, каждая из которых состоит примерно из 103 атомов. В крови человека в среднем содержится ~ 14,5% гемоглобина, его общее количество ~ 750 г. Гемоглобин представляет собой сложный белок, относящийся к группе гемопротеинов; белковый компонент в котором представлен глобином, небелковый – простетической группой. Простетическая группа в молекуле гемоглобина представлена 4 одинаковыми железопорфириновыми соединениями, которые называются гемами. Молекула гема состоит из порфирина IХ, связанного с железом двумя атомами азота ковалентными и двумя другими атомами азота координационными связями. Атом железа (II) расположен в центре гема и придает крови характерный красный цвет, степень его окисления не изменяется независимо от присоединения или отдачи кислорода.
Видовые различия гемоглобина обусловлены химическим составом и строением глобина. Гемоглобины представляют собой тетрамерные белки, молекулы которых образованы различными типами полипептидных цепей, обозначаемых как α ,β, γ, δ. В состав молекулы входят по 2 полипептидные цепи двух разных типов, каждая из которых оборачивает 1 гем гемоглобина. Гемоглобины различных видов различаются вторичной, третичной и четвертичной структурами, и индивидуальные свойства гемоглобинов неразрывно связаны с их структурами. Известно, что гемоглобин человека состоит из двух равных половин, каждая из которых образована двумя одинаковыми полипептидными цепями. У человека обнаружены гемоглобины различных типов, которые отличаются по химическому строению. В крови взрослого человека содержится гемоглобин А (HbA), состоящий из α2β2 цепей. В дополнение к основному HbA в крови взрослого человека обнаружен гемоглобин A2 (HbA2), на долю которого приходится ~ 2,5% от всего гемоглобина. Кроме того, известен фетальный гемоглобин F (HbF) – гемоглобин новорожденных, имеющий структуру α2γ2, и отличающийся от HbA вторичной, третичной и четвертичной структурами, что обусловливает их различия: по спектральным характеристикам, электрофоретической подвижности, устойчивости к тепловой денатурации и др. Кровь новорожденного ребенка состоит на ~ 80% из HbF, который к концу первого года жизни почти целиком заменяется на HbA (в крови взрослого человека содержится до ~ 1,5% HbF от общего количества гемоглобина).
Гемоглобин – кристаллическое вещество, хорошо растворимое в воде и нерастворимое в спирте, эфире и хлороформе. В эритроцитах гемоглобин находится в растворенном состоянии, несмотря на то, что его содержание более 30%. При изменении аминокислотного состава глобина может произойти и изменение его растворимости, как у HbS.
Растворы гемоглобина окрашены в темно-красный цвет и имеют характерные спектры поглощения в ультрафиолетовой и видимой областях спектра. Изоэлектрическая точка гемоглобина ~ 7. В кислой и щелочной среде гемоглобин легко денатурируется, скорость денатурации различна у различных видов гемоглобинов. В кислой среде связь между гемом и глобином легко разрывается. Свободный гем легко окисляется кислородом воздуха до гематина, в котором атом железа трехвалентен.
Наиболее характерным свойством гемоглобина является обратимое присоединение газов О2, СО и др. Образовавшиеся при этом соединения называются оксигемоглобином и карбоксигемоглобином, соответственно. Реакция присоединения молекулярного кислорода не является истинным окислением гемоглобина, так как валентность железа в гене при этом не изменяется, и эту реакцию правильнее называть оксигенацией. Истинное окисление гемоглобина происходит только тогда, когда железо переходит в трехвалентное состояние.
В крови гемоглобин существует по крайней мере в четырех формах: оксигемоглобин, дезоксигемоглобин, карбоксигемоглобин, метгемоглобин. В эритроцитах молекулярные формы гемоглобина способны к взаимопревращению, их соотношение определено индивидуальными особенностями организма.
Клиническое значение
Снижение концентрации гемоглобина: анемии.
Повышение концентрации гемоглобина: полицитемия, гемоконцентрация при дегитратации, ожогах, кишечной непроходимости, упорной рвоте; пребывание на больших высотах, чрезмерная физическая нагрузка или возбуждение; сердечно-сосудистая патология, обычно врожденная, приводящая к значительному венозному сбросу; заболевания легких, приводящие к снижению легочной перфузии, плохой аэрации легких, легочной артериальной фистуле; хроническое химическое воздействие нитритов, сульфонамидов, вызывающих образование мет- и сульфогемоглобина.
Нормальные величины: у мужчин 130-160 г/л; у женщин; 120-140 г/л.
Содержание гемоглобина обычно ниже у недоношенных, чем у доношенных новорожденных. Содержание гемоглобина снижается на ~ 10% в промежутке времени от 17 до 07 час утра, а также после еды. Снижение гемоглобина от нормальных величин на ~ 6% наблюдается при взятии пробы в положении лежа. Незначительное, но диагностически значимое, снижение нижнего порога нормальных величин гемоглобина встречается у мужчин возрастной группы 65-74 года.
МЕТОДЫ АНАЛИЗА
Общая характеристика методов
Определение содержания гемоглобина в крови человека является одним из самых важных и массовых показателей. Для определения гемоглобина чаще всего анализируют производные гемоглобина, образовавшиеся в процессе его окисления и присоединения к гему различных химических групп, приводящих к изменению валентности железа и окраски раствора.
Из «старых» методов, все еще применяемых в ряде лабораторий, остановимся на следующих: сапониновом и методе Сали.
При использовании сапонинового метода тельца Гейнца не растворяются, раствор остается мутноватым, за счет чего может меняться спектр поглощения раствора, и ошибка при этом достигает 20-30%.
В методе Сали измеряется гематин, образовавшийся при взаимодействии гемоглобина с соляной кислотой. Метод основан на визуальной оценке содержания гемоглобина путем сравнения окраски исследуемой пробы со стандартными растворами солянокислого гематина. Ошибка метода достигает ~ 30%, на результаты определения влияют многие факторы: время реакции между гемоглобином и соляной кислотой, которое может колебаться от 2 до 40 мин в зависимости от содержания белков крови; оттенок цвета геминхлорида, зависящий от содержания билирубина в крови; характера освещения и пр.
Химические и спектрофотометрические методы имеют высокую точность и рекомендуются в качестве референсных, но из-за трудоемкости и значительной стоимости анализа для рутинных определений не применяются.
Для рутинных лабораторных исследований наиболее предпочтительны колориметрические методы, как наиболее дешевые, простые и быстрые в исполнении. Кровь человека – это нормальная смесь производных гемоглобина с различными спектрами поглощения. При количественном определении гемоглобина колориметрическими методами возникает проблема в выборе реагента, который превращал бы все производные гемоглобина только в одну форму перед фотометрическим анализом. Лучшими методами, количественно превращающими гемоглобин в его производные, оказались гемиглобинцианидный (HbCN), гемихромный (HbChr) и гемиглобиназидный (HbN3), которые при фотометрировании дают наименьшую ошибку определения среди других методов анализа. Однако, некоторые данные не позволяют использовать гемиглобиназидный метод в качестве альтернативного в силу следующих причин: конечный продукт превращения гемоглобина – HbN3 имеет слабый пик поглощения при λ = 540 нм, что не дает возможности использовать фотометры с широкополосными фильтрами; иногда возникают проблемы, связанные с мутностью растворов; и наконец, раствор HbN3 не хранится при комнатной температуре. Напротив, гемиглобинцианидный и гемихромный методы лишены этих недостатков и при дальнейших исследованиях им было отдано предпочтение.
Интерференция при всех колориметрических методах анализа
Повышение гемоглобина: гипертриглицеридемия, количество лейкоцитов более 25х109 /л, прогрессирующие заболевания печени, наличие легко преципитирующихся глобулинов (при миеломной болезни или при макроглобулинемии Вальденстрема).
Понижение гемоглобина: у заядлых курильщиков вследствие образования неактивного HbСО.
Гемиглобинцианидный метод
Принцин гемиглобинцианидного метода основан на переводе всех форм гемоглобина в одну - гемиглобинцианид. Перевод гемоглобина в гемиглобинцианид осуществляется при его взаимодействии с трансформирующим раствором, содержащим феррицианид калия, цианид калия, дигидрофосфат калия и неионный детергент. Дигидрофосфат калия поддерживает уровень рН, при котором реакция проходит за 3-5 минут. Детергент усиливает гемолиз эритроцитов и предотвращает мутность, связанную с белками плазмы. Феррицианид калия окисляет все формы гемоглобина в метгемоглобин, который образует с цианистым калием гемиглобинцианид, имеющий красноватый цвет, интенсивность окраски которого прямо пропорциональна концентрации гемоглобина в пробе.
Характеристика метода
Гемиглобинцианидный метод, разработанный в 1936 г Драбкиным, был одобрен Международным Комитетом по стандартизации в гематологии (ICSH) в 1963 г.
Экспериментальное изучение данного метода для его стандартизации в гемиглобинометрии имело следующие главные цели: найти точное значение коэффициента молярной экстинкции для HbCN при λ = 540 нм; разработать требования для получения калибровочного раствора HbCN, обеспечивающие его стабильность в течение нескольких лет; усовершенствовать процедуру анализа при определении гемоглобина для снижения экспериментальных ошибок; оценить надежность других методов в сравнении с гемиглобинцианидным. На основе широкомасштабных исследований был определен коэффициент молярной экстинкции гемиглобинцианида, равный 11,00 (ε540 = 11,00), и выработаны требования к его качеству.
Основные достоинства гемиглобинцианидного метода:
- HbCN является стабильным производным гемоглобина, и все имеющиеся в крови формы гемоглобина могут быть быстро и количественно превращены в HbCN;
- спектр поглощения HbCN имеет плоский максимум при λ = 540 нм, поэтому достаточная точность анализа возможна при измерении оптической плотности на фотометрах даже со светофильтрами;
- растворы HbCN строго подчинены закону Ламберта-Бера при λ = 540 в широком диапазоне концентраций;
- калибровочный раствор HbCN устойчив в течение нескольких месяцев и даже лет.
Гемихромный метод
С развитием методов анализа для определения гемоглобина в крови разработан новый колориметрический метод, не содержащий в составе реагентов цианистых соединений, которые заменены жирными кислотами с феррицианидом калия или поверхностноактивными веществами, лучший из которых – додецилсульфат натрия (SDS).
Принцип гемихромного метода
Принцип гемихромного метода основан на переводе всех форм гемоглобина в одну – гемихром. При взаимодействии гемоглобина с трансформирующим раствором, содержащим жирные кислоты с феррицианидом калия или додецилсульфат натрия, происходит его превращение в окисленную низкоспиновую форму – гемихром (HbChr), имеющую красноватый цвет, интенсивность окраски которого прямо пропорциональна концентрации гемоглобина в пробе.
Характеристика метода
Гемихромный метод определения гемоглобина в крови разработан Ахрем А.А. с соавторами в 1986 г. Набор реагентов для определения гемоглобина в крови, основанный на данном методе, одобрен Комитетом по новой медицинской технике МЗ РФ и рекомендован к применению в клинико-диагностических лабораториях уже в 1998 г.
Основные достоинства гемихромного метода:
- гемихром – стабильное производное гемоглобина, и все имеющиеся в крови формы гемоглобина могут быть быстро и количественно превращены в HbChr;
- спектр поглощения HbChr имеет плоский максимум вблизи λ = 540 нм (533), поэтому достаточная точность анализа возможна при измерении оптической плотности на фотометрах даже со светофильтрами;
- растворы HbChr строго подчинены закону Ламберта-Бера при λ = 540 нм в широком диапазоне концентраций;
- калибровочный раствор HbChr устойчив в течение нескольких месяцев и даже лет;
- трансформирующий реагент не ядовит и безвреден: в его составе не содержится цианистых соединений.
Молярный коэффициент экстинкции HbChr при λ = 540 нм равен ~ 10,14 (ε540 ~ 10,14).
Сравнение гемихромного и гемиглобинцианидного методов
При широкомасштабных испытаниях гемихромного метода было показано, что в интервале концентраций гемоглобина от 40 до 200 г/л калибровочные графики гемиглобинцианида и гемихрома представляют прямую линию, выходящую из начала координат, а близкие углы наклона прямых указывают на сопоставимость обоих методов.
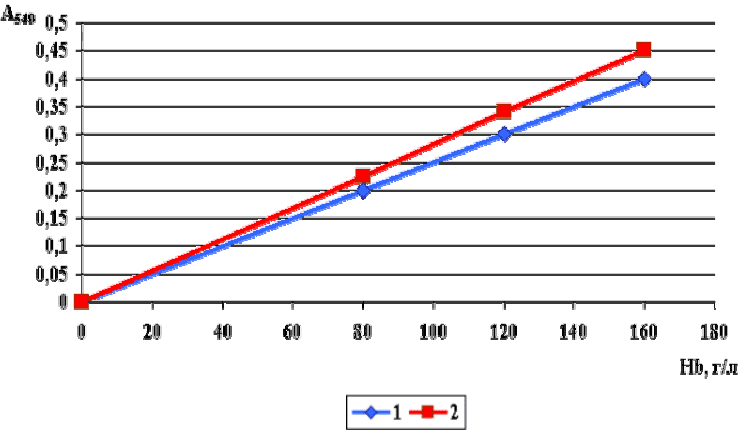
Рисунок 1 – Величина оптической плотности гемихрома (1) и гемиглобинцианида (2)
При определении гемоглобина двумя методами Ахрем А.А. с соавторами показали, что большую точность (и меньшую s) дает гемихромный метод. Авторы предполагают, что SDS способствует солюбилизации мембранных частиц и препятствует адсорбции белка на стекле пробирок и кювет, тем самым обеспечивается высокая точность анализа.
Сравнительная оценка результатов определения гемоглобина в крови двумя методами показала, что результаты сопоставимы, а коэффициент корреляции методов составляет 0,99.
Таким образом, гемихромный метод определения гемоглобина в крови обладает всеми достоинствами гемиглобинцианидного метода, которые дополняются отсутствием в составе трансформирующего реагента высокотоксичных цианидов и других ядовитых веществ.