Реферат по теме выпускной работы
Содержание
- Введение
- 1. Актуальность темы
- 2. Цель и задачи исследования
- 3. Основная часть
- 3.1. Теория адсорбции
- 3.2. Типы адсорбентов
- 3.3. Способы получения адсорбентов
- 3.4. Строение и свойства адсорбентов
- 4. Влияние солей на окрашенность растворов
- Выводы
- Список источников
Введение
В любой отрасли промышленности используются процессы сорбции веществ.
Адсорбенты – высокодисперсные природные или искусственные материалы с большой удельной поверхностью, на которой происходит адсорбция веществ из соприкасающихся с ней газов или жидкостей. Адсорбенты применяют для очистки воды от металлов и примесей, в противогазах, в качестве носителей катализаторов, в медицине для поглощения газов и ядов.
Также адсорбенты применяются как наполнители для полимеров, для хроматографического разделения смесей в хроматографии, в нефтепереработке (риформинг, гидроочистка, гидрокрекинг), нефтехимии для очистки нефтепродуктов (нефти, бензина и т. д.) и газов, адсорбционной очистки масел, прежде всего трансформаторных, от кислот – продуктов окисления масел, как статические осушители при консервации приборов и оборудования, а также в высоковакуумной технике для сорбционных насосов.
Адсорбционные свойства адсорбентов зависят от химического состава и физического состояния поверхности, от характера пористости и удельной поверхности (поверхности, приходящейся на 1 г вещества). Непористые адсорбенты (молотые кристаллы, мелкокристаллические осадки, частицы дымов, сажи, аэросил) имеют удельные поверхности от 1 м2/г до 500 м2/г. Удельная поверхность пористых адсорбентов (силикагелей, активированного оксида (окиси) алюминия (алюмогелей), алюмосиликатных катализаторов, активированных углей) достигает 1000 м2/г. Пористые адсорбенты получают, создавая сети пор в грубодисперсных твёрдых телах химическим воздействием.
Самыми распространенными адсорбентам являются активные (активированные) угли, которые получаются путем термической деструкции веществ, содержащих углерод. Наиболее часто, в качестве сырья используется береза. Березовые активные угли (БАУ) можно применять для процессов сорбции в пищевой промышленности и медицине – это говорит о высоком качестве данных адсорбентов. Но следует помнить, что береза – долго восстанавливаемый источник сырья, не говоря уже об ухудшении экологического состояния регионов, где производится массовая вырубка этих деревьев.
1. Актуальность темы
В качестве адсорбентов могут выступать разнообразные материалы с высокой удельной поверхностью: пористый углерод (наиболее распространённая форма – активированный уголь), силикагели, цеолиты, а также некоторые другие группы природных минералов и синтетических веществ. Высококачественные адсорбенты получают пиролизом малосмолистых пород деревьев, например березы, что, безусловно, не приемлемо как с социальной, так и с экологической точек зрения. Поэтому в настоящее время активно разрабатываются способы получения активных углей из альтернативного сырья.
2. Цель и задачи исследования
Основной целью данной работой является разработка способа получения новых адсорбентов из быстро возобновляемого растительного сырья, а также углеродсодержащих отходов пищевых производств.
Основные задачи исследования:
- Рассмотреть возможность получения адсорбентов из нетрадиционного вида сырья.
- Получить образцы адсорбентов из растительного сырья.
- Изучить влияние солей на процесс получения активированных углей.
- Сделать вывод о возможности применения полученных образцов вместо традиционных активированных углей.
3. Основная часть
Адсорбция – процесс самопроизвольного перераспределения компонентов системы между поверхностным слоем и объемной фазой.
3.1. Теория адсорбции
Адсорбция представляет собой механизм закрепления веществ, находящихся в молекулярной или ионной форме, на поверхности материалов с определенными свойствами. Этот процесс сопровождается, как правило, переносом вещества, находящегося в состоянии истинного или коллоидного раствора на твердофазную поверхность. Адсорбционные свойства таких твердых тел определяются, прежде всего, их удельной поверхностью, измеряемой в квадратных метрах на грамм адсорбирующего вещества.
Адсорбция заключается в улавливании поверхностью микропористого адсорбента (активированный уголь, силикагель, цеолиты) молекул вредных веществ. Одним из лучших адсорбентов является активированный уголь, у которого в 1 г содержится до 1600 м2 поверхностей.
Кроме общей площади поверхности адсорбента, уровень адсорбции определяется так же и характером связи адсорбента и адсорбируемого вещества. То есть, свободной энергией взаимодействия адсорбционным центром сорбирующего материала и часть молекулы, вступающей с ним во взаимодействие [1].
Преимущественно на величину адсорбции влияют силы Ван-дер-Ваальса [2], а также силы электростатического притяжения.
Механизм протекания процесса физической адсорбции по модели Ван-дер-Ваальса объясняется ориентационным, индукционным и дисперсионным эффектами. Ориентационный эффект заключается в следующем. Незаряженные молекулы могут иметь дипольный момент, характерной чертой которого является несовпадение центров тяжести положительных и отрицательных зарядов (дипольный момент зависит от самого заряда и расстояния между центрами тяжести). Взаимодействие молекул с дипольными моментами происходит по типу притяжения в случае, если разноименные заряды ближе друг к другу, чем одноименные.
Имеет значение и сродство между молекулами, например, ароматическими углеводородами и углеродом, имеющим структуру графита, у которого возникают силы отталкивания с органическими соединениями иного строения. Так же имеет значение и время контакта между адсорбирующим веществом и осаждаемыми на нем загрязнениями сточной воды, определяющее степень достижения ими поверхности адсорбента. Масса адсорбированного вещества, приходящаяся на единицу поверхности сорбента, определяется его концентрацией в водной среде. В равновесном состоянии молекулы, адсорбированные на поверхности, постоянно меняются местами, что в определенном приближении описывается законом Фрейндлиха [3].
Экспериментальные изотермы адсорбции являются наиболее распространенным способом описания адсорбционных явлений. Методы получения адсорбционных данных для построения изотерм адсорбции основаны на измерении количества газа (жидкости), удаленного из газовой (жидкой) фазы при адсорбции, а также на различных способах определения количества адсорбата (адсорбированное вещество) на поверхности адсорбента (адсорбирующее вещество), например, волюметрический метод, гравиметрический метод и др.
Различают шесть (пять) основных типов изотерм адсорбции (рис. 1). Тип I характерен для микропористых твёрдых тел с относительно малой долей внешней поверхности. Тип II указывает на полимолекулярную адсорбцию на непористых или макропористых адсорбентах. Тип III характерен для непористых сорбентов с малой энергией взаимодействия адсорбент-адсорбат. Типы IV и V аналогичны типам II и III, но для пористых адсорбентов. Изотермы типа VI характерны для непористых адсорбентов с однородной поверхностью [4].
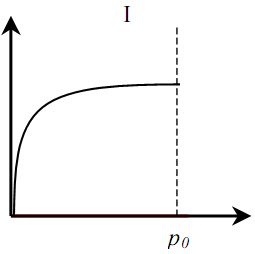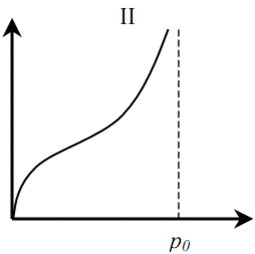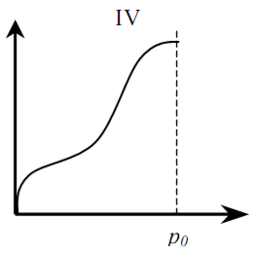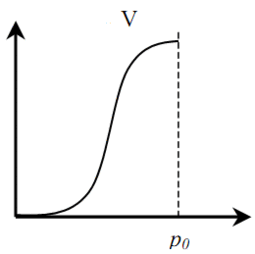
Рисунок 1 – Типы изотерм адсорбции
Изотермы адсорбции используются для расчета удельной поверхности материалов, среднего размера пор или среднего размера нанесённых частиц, распределения пор или частиц по размерам.
3.2. Типы адсорбентов
Рассматривая влияние полярности на увеличение энергии взаимодействия, Киселев и соавторы разделили адсорбцию на специфическую и неспецифическую. В первом случае адсорбция обусловлена лишь соотношением дисперсионных сил и сил отталкивания, а во втором – еще и действием кулоновских сил.
Киселев разделил адсорбенты на три класса [5] в соответствии со следующими признаками:
1-й класс – на поверхности не содержится никаких ионов или положительно заряженных групп, например, графитовая сажа.
2-й класс – на поверхности имеются сосредоточенные положительные заряды, например, группы ОН на гидроксилированных оксидах.
3-й класс – на поверхности имеются сосредоточенные отрицательные заряды, например, =О, =СО.
Адсорбаты же были разделены на четыре группы. Молекулы адсорбатов, входящие в эти группы имеют:
– сферически симметричные оболочки или сигма-связи, например, благородные газы, насыщенные углеводороды;
– пи-связи, например, ненасыщенные или ароматические углеводороды, или свободные пары электронов, например, эфиры, третичные амины;
– положительные заряды, сосредоточенные на периферии молекул;
– функциональные группы с электронной плотностью или положительными зарядами, сосредоточенными на периферии, например, молекулы с группами ОН или =NH.
Кроме химической структуры следует учитывать и особенности внутренней геометрической структуры адсорбентов. С этой точки зрения адсорбенты делятся на две группы [5]:
1-я группа – непористые адсорбенты;
2-я группа – пористые адсорбенты, подразделяющиеся на однородно пористые и неоднородно пористые.
На практике методы адсорбции обычно используются для определения удельной поверхности и пористой структуры лишь высокодисперсных твердых тел или систем с развитой пористостью.
Удельная поверхность твердого тела данной конкретной массы обратно пропорциональна размеру составляющих частиц. В идеальном случае, когда частицы имеют форму куба одинакового размера.
Обычно частицы высокодисперсного порошка – первичные частицы – под действием поверхностных сил слипаются в более или менее плотные вторичные частицы. Если контакты между соседними частицами слабые, эти укрупнения, называемые агрегатами, могут разрушаться. При повышенных температурах или под прессованием под давлением первичные частицы соединяются в более прочные вторичные частицы – так называемые агломераты [6].
Промежутки между первичными частицами внутри вторичных частиц и промежутки между вторичными частицами образуют пористую структуру (систему), в которой форма и размер индивидуальных пор зависит от формы и размеров первичных и вторичных частиц. Хотя в принципе первичные частицы могут иметь любую форму, чаще всего встречаются глобулы и пластинки.
Пористые адсорбенты отличаются от непористых наличием системы пор, имеющих характерную структуру. Форма и ширина пор могут быть самыми разными: это могут быть и микроскопические углубления, и бороздки глубиной порядка 1 мкм, и пустоты, диаметр которых близок к диаметру молекулы адсорбируемого соединения.
Размеры отверстий пор влияют на массообмен, т.е. на скорость переноса вещества к внутренней поверхности, на которой происходят процессы адсорбции и десорбции, наиболее важные для осуществления процесса газохроматографического разделения.
В узких порах адсорбированные молекулы одновременно взаимодействуют с адсорбционными центрами, расположенными на противоположных стенках пор.
Такой подход приводит к делению пористых адсорбентов на три группы [7]:
– микропористые адсорбенты;
– мезопористые адсорбенты;
– макропористые адсорбенты.
Адсорбционные свойства зависят от интервала размеров пор – каждому размеру соответствуют определенные характеристики. В микропорах потенциал взаимодействия с адсорбированными молекулами значительно больше, чем в более широких порах, таких как у мезо- и макропор – это обусловлено близостью стенок пор. Величина адсорбции при данном конкретном относительном давлении соответственно также больше. Капиллярная конденсация происходит в порах среднего размера – в мезопорах. К сожалению, не всегда можно изучить изотерму адсорбции – макропоры для этого слишком широки.
Граница между различными классами не является жестко определенной, поскольку она зависит и от формы пор, и от природы молекул адсорбтива. Так, наибольший размер пор при котором еще наблюдается увеличение адсорбции, т.е. верхний предел размеров микропор, у различных адсорбтивов может быть различным [8].
Скорость массообмена также сильно зависит от размера пор: для того чтоб он проходил достаточно быстро, адсорбент должен быть преимущественно макропористым. Но, следует учитывать, что большая удельная поверхность обуславливает высокий коэффициент емкости, следовательно, и критерий разделения. В этой связи приходится искать оптимальные соотношения между желаемым временем анализа и степенью разделения.
3.3. Способы получения адсорбентов
Важнейшим сырьем для получения активных углей является древесина (в виде опилок), древесный уголь, торф, торфяной кокс, некоторые каменные и бурые угли, а также полукокс бурых углей.
Мелкоизмельченные древесные отходы, карбонизируют во вращающихся печах или аппаратах с движущимися слоями. Кусковые и гранулированные угли, а также прессованные изделия из древесноугольной пыли и связующего, активируются в шахтных и вращающихся печах водяным паром или диоксидом углерода при 800 °С. В процессе активации возрастают объем пор, удельная поверхность сорбента, меняется соотношение между объемами микро-, мезо- и макропор. Скорость газификации поверхностного углерода в процессе активации зависит от степени структурной упорядоченности углеродного материала. Наиболее легко и быстро газифицируется углерод в разупорядоченных областях углеродной поверхности. Приготовленные со связующим формованные угли необходимо термически обрабатывать перед активированием при температуре около 5000 °С, связующее в этих случаях частично карбонизуется. Качество активного угля зависит от свойств исходного углеродсодержащего материала и от режима активирования. Характеристикой степени активирования угля является обгар, то есть процент сгоревшего угля по отношению к исходному его количеству. Активные древесные угли отличаются высокой степенью чистоты и тонкопористостью [8].
Количество и размер образующихся пор определяются природой сырья и режимными параметрами процесса термической обработки. Важное значение имеет скорость нагрева сырья. Общий объем пор, а также количество крупных пор (макропор) значительно возрастают с ростом скорости нагрева сырья. Медленные скорости нагрева реализуются в технологиях пиролиза в реакторах с неподвижным слоем сырья. Более производительные технологии пиролиза основаны на использовании измельченного сырья и реакторов с так называемым псевдоожиженным или кипящим слоем: увлекаемые потоком газа мелкие частицы сырья как бы находятся в кипящем состоянии. Преимуществом реакторов с кипящим слоем является высокая скорость массо- и теплопереноса, что обеспечивает повышенную интенсивность процесса пиролиза по сравнению с технологиями пиролиза в неподвижном слое сырья. Объем пор и распределение пор по радиусам можно регулировать также путем изменения продолжительности процесса пиролиза. В реакторах с псевдоожиженным слоем продолжительность пребывания частиц измельченного сырья в зоне пиролиза составляет от десятых долей секунды до нескольких минут [9].
Также важным адсорбентом на сегодняшний день является силикагель. Это один из самых первых минеральных синтетических сорбентов, нашедших широкое применение в промышленности. Силикагель не потерял своего промышленного значения, несмотря на то, что в последние годы бурно развиваются адсорбционные процессы с использованием уникальных кристаллических сорбентов – цеолитов.
Технический силикагель получают следующим образом: путем взаимодействия раствора силиката натрия или калия (жидкое стекло) с соляной или серной кислотой получают гель, который высушивают, а затем разламывают на куски, промывают водой, снова сушат, измельчают, фракционируют и прокаливают до полного удаления влаги. Товарный силикагель выпускают в виде зёрен или шаровидных гранул [10].
Следует отметить, что современные подходы к изучению структурно-сорбционных свойств позволяет прогнозировать соответствие структуры пористых материалов задачам их применения и теоретически обосновать закономерности адсорбции различных веществ.
3.4. Строение и свойства адсорбентов
В настоящее время активный уголь относят к группе микрокристаллических разновидностей углерода. Хотя графитовые кристаллиты состоя из плоскостей протяженностью 2-3 нм, образованных шестичленными кольцами, типичная для графита ориентация отдельных плоскостей решетки относительно друг друга нарушена. Это означает, что в активных углях слои беспорядочно сдвинуты относительно друг друга и не совпадают в направлении, перпендикулярном плоскости слоев (рис. 2).
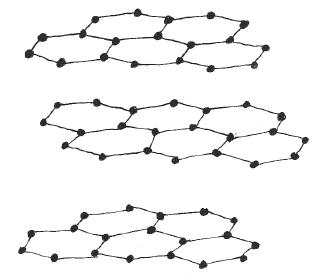
Рисунок 2 – Структура графитовых слоев
Кроме графитовых кристаллитов активные угли содержат по данным рентгеновского анализа от одной до двух третей аморфного углерода, наряду с этим присутствуют гетероатомы, в частности, кислород. Неоднородная масса, состоящая из кристаллитов графита и аморфного углерода, обуславливает необычную структуру активных углей. Между отдельными частицами появляются щели и трещины (поры). Между микро- и макропорами существуют мезопоры, являющиеся основными транспортными артериями, по которым осуществляется подвод сорбируемого вещества к емкостям – микропорам. Макропоры выполняют роль крупных транспортных артерий в зернах адсорбентов. Через эту систему пор осуществляется транспорт сорбируемых веществ к внутренней поверхности углеродсодержащего материала. Полости, не сообщающиеся с внешней поверхностью, – криптопоры – с точки зрения адсорбционной практики не имеют никакого значения [11].
4. Влияние солей на окрашенность растворов после собции
Коллоидные системы – дисперсные системы, промежуточные между истинными растворами и грубодисперсными системами – взвесями и эмульсиями [12].
В свободнодисперсных коллоидных системах (дымы, золи) частицы не выпадают в осадок.
Высаливание – это выделение в осадок растворенного вещества, вызываемое добавкой к раствору больших количеств нейтральных солей [13].
В явлениях высаливания, основное значение имеет вытеснение молекул растворенных веществ из электрического поля ионов, которые сильно связываются с дипольными молекулами растворителя. По своему влиянию на высаливание ионы располагаются в последовательности, называемой лиотропными рядами или рядами Гофмейстера, в частности для натриевых солей: SO42- > цитрат > ацетат > Cl->NO3->Br->J->CNS-, где левые члены ряда способствуют высаливанию, а правые три члена препятствуют высаливанию; для хлористых солей Li+>Na+> K+>NH4+ [13].
Лиотропные ряды проявляются также во влиянии ионов на набухание, застудневание, поверхностное натяжение, повышение растворимости. Ионы, способствующие высаливанию (SO42-, Li+) усиливают упорядоченность расположения молекул воды, что соответствует как бы понижению температуры растворителя, а ионы, стимулирующие повышение растворимости (J-, CNS-, K+), усиливают степень дезориентации молекул воды, что соответствует как бы повышению температуры растворителя; таким образом они связывают лиотропные ряды с изменением «структурной температуры» растворителя.
Выводы
Магистерская работа посвящена актуальной задаче поиска новых адсорбентов на основе быстровозобновляемого растительного сырья. В рамках проведенных исследований выполнено:
- В ходе написания магистерской работы были изучены и систематизированы данные о способах получения адсорбентов из растительного сырья, в частности – крахмала.
- Изучены методики спектрофотометрического анализа.
- Подтверждено, что крахмал может быть использован в качестве легковозобновляемых источников сырья для производства активированного угля.
- Установлено, что крахмал проявляет свои адсорбционные свойства при взаимодействии с микрокремнеземом.
- Определено, что добавление в смесь крахмала с активатором таких солей, как AlCl3 и NaCl уменьшает содержание водорастворимых веществ в продуктах пиролиза.
- Изучено, что полученные адсорбенты могут применяться для сорбции фенола из водных растворов
Производство и применение углеродсодержащих адсорбентов на основе природных минеральных и органических компонентов, является целесообразным, т.к. они могут заменить существующие адсорбенты получаемые на основе древесины, что значительно улучшит состояние окружающей среды региона.
При написании данного реферата магистерская работа еще не завершена. Окончательное завершение: май 2020 года. Полный текст работы и материалы по теме могут быть получены у автора или его руководителя после указанной даты.
Список источников
- Грег, С. Адсорбция, удельная поверхность, пористость/ С. Грег. – М.: Мир, 1984. – 306 с.
- Фенелонов, В. Б. Пористый углерод / В. Б. Фенелонов. – Новосибирск.: Химия, 1995. – 513 с.
- Кинхле, Х. Активные угли и их промышленное применение / Х. Кинхле, Э. Бадер . – Л.: Химия, 1984. – 216 c.
- Кузнецов, Б. Н. Новые подходы в переработке твердого органического сырья / Б. Н. Кузнецов – Красноярск, 1991. – 371 с.
- Трепнел, Б. Хемосорбция / Б. Трепнел. – М.: Издательство иностранной литературы, 1958. – 326 с.
- Бур, Я. Х. Динамический характер адсорбентов / Я. Х. Бур – М.: Издательство иностранной литературы, 1962. – 291 с.
- Кельцев, Н. В. Основы адсорбционной техники / Н. В. Кельцев – М.: Химия, 1984. – 592 с.
- Гориславец, С. П. Пиролиз углеводородного сырья / С. П. Гориславец, Д. Н. Тменов, – Киев: Наукова думка, 1977. – 309 с.
- Мухин, В. М. Новые технологии получения активных углей из реактопластов / Мухин В. М., Зубова И. Д., Гурьянов В. В., Курилкин А. А., Гостев В. С.– 2009 - 195 с.
- А. О. Еремина, Углеродные адсорбенты из гидролизного лигнина для очистки сточных вод от органических примесей / А. О. Еремина, В. В. Головина, Н. В. Чесноков, Б. Н. Кузнецов - Journal of Siberian Federal University. Chemistry 1 (2011 4) С.100-107
- Манина Т. С. Получение и исследование высокопористых углеродных сорбентов на основе естественно окисленных углей кузбасса. Дис.к.х.н., Кемерово, 2013, - 133 с.
- Болдырев А. И. Физическая и коллоидная химия / А. И. Болдырев. - М., 1983.
- Кабачный В. И. Физическая и коллоидная химия / В. И. Кабачный, Л. К. Осипенко, Л. Д. Грицан и др. - Х., 1999.
