Реферат за темою випускної роботи
Зміст
- Вступ
- 1 Дефосфорація сталі
- 1.1 Дефосфорація сталі у відновлювальних умовах
- 1.2 Дефосфорація сталі у вакуумі
- 1.3 Дефосфорація сталі в високолегованих сталях
- Список використаних джерел
- STUDYPORT [Электронный ресурс], 2020 – Режим доступа: https://studyport.ru/referaty/tehnika...
- VT-METALL металлообрабатывающая компания [Электронный ресурс], 2020 – Режим доступа: https://vt-metall.ru/articles...
- Т.3: Сборник научных трудов Черная металлургия России и стран СНГ в XXI веке / Москва, 1994.
- Краснянская, И.А. Исследование закономерностей удаления фосфора и се-ры из оксидных расплавов для разработки технологии предварительного ра-финирования сплавов железа в печах барботажного типа: дис. на соиск. учен. степ. канд. техн. наук (05.16.02) / И.А. Краснянская. – Москва, 2015. – 127 с.
- Т.2: Сборник научных трудов Черная металлургия России и стран СНГ в XXI веке / Москва, 1994.
- Способ дефосфорации легированного металла в электропечи // Патент России № 2009208. 1994. Родинков С.В., Антипов В.М., Гутовский И.Б., [и др.].
Вступ
Фосфор потрапляє в сталь головним чином з вихідним чавуном, використовуваним для виплавки сталі.
Фосфор володіє великою схильністю до ліквації, тому навіть при незначній середній кількості фосфору в литві завжди можуть утворитися ділянки, багаті фосфором.
Розташований поблизу кордонів фосфор підвищує температуру переходу в крихкий стан (хладноломкість). Тому фосфор, як і сірка, є шкідливою домішкою, зміст його в вуглецевої сталі допускається до 0.050% [1].
Сегрегація фосфору (Р) в значно меншій мірі, ніж сірки і вуглецю, відбувається в ході затвердіння сталей. Чим більший відсоток фосфору містить сталь, тим вища її холодноламкість і нижче ударна в'язкість, пластичність.
Висока температура середовища дозволяє досягти розчинності фосфору в межах 1,2%. Чим нижче стає температура, тим менше розчинність фосфору. Вона поступово опускається до 0,02-0,03%. Це може говорити про те, що він, як правило, повністю розчиняється в альфа-залізі.
Відпускна крихкість хромистих, хромонікелевих і хромомарганцевих, марганцевих і магнієво-кремнієвих легованих сталей багато в чому залежить від сегрегації фосфору по межах зерен. Елемент сприяє уповільненню розпаду мартенситу і підвищує упрочняемость.
Наявність фосфору в хромонікелевих аустенітних сталях призводить до збільшення межі плинності. При попаданні аустенітної нержавіючої сталі в середу сильного окислювача присутність в її складі фосфору викликає корозію на кордонах зерен. Така поведінка зумовлена сегрегацією фосфору на цих кордонах [2].
Далі розглянемо принципи видалення фосфору при різних умовах.
1 Дефосфорація сталі
1.1 Дефосфорація сталі у відновлювальних умовах
Ця технологія дефосфорації перспективна для сталі, що містить у своєму складі значну кількость хрому, марганцю, вуглецю або інших активних елементів.
За класичною технологією видалення фосфору з рідкої сталі протікає в період, що позначається умовно з моменту закінчення розплавлення шихти до кисневої продувки ванни. Поряд з фосфором в цей же час окислюється помітна частина втримуючихся в сталі дорогих легуючих, які губляться безповоротно з видаляємим з печі шлаком.
За новою технологією пропонується рафінувати метал від фосфору в відновлювальний період плавки. В цьому випадку дефосфорацію сталі здійснюють після проведення операції по раскислению і десульфурації металу або поєднують з цими процесами. В результаті угар елементів практично відсутній, а рафінувальний шлак містить мінімальну кількість оксидів цінних легуючих.
У якості дефосфораторів застосовують метали лужної і лужно-земельної групи або їх сполуки. Так, при використанні кальцію процес видалення фосфору з рідкого заліза описується реакцією 3 (Са) + 2 [Р] = (Са2Р2), а зміна стандартної вільної енергії AF ° = 88230 + 40,4Г, кал.
Повноті розвитку рафінувального процесу сприяє зниження температури ванни. Розрахунки показали, що зменшення температури металевого розплаву на 100 °C знижує рівноважну концентрацію фосфору в сталі більш ніж в 2 рази. Таким чином, температурний фактор має важливе значення для успішного здійснення відновної дефосфорації сталі.
Відомо також, що кальцій має значно більшу спорідненість до кисню, ніж до фосфору. Тому для переважного з'єднання кальцію з фосфором необхідні безокисні умови. Практично забезпечити їх можна за рахунок глибокого розкислення металевої ванни, низького вмісту монооксиду заліза в шлаковій фазі і мінімального вмісту кисню в пічної атмосфері.
Приведена реакція є оборотною. Тому при зміні зазначених умов можлива рефосфорація металу. Звідси важливе значення приймає тривалість обробки ванни реагентом-дефосфоратором. На ефективність дефосфорації може також впливати і спосіб введення кальцію в піч.
Після визначення необхідних технологічних параметрів процес відновної дефосфорації був випробуваний в 0,3т плазменнодуговій печі постійного струму на експериментальній базі ЦНІІчермету і в 3т дуговій печі на одному з машинобудівних заводів. Плазмообразуючим газом служив технічно чистий аргон. У якості дефосфоратора застосовували металевий кальцій або карбід кальцію (останній головним чином для вуглецевих сталей). Шихту становили з 100% відходів сталі заданої марки. Після повного розплавлення шихти шлак скачували (повністю або частково), в метал присажували раскислителі двох видів, потім наводили рафінувальний шлак з суміші вапна і плавикового шпату, а також порошкоподібного раскислителя в дещо зміненій пропорції в порівнянні зі звичайною технологією. Піч ущільнювали. Далі в піч порціями протягом ~ 15 хв вводили дефосфоратор. Після закінчення реакції фосфорвмістовий шлак повністю видаляли з печі. Подальші операції проводили за загальновідомою технологією.
Ступінь видалення фосфору з рідкої сталі за новою технологією (в відновлювальний період плавки) досягала 40%. При цьому зміст легуючих елементів зберігалося незмінним. Одночасно з фосфором віддалялося до 50% міститься в стали сірки.
Досліди в 3т дугової печі підтвердили ефективність нової технології дефосфорації сталі [3].
1.2 Дефосфорація сталі у вакуумі
Ступінь видалення фосфору помітно знижується при наявності оксидів заліза у розплаві. Можливість видалення оксиду фосфору із з'єднання з залізом по реакції
12(FePO4)=4(Fe3O4)+6{P2O5}+{O2}
можна оцінити, використовуючи дані термодинамічного моделювання програми HSC Chemistry 6.0 (малюнок 1)
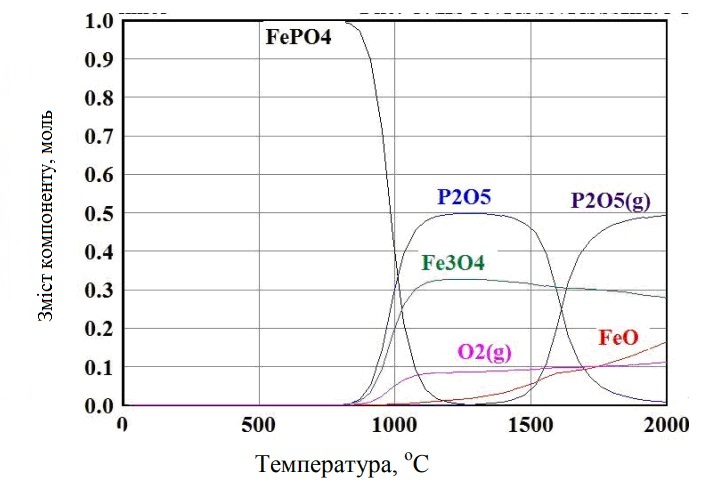
Малюнок 1 - Результати термодинамічного моделювання поведінки фосфату заліза у залежності від температури
На графіку видно, що при Т = 1500 °С міцних сполук фосфору і заліза немає, і фосфор повинен перебувати в газоподібному стані. Оцінимо температуру, при якій в такій системі тиск P2O2(г) = 1 атм і з урахуванням активностей компонентів в розплаві фосфор переходить в газову фазу.
Температурну залежність константи рівноваги реакції можна визначити, використовуючи дані програми HSC Chemistry 6.0 (таблиця 1).
Таблиця 1 - Залежність константи рівноваги реакції від температури

Температурна залежність константи рівноваги виражається рівнянням:
![]()
Була отримана залежність можливості переходу фосфору в газову фазу від температури. При цьому враховувалося, що Pp2o5 = 1 атм. Однак якщо процес проводити в вакуумі, то слід очікувати більш повного протікання процесу видалення фосфору в газ. Аналогічну дію може надавати продування інертними або окисними газами.
1.3 Дефосфорація сталі в високолегованих сталях
Можна виділити ряд напрямків у вирішенні проблеми видалення фосфору з високолегованих розплавів, заснованих на розведенні шихти малофосфорістимі матеріалами, дефосфорація електрохімічним методом, обробці жужільними сумішами в відновлювальних умовах, дефосфорація шляхом утворення летючих сполук фосфору (галогенів, фосфіну і ін.), Зв'язуванні фосфору фосфідообразуючими єлементами (В, Nb, Zr, V, Са, Mg, РЗМ).
Аналіз економічних, технологічних і екологічних аспектів перерахованих способів дозволяє зробити висновок, що найбільш перспективними напрямками рафінування високолегованих сталей і феросплавів від фосфору слід вважати шлакову дефосфорацію у слабоокислювальних умовах, переклад цього елементу в газову фазу і зв'язування його в стійкі неметалеві включення типу фосфидів.
Для розплавів, де основними легуючими компонентами є W, Сг у певній мірі V, доцільно проводити дефосфорацію у слабоокислювальних умовах (10 ~ 14 атм.), що дозволяє істотно спростити видалення фосфору і уникнути помітного угару легуючих. Однак в цьому випадку використання традиційних пічних шлаків виявляється неефективним. Наприклад, для сталі типу Х18Н10 парціальний тиск кисню не повинен перевищувати 10-12 атм. (це відповідає рівновазі металевого розплаву, що містить 18% Р, зі шлаком, насиченим Сг203 при 1 823 К). При таких значеннях р окислювальна дефосфорація ефективно може здійснюватися тільки з використанням флюсів, що володіють високою фосфатной ємністю С. До таких рафінуючих сумішей відносяться системи СаО-CaF2; BaO-BaCl2: BaO-BaF 2; NaO-SiО2; BaO-MnO, сорбційна здатність яких по відношенню до фосфору на 46 порядків перевищує можливості пічних шлаків.
Разом з тим необхідно відзначити нестабільність отриманих результатів з видалення фосфору з високохромистих розплавів, що пов'язано перш за все з кінетичними труднощами протікання процесу через гетерогенізації шлаку і зниженням його фосфатной ємності за рахунок переходу в нього хрому з металу.
Дефосфорація за рахунок переведення фосфору в газову фазу. На основі термодинамічного аналізу процесу дефосфорації корозійностійкої сталі типу Х18Н10 при обробці газовими сумішами, що містять водяну пару, і шлаком з низьким окислювальним потенціалом, показана принципова можливість перекладу фосфору з високолегованого розплаву у газову фазу. Розглянуто два механізми видалення фосфору: за першим фосфор в чистому вигляді або у вигляді сполук переходить в газову фазу; по другому фосфор спочатку переходить в шлак, а далі в газову фазу [4].
Процес дефосфорації може бути полегшений, якщо в зону реакції штучно додати вуглець, наприклад, у вигляді графіту.
Найбільш близькі по технічній сутності і досягаємому результату є спосіб дефосфорації сталі в високочастотій індукційній печі. Тигель магнезитовий. Піч додатково обладнана кришкою для ізоляції металу, що плавиться від повітряної атмосфери [5].
За способом-прототипу після повного розплавлення і нагріву металу до необхідної температури метал раскисляють алюмінієм на 0,3-0,4%, піч накривають кришкою, плавильний простір заповнюють аргоном з витратою 2 нм3/год і на метал присажують дефосфораційну суміш, що складається з Ca-CaF2, або карбіду кальцію в кількості 20-25 кг/т і плавикового шпату у кількості 6-10 кг/т. Після здійснення дефосфорації, тривалість якої 10-20 хв фосфоровмісний шлак скачується з печі і піддається окисленню з метою запобігання шкідливих виділень PH3 у атмосферу цеху. В результаті вміст фосфору в високохромистій сталі знизився з 0,030% до 0,016% тобто на 47% [6].
Розрахунок реакцій видалення шкідливих газів PH2 в виде: P + 2H(g) = PH2(g) и PH3 в виде: Ca3P2 + 3H2O = 3CaO + 2PH3(g) у программі HSC Chemistry 5 показал слідуючі результаты (таблиця 2, 3):

Таблиця 2 – Результати розрахунку реакцій виділення шкідливі газів в програмі HSC Chemistry 5

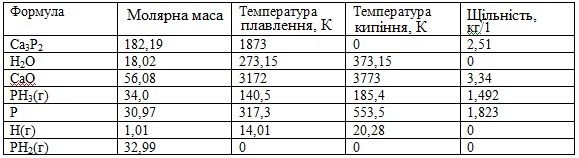
Таблиця 3 – Характеристика речовин, задіяних в реакціях
Залежність ΔG від температури для двох реакцій наведена на малюнках 1 і 2.

Малюнок 1 - Залежність ΔG від температури реакції P + 2H(g) = PH2
Малюнок 2 - Залежність ΔG від температури реакції Ca3P2 + 3H2O = 3CaO + 2PH3(g). Реакції протікають у сторону отримання продуктів реакції. Характеристика речовин, задіяних в даних реакціях наведена у таблиці 4 Таблиця 4 - Характеристика речовин, задіяних в реакціях При написанні даного реферату магістерська робота ще не завершена. Остаточне завершення: листопад 2021 року. Повний текст роботи
і матеріали по темі можуть бути отримані у автора або його керівника після зазначеної дати.
Список використаних джерел
