Реферат за темою випускної роботи
Зміст
- Вступ
- 1. Аналіз публікацій
- 2. Постановка проблеми дослідження
- 3. Викладення матеріалу і результатів
- Висновки
- Перелік джерел
Вступ
Серед продуктів, одержуваних за допомогою хімічного синтезу, значна частка припадає на метанол. Метанол є гарною заміною для палив і сировиною для багатьох виробництв органічного синтезу. До перспективних напрямків використання метанолу відносяться: виробництво оцетової кислоти, очищення стічних вод, виробництво синтетичного протеїну, синтез вуглеводнів з метою отримання палива.
Важливою задачею є зниження собівартості виробництва метанолу та підвищення екологічної безпеки за рахунок реалізації сучасних підходів. Для ефективного використання передового світового досвіду в цій галузі необхідна розробка в рамках вітчизняної науки рішень для вивчення, оптимізації та управління сучасним обладнанням і процесами.
1. Аналіз публікацій
Принципово технологічний процес отримання метанолу включає ряд операцій, які обов'язкові для будь-якої технологічної схеми синтезу [1, 2]:
- отримання синтез-газу (газу, основними компонентами якого є H2 і CO, що містяться в заданій пропорції);
- очищення синтез-газу від карбінолу заліза і сірчастих сполук;
- підігрівання газу до температури початку реакції;
- робота газу в реакторі синтезу метанолу;
- виділення з потоку газів, що залишають реактор, метанолу за рахунок охолодження;
- стиснення газу, що залишився, до тиску синтезу і повернення в процес.
Класична технологія синтезу метанолу припускає використання в якості реакторів колон синтезу (рисунок 1). При цьому рівноважна ступінь перетворення метанолу за один прохід, як правило, не перевищує 20%.
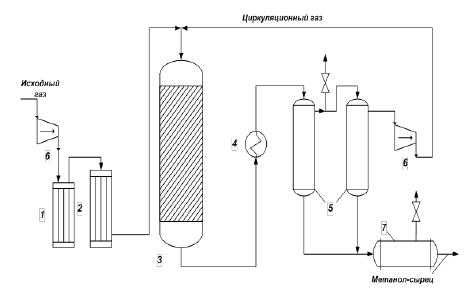
Рисунок 1 - Схема синтезу метанолу
(1 - масляний фільтр, 2 - вугільний фільтр, 3 - колона синтезу; 4 - холодильник-конденсатор, 5 - сепаратори; 6 - компресори; 7 - збірник)
Декілька десятиліть тому компанією Лургі були розроблені трубчаті реактори, в яких тепло реакцій передається киплячій воді.
Водоохолоджувальний реактор синтезу метанолу представляє собою вертикальну шахту з трубчатим теплообмінником і фіксованими трубними решітками. Каталізатор розташований в трубках і лежить на підстилці з інертного матеріалу. Кипляча вода заповнює міжтрубний простір. Паро-водяна суміш, отримана завдяки теплу реакцій, відводиться з під верхньої трубної решітки. Контроль тиску пари дозволяє управляти температурою реакції. Цей ізотермічний реактор дозволяє досягти високої продуктивності при низькій частці повернення та мінімізує виробництво попутних продуктів.
Останнім часом компанією Лургі розроблена подвійна система реакторів, в рамках якої ізотермічний водоохолоджувльний реактор поєднується з газоохолоджуємим реактором. Також відомий цілий ряд праць, які пропонують високоефективні реактори синтезу метанолу, в яких в тій чи іншій мірі використовуються викладені вище підходи [3].
Таким чином, освоєння водоохолоджувальних реакторів і подвійних систем реакторів є актуальною задачею для вітчизняної хімічної промисловості, тому що при цьому виробничий комплекс стає більш компактним, зменшуються капітальні витрати на його спорудження і витрата енергії на виробництво одиниці продукції.
2. Постановка проблеми дослідження
У цій роботі вирішується задача створення концептуальних і алгоритмічних основ систем діагностики теплової роботи водоохолоджувальних реакторів синтезу метанолу. Задача вирішується за рахунок розробки методики складання теплового балансу реактора та її використання для визначення важливих технологічних параметрів на стадії проектування (максимальні і номінальні витрати пари і живильної води) і створення алгоритму для оперативної діагностики теплової роботи реактора шляхом визначення частки витрачання монооксиду вуглецю в реакціях синтезу і відповідно винесення судження про виснаження каталітичної здатності каталізатора.
3. Викладення матеріалу і результатів
Схема водоохолоджувального реактора синтезу метанолу із запропонованим набором елементів КВП та АСУ ТП для діагностики теплової роботи представлена на рисунку 2.
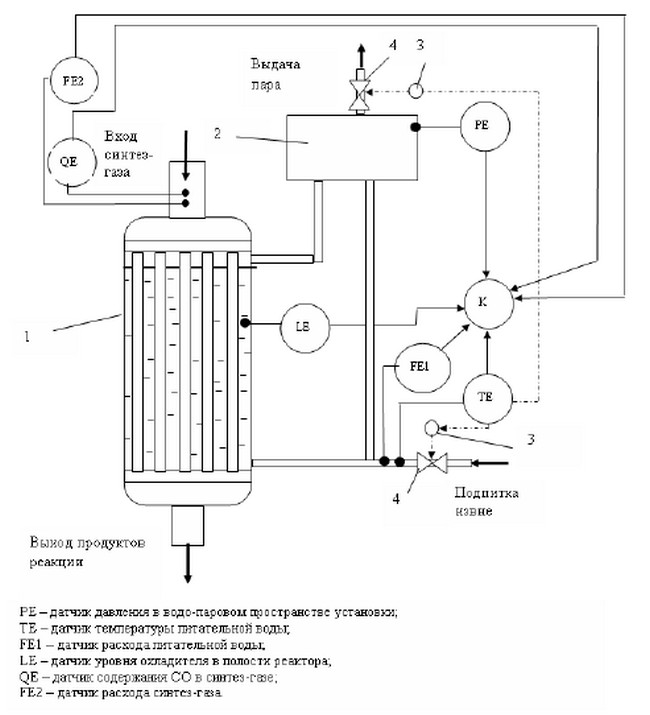
Рисунок 2 - Система діагностики теплової роботи реактора синтезу метанолу
(1 - водоохолоджувальний реактор, 2 - сепаратор, 3 - виконавчі механізми, 4 - регулюючі органи)
Постійна температура в порожнині реактора підтримується за рахунок встановлення тиску пари за допомогою відповідних регулюючих органів. Пароводяна суміш, що утворюється при кипінні води в міжтрубному просторі, піднімається в сепаратор, в якому відділяється і виводиться сухий насичений пар. Поповнення маси охолоджувача реалізується за рахунок підведення свіжої живильної води. Витрата підживлюючої води визначається з умови підтримки заданого рівня охолоджувача в міжтрубному просторі реактора або заданої маси охолоджувача в реакторі. У першому випадку необхідне використання датчика рівня, у другому зважування реактора за допомогою тензодатчиків. На думку авторів, через малу частку випаровуваної рідини в порівнянні з її загальною масою в реакторі, верхній рівень рідини в реакторі буде мати хоча декілька коливну проте досить чітку межу, що дозволяє використовувати, наприклад, ємнісні датчики рівня.
Складання теплового балансу водоохолоджувального реактора необхідно як на стадії його проектування, так і для створення алгоритму управління і моніторингу.
На стадії проектування сепаратора необхідно знати номінальну і максимальну витрати пари, які будуть утворюватися в реакторі.
Ці величини можуть бути визначені за допомогою наступного комплексу залежностей:
| Qp= ξ · | CO | · | V | · | 1 | · QM , | (1) |
| 100 | 3600 | 22,4 |
де Qp – тепловиділення в реакторі синтезу метанолу, Вт;
ξ – частка витрат монооксиду вуглецю в реакціях синтезу;
СО – процентний вміст монооксиду вуглецю в синтез-газі, %;
V – об'ємна витрата синтез-газу, м3/год;
Qм – тепловий ефект утворення метанолу, Дж/кмоль.
| Gпар= | Qp | , | (2) |
| iнп − iжв |
де Gпар – витрата пари з сепаратора, кг/с;
iнп, iжв – ентальпія насиченої пари на виході з реактора і живильної води відповідно, Дж/кг.
Ентальпія живильної води обирається в залежності від її тиску і температури, а насиченої пари - в залежності від заданого рівня тиску в водо-паровому просторі з термодинамічних таблиць, що описують властивості води і водяної пари, [4] або відповідних інтерполяційних залежностей.
Тиск у водо-паровому просторі обирається виходячи з умови забезпечення заданої температури кипіння води, що і визначає стабілізоване значення температури в реакційному просторі. Для визначення максимально можливого виходу пари в якості аргументів для залежностей (1) і (2) використовуються максимально можливі за технологією витрата синтез-газу і добуток змісту синтез газу на частку його засвоєння в реакції. Для визначення номінального значення цієї величини аргументи встановлюються на проектному рівні.
Для проектування системи постачання реакторів живильною водою повинні бути визначені номінальне і максимальне значення цієї величини. Для кожного з характерних режимів роботи реактора масова розрахункова витрата живильної води дорівнює відповідному розрахунковому виходу пари.
Приклад використання запропонованих залежностей для визначення витрати живильної води представлений на рисунку 3. При цьому були використані такі вихідні дані:
Вміст СО в синтез-газі, % ……………………………….….21,5
Ентальпія насиченої пари при тиску 43 атм, кДж/кг…....2799
Ентальпія живильної води (43 атм, 50oС), кДж/кг ……………..213
Тепловий ефект реакції утворення метанолу, МДж/кмоль ...110,8
Діагностику протікання реакцій і аналіз виснаження реакційної здатності каталізатора запропоновано вести на підставі аналізу величини витрат монооксиду вуглецю в реакціях синтезу, розрахованої в залежності від поточної витрати живильної води:
| ξ = | Gв · (iнп − iжв) · 100 · 3600 · 22,4 | . |
| CO · V · Qм |
Використання запропонованої залежності представлено на рисунку 4. При цьому були взяті ті ж вихідні дані, що і при побудові рисунка 3.
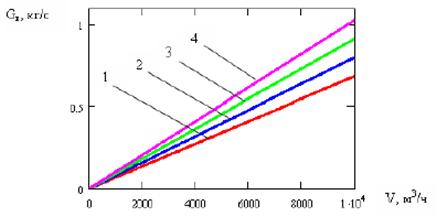
Рисунок 3 - Залежність витрати живильної води від витрати синтез-газу через апарат
(1 – для частки використання монооксиду вуглецю 60%, 2 – 70%, 3 – 80%, 4 – 90%)
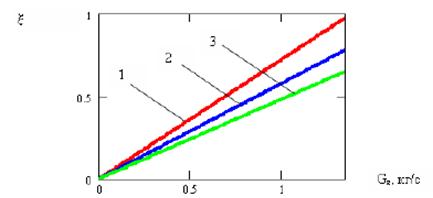
Рисунок 4 - Залежність частки прореагувавшого монооксиду вуглецю від витрати живильної води
(1 – для витрати синтез-газу 10000 м3/год, 2 – 15000 м3/год, 3 – 18000 м3/год)
Представлена на рисунку 4 інформація показує, як для заданих параметрів роботи реактора в залежності від витрати живильної води може бути однозначно визначена величина витрат монооксиду вуглецю в реакціях синтезу, що дозволяє в реальному часі отримувати інформацію про інтенсивність протікання реакцій і виносити судження про виснаження реакційної здатності каталізатора.
Наявність такої інформації необхідне для прийняття рішення про припинення процесу для заміни або регенерації каталізатора. Накопичення цієї інформації та її аналіз спільно зі статистикою зміни інших важливих виробничих факторів дозволяють поглибити уявлення про процес і підібрати умови, що дозволяють розширити часові рамки використання каталізаторів.
Створення передумов для раціонального використання сучасного обладнання синтезу метанолу підвищує екологічну безпеку за рахунок скорочення обсягів перероблюваної сировини, зниження обсягів шкідливих викидів в атмосферу та зменшення площ займаних відповідними підприємствами.
Висновки
Обгрунтовано доцільність розробки систем діагностики теплової роботи водоохолоджуваних реакторів синтезу метанолу, що дозволяють на підставі безперервного аналізу теплового балансу виносити судження про виснаження реакційної здатності каталізатора.
Запропоновано конкретна схема діагностики теплової роботи водоохолоджуваних реакторів синтезу метанолу і алгоритм її використання в рамках систем АСУ ТП ділянки синтезу метанолу.
Перелік джерел
- Химическая технология ТГИ / Под ред. Г.Н. Макарова, Г.Д. Харламповича. – М.: Химия, 1986. – 496 с.
- Печуро Н.С. Химия и технология синтетического жидкого топлива и газа / Н.С. Печуро, В.Д. Капкин, О.Ю. Песин. – М.: Химия, 1986. – 352 с.
- Мещеряков Г.В. Химическая технология неорганических и органических веществ, теоретические основы / Г.В. Мещеряков // Химия и химическая технология .– 2009.– №6.– 86-88
- Ривкин С.Л. Термодинамические свойства воды и водяного пара. Справочник. - 2-е изд., перераб., и доп. / С.Л. Ривкин, А.А. Александров – М.: Энергоатомиздат, 1984. – 80 с.
- Теплотехника термической переработки твердых топлив: Учебное пособие/ Кравцов В.В., Бирюков А.Б., Дробышевская И.П. - Донецк: Издательство «Ноулидж», 2011. – 170с.
- Промышленные печи. Справочное руководство для расчетов и проектирования. 2-е издание, дополненное и переработанное. Казанцев Е.И. М., "Металлургия", 1975. 368 с.
- Бондалетова Л.И., Бондалетов В.Г. Процессы переработки сырья и рациональное использование природных ресурсов: Учебное пособие. – Томск: Изд-во ТПУ, 2006. – 160 с.
