Реферат по теме магистерской работы
Содержание
- Введение
- 1. Постановка задачи
- 2. Алгоритмы, применяемые для обработки рентгеномаммограммы
- 3. Обзор исследований и разработок
- 3.1 Детектирование краев новообразований
- 3.1.1 Сегментация рентгенограмм методом аппроксимаций перепада яркости
- 3.1.2 Алгоритм выделения контура изображения оператором Собеля
- 3.1.3 Сопоставительный анализ методов
- 3.2 Детектирование микрокальцинатов на маммограмме
- Выводы
- Список источников
Введение
В настоящее время одним из самых распространенных онкологических заболеваний среди женского населения является рак молочных желез, наиболее эффективное лечение, которого происходит в том случае если он был диагностирован на ранних стадиях, что возможно сделать лишь при прохождении маммографии, результаты которой обработать в кротчайшие сроки можно при помощи компьютерной обработки рентгеновских снимков.
Рентгенмаммография является основным методом объективной оценки состояния молочных желез. Эта методика рентгенологического исследования позволяет своевременно распознать патологические изменения в молочных железах в 95-97% случаев. В последнее время в литературе появились сообщения о том, что маммография может способствовать развитию рака. Однако серьезные исследования, в том числе отечественные, опровергли это. В настоящее время во всем мире женщины старше 40 лет проходят маммографию каждые 2 года, после 50 лет - каждый год.
Маммография - высокоэффективный и безопасный метод исследования, позволяющий выявить опухолевое образование ничтожно малых размеров, которое не проявляется клинически. Ранняя диагностика играет важную роль в проведении своевременного лечения, как результат становится высока вероятность полного выздоровления, в большинстве случаев при сохранении молочных желез [1].
1. Постановка задачи исследования
В связи с неуклонным ростом заболеваемости раком молочной железы, диагностика и лечение этого заболевания на сегодняшний день является одной из главных проблем клинической онкологии. Согласно статистике, ежегодно в США и развитых странах Европы выявляется свыше 900.000 новых случаев рака молочной железы. В структуре заболеваемости и смертности женского населения Украины от онкологических заболеваний рак молочной железы вышел на первое место. В среднем риск заболеть раком молочной железы имеет каждая десятая женщина. Учитывая это, основным направлением современной маммологии по-прежнему является поиск путей ранней диагностики рака молочной железы.
Основной задачей данной работы является создание нового программного продукта определения патологических изменений молочных желез, который бы был независимым от каких-либо конкретных установок, определял бы места патологических изменений с координатами их расположения, самостоятельно бы рассчитывал размеры патологий и делал вывод о возможной дальнейшей диагностике, а также формировал соответствующий отчет.
Основной целью является разработка специализированной компьютерной системы, которая будет определять патологические изменения молочной железы по полученным рентгеновским снимкам.
Объектом исследования в данной работе являются изображения молочной железы, полученные путем снятия рентгенограммы. Основными требованиями к компьютерной системе обработки таких изображений являются: точность, скорость обработки данных, адаптивность к обработке различных типов патологий.
Предметом исследования являются методы обработки рентгеновских снимков молочной железы, позволяющие определить наличие новообразований и степень их доброкачественности.
Задания для создания специализированной компьютерной системы определения патологических изменений молочных желез по рентгеновским снимкам можно сформулировать следующим образом:
- предварительный анализ изображения;
- выбор методов обработки изображения;
- разработка соответствующего программного обеспечения;
- расчет параметров патологических участков;
- формирование и передача соответствующего отчета врачу;
- апробация системы для определения эффективности ее работы.
2. Алгоритмы, применяемые для обработки рентгеномаммограммы
Сегодня в мире разрабатываются и используются различные системы компьютерного анализа цифровых рентгенограмм, алгоритмы и программы поиска и детализации различных признаков злокачественных процессов.
Система оценки маммограмм – ImageChecker M1000 System – производит компьютерный анализ цифровых маммограмм для выявления микрокальцинатов и плотных масс опухоли как градиентов интенсивности пикселов изображения с разрешающей способностью 50 микрон в 12-битовой серой шкале. Сложные зрительные образы, такие как спикулы, анализируются нейронными сетями. При совместном прочитывании с рентгенологами система улучшает чувствительность маммографии на 8%, так что общая чувствительность достигает 88%. В указанной системе используется мощная компьютерная техника для обработки изображения, при анализе одного снимка проводится приблизительно до 1 млрд. операций.
Английские исследователи описывают специфические модели «спикульных» поражений, в которых анализируются патологические образцы линейных структур и центральных масс на маммограммах. Линейные структуры детектировались с использованием факторного анализа для разделения систематических и случайных особенностей классов образцов. Центральные массы разделялись на рекурсивном медианном фильтровании с использованием признаков локальной ориентации. Для «спикульных» поражений размерами в 16 мм и больших образцов определена чувствительность 80% к 1,4% ложноположительных данных. Определение масс детекции имеет чувствительность 80% к 23% ложноположительных данных на изображении.
Калифорнийские исследователи используют для поиска микрокальцинатов по маммограммам медианную фильтрацию для автоматического анализа морфологии серой шкалы с 20% ложноотрицательных результатов. Анализируют оцифрованные маммограммы с пикселом 70 и 35 микрон и глубиной серой шкалы 4096 (12 бит). Алгоритм определяет микрокальцинаты, которые может пропустить радиолог. Каждый объект классифицируется на три категории: доброкачественные микрокальцинаты, суспициозные и артефакты. Данные представляются радиологу для последующего заключения [2].
Анализ рентгенологической картины показал, что задачи, которые необходимо решить, что бы врач рентгенолог поставил достоверный диагноз, можно свести к следующим:
- повышение контраста (качества) маммограмм;
- детектирование краев новообразований;
- детектирование микрокальцинатов на маммограммах;
- классификация (распознавание) обнаруженных образований.
Контраст изображения может быть увеличен просто, увеличением или растяжением мультимасштабных максимумов градиента изображения. Если работа происходит с вейвлетовскими коэффициентами, то их меняют методом адаптивного выравнивания гистограммы. Изображения с повышенным контрастом обеспечивают тонкие детали тканей, которые являются видимыми с трудоемкими контраст/яркость оконными методами. Увеличение контраста производится любым методом даже классическим линейным.
Учитывая, что микрокальцинаты соответствуют высокочастотным компонентам спектра изображения, их обнаружение осуществляется путем разложения маммограммы на различные частотные полосы, затем подавляются подполосы низкой частоты, затем для восстановления мамограммы используются подполосы только высоких частот. Так же обнаружение микрокальцинатов можно производить и с использованием вейвлет фреймов, оператора улучшения и подходящей технологии реконструкции. Либо же можно использовать метод, основанный на избыточном дискретном вейвлет преобразовании из-за его хороших свойств: постоянство сдвига и численной ошибкоустойчивости. Процедура эта состоит из 3 шагов: удаление низкочастотной компоненты плотной ткани, фильтрация шума и улучшение видимости микрокальцинатов. Так же есть и множество других методов, основанных на классификаторах нейронных сетей, применении адаптивных вейвлетов, технике оптимального взвешивания вейвлет пакетов и т .д.[3]
Для классификации обнаруженных образований можно также использовать вейвлетные методы, такие как: Мультимасштабный статистический подход к анализу структуры, для классификации микрокальцинатов на доброкачественные и злокачественные, извлекая мультимасштабные статистические признаки текстуры, основанные на матрице совместного появления, а так же вейвлетные признаки текстуры, в областях интереса, содержащих микрокальцинаты. И коэффициенты разложения скейлинг функции на некотором масштабе, т.е. когда при больших значениях масштаба скейлинг функция аппроксимирует дельта функцию, ошибка аппроксимации же минимизируется за счет использования генетического алгоритма [4].
3. Обзор исследований и разработок
3.1 Детектирование краев новообразований
В ряде задач диагностики состояния организма используется количественный анализ, который эффективно проводится в цифровых системах анализа медицинских изображений. Наиболее важным этапом в таких системах является выделение исследуемого объекта - этап сегментации. Существует два общих подхода к решению задачи выделения объекта из общей сцены изображения, основанные на альтернативных концепциях; выделение точек изображения, однородных по своим локальным свойствам; выделение точек изображения, свойства которых обладают разрывностью при переходе от одной области к другой. Для рентгенограммы характерным является затемнение объектов друг другом, если на пути ионизирующего излучения они встречаются дважды. Вследствие этого объект наблюдения представляет неоднородную область по оптической плотности на рентгенограмме. Поэтому, для построения алгоритма сегментации предпочтительней концепция, основанная на выделении точек изображения с разрывными локальными свойствами [5].
3.1.1 Сегментация рентгенограмм методом аппроксимаций перепада яркости
Полагаем, что исходное изображение прошло все этапы кодирования, результатом которого является дискретное цифровое изображение вида {fij} (I=0,1,…, N-l; J=0,1,...,M-1), где N и М - число элементов изображения по вертикали и горизонтали, соответственно; fIJ - значение яркости элемента изображения и I-ой строке и J-ом столбце. В реальных условиях цифровое изображение представляет смесь идеального изображения и помехи, которую считаем некоррелированной и гауссовской. Тогда элемент цифрового изображения представляет аддитивную смесь идеального изображения и шума.
Введем систему непрерывных координат XY и шаг Δх по оси X и Δу - по оси Y. Тогда элементы множества fIJ в системе XY располагаются с координатами (I*Δу,J*Δх).
Аппроксимируем перепад контраста в скользящем окне размером n*m прямой линией. Однако, полагается, что линия проходит через фиксированную точку с координатами х0, у0. Введение фиксированной точки позволяет почти в два раза сократить число параметров, которые в дальнейшем подлежат оценке [6]. С учетом принятых допущений модель перепада яркости имеет вид (1).
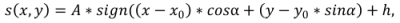 |
(1) |
где 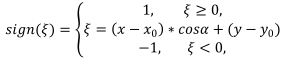
α - направление перепада;
A - половинная часть перепада;
h - смещение перепада.
Параметры перепада α, A, h определяются исходя из минимума ошибки аппроксимации реального перепада яркости. Ошибка аппроксимации дискретных значений {fij}r, принадлежащие окрестности радиусом r и центром в точке (х0,у0) определяется выражением (2).
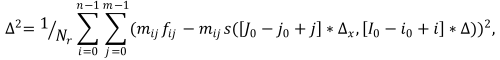 |
(2) |
где
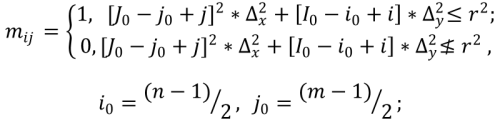
Nr - число элементов множества {fij}r.
3.1.2 Алгоритм выделения контура изображения оператором Собеля
Процесс основан на простом перемещении маски фильтра от точки к точке изображения. В случае линейной пространственной фильтрации отклик задается суммой произведения коэффициентов фильтра на соответствующие значения пикселей в области, покрытой маской фильтра. При обнаружении перепадов яркости используются дискретные аналоги производных первого и второго порядка. Для простоты изложения будут рассмотрены одномерные производные.
Первая производная одномерной функции f(x) определяется как разность значений соседних элементов (3).
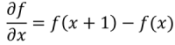 |
(3) |
Аналогично, вторая производная определяется как разность соседних значений первой производной (4).
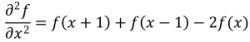 |
(4) |
Вычисление первой производной цифрового изображения основано на различных дискретных приближениях двумерного градиента. По определению, градиент изображения f(x,y) в точке (x,y) — это вектор (5).
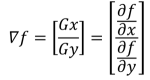 |
(5) |
Как известно из курса математического анализа, направление вектора градиента совпадает с направлением максимальной скорости изменения функции f в точке (x,y).
Важную роль при обнаружении контуров играет модуль этого вектора, который обозначается ∇f (градиент) и равен (6).
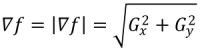 |
(6) |
Направление вектора градиента также является важной характеристикой. Обозначим α(x,y) угол между направлением вектора ∇f в точке (x,y) и осью x, который вычисляется по формуле (7).
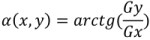 |
(7) |
Вычислить градиент изображения можно, вычислив величины частных производных ∂f/∂x и ∂f/∂y для каждой точки.
Оператор Собеля использует область изображения 3х3 и использует весовой коэффициент 2 для средних элементов (8).
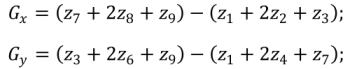 |
(8) |
Это увеличенное значение используется для уменьшения эффекта сглаживания за счет придания большего веса средним точкам [7]. Маски, используемые оператором Собеля:
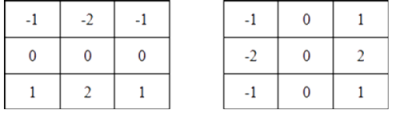
3.1.3 Сопоставительный анализ методов
Можно привести сопоставительный анализ способа сегментации и основанного на градиентном выделении перепадов с использованием оператора Собеля. Для численной оценки при сопоставлении используется показатель правильной классификации граничных (9) и неграничных точек (10).
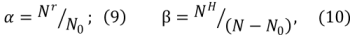
где Nr - число точек правильно классифицированных как граничные, NH - число точек правильно классифицированных как неграничные, N0 - число граничных точек, N-число точек в пределах двумерного изображения [8].
Таблица 1 - Результаты сравнения методов выделения границ объектов.
| Способ сегментации | α | β |
| Оператор Собеля | 0,9 | 0,91 |
| Аппроксимационный подход | 1 | 0,998 |
На основании приведенных результатов можно утверждать: аппроксимационный подход минимизирует число разрывов в контурах объекта на изображении, что является определяющим в пользу предлагаемого способа сегментации.
3.2 Детектирование микрокальцинатов на маммограмме
Примерно в 75% случаев злокачественной опухоли молочной железы встречается местноинфильтрирующий узловой рак, то есть скиррозные опухоли, которые сопровождаются мелкоточечными обызвествлениями – микрокальцинатами (гидроксилфосфат кальция). Установлена совершенно четкая зависимость между числом, характером распределения микрокальцинатов и вероятностью рака. С увеличением числа микрокальцинатов на единицу площади вероятность рака возрастает. Так, при 15 микрокальцинатах на 1 см3 вероятность рака достигает 87%. Выявление микрокальцинатов даже при отсутствии опухолевого узла весьма подозрительно на рак, поскольку микрокальцинаты нередко являются единственным признаком, позволяющим заподозрить рак молочной железы. На рентгеновских маммографических снимках микрокальцинаты выглядят как тонкие и яркие пятна, размером от 0,1 до 0,6 мм, и находятся в области плотной ткани молочных желез, что делает их практически невидимыми [9].
Процесс поиска микрокальцинатов производится по следующей схеме:
- Улучшение качества изображения: фильтрация с помощью вейвлет-преобразований (Добеши 2-ого уровня);
- Определение области интереса с помощью использования статистических характеристик третьего и четвертого порядков: эксцесс и асимметрия;
- Нечеткая кластеризация для выделения узловых структур на области интереса;
- Узловой отбор, для выделить действительных областей микрокальцинатов по параметра: плотность кластера и толщина кластеризации.
Более подробное описание данных методов поиска микрокальцинатов произведено в статье [10], а результаты выполнения приведены на рисунке 1.
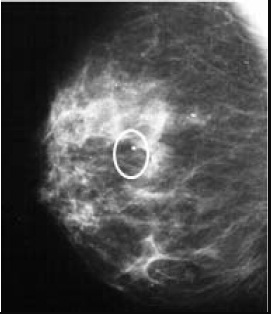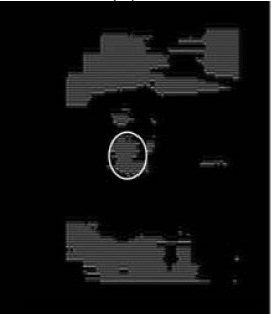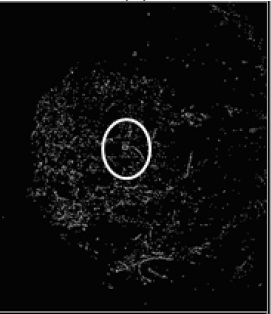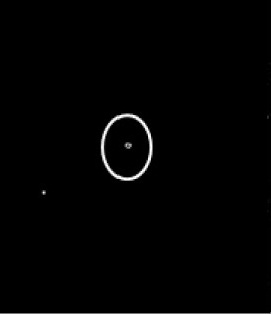
Рисунок 1 - Результат работы выделения микрокальцинатов
Выводы
Среди методов доклинической диагностики рака молочной железы ведущее место сегодня занимает маммография. Современные рентгеновские установки обладают очень высокой разрешающей способностью, позволяя выявлять злокачественные опухоли размером до 2 мм в доклинической стадии. Создавая более эффективные методы обработки рентгеномаммографий можно добиться увеличения успехов в маммографии в области ранней диагностики, которые шире откроют перспективу для применения органосохраняющих операций на молочной железе.
На момент написания данного реферата из предложенных выше 4 пунктов обработки изображения маммограммы был произведен выбор метода выделения края новообразования, и описание алгоритма выделения микрокальцинатов на маммограммах.
При написании данного реферата магистерская работа еще не завершена. Окончательное завершение: декабрь 2013 года. Полный текст работы и материалы по теме могут быть получены у автора или его руководителя после указанной даты.
Список источников
- Терновой С.К. Лучевая маммография / А.Б. Абдураимов, С.К. Терновой – М.: «ГЭОТАР-Медиа», 2007.
- Останькович А.А., Методы обработки маммограмм для выявления скрытых процессов в молочных железах/ А.А. Останькович, С.Д. Вайман, А.П. Тананакин, В.В. Небрат, А.И. Ходанов// Радиология – Новосибирск, 2003.
- Смоленцев Н.К. Основы теории вейвлетов – М: ДМК Пресс, 2005.
- Пикар Д. Вейвлеты, аппроксимация и статистические приложения// перевод К.А.Алексеев - ПГУ, Пенза, 2002.
- Гонсалес Р. Цифровая обработка изображений / Р. Гонсалес, Р. Вудс. – М.: Техносфера, 2005.
- Хюккель М. Оператор нахождения контуров на кодированных изображениях. // Интегральные роботы. - М.: Мир, 2003.
- Буй Т.Т.Ч. Анализ методов выделения краев на цифровых изображениях/ Т.Т.Ч. Буй, В.Г. Спицын// М.: Техносфера,2010.
- Senthilkumaran N. A. Study on Edge Detection Methods for Image Segmentation // N. Senthilkumaran, R. Rajesh // Proceedings of the International Conference on Mathematics and Computer Science – 2009.
- Лучевая диагностика. Заболевания молочных желез / Уве Фишер, Фридеман Баум, Сузанне Люфтнер-Нагель ; пер. с англ. ; под общ. ред. чл.-кор. РАМН, проф. Б.И.Долгушина. – М. : МЕДпресс-информ, 2009.
- Доценко В.В. Выбор метода определения патологических изменений молочной железы по рентгеновским снимкам/ В.В. Доценко, Е.В. Меркулова// Донецьк, ДонНТУ — 2013.
