Реферат за темою випускної роботи
Зміст
- Вступ
- 1. Аналіз теоретичних основ випарювання
- 2. Аналіз технологічного процесу як об’єкту управління з точки зору основних матеріальних потоків та їх інформаційних змінних
- 3. Особливості процесу випарювання в схемі багатоконтурного регулювання
- 4. Математична модель процесу випарювання гідроксиду калію
- 4.1. Структурна схема САР співвідношення потоків вихідного розчину і гріючої пари
- 4.2. Структурна схема САР концентрації розчину гідроксиду калію
- Висновки
- Перелік посилань
Вступ
Хімічна промисловість дозволяє синтезувати матеріали, яких немає в природі, використовувати їх для створення всіляких машин і приладів, для будівництва помешкань і виробництва товарів споживання. Тому хімічна промисловість у світі розвивається швидкими темпами.
Хімічна промисловість випускає синтетичний каучук, пластичні маси, штучне волокно, штучне паливо, барвники, лікарські речовини та багато іншого.
Випарювання – процес концентрування розчинів нелетких речовин шляхом видалення рідкого летючого розчинника у вигляді пари.
Цей процес широко поширений (в хімічній, харчовій, металургійній та інших галузях) з причини того, що багато речовин отримують у вигляді розбавлених водних розчинів, а для подальших виробничих етапів вони потрібні в концентрованому вигляді. Також за рахунок концентрування розчинів зменшується їх об'єм і знижуються витрати на їх транспортування.
У процесі випарювання відбувається часткове видалення розчинника з усього обсягу розчину при його температурі кипіння. Це є принциповою відмінністю випарювання від випаровування, яке відбувається на поверхні розчину при будь-яких температурах нижче температури кипіння. У деяких випадках випарений розчин піддають наступній кристалізації у випарних апаратах, спеціально сконструйованих для цих цілей.
На практиці часто в якості гріючого агента при випарюванні використовують водяний пар, який називають гріючим або первинним. Первинним служить пар, одержуваний з парогенератора, або відпрацьований пар. Пар, який утворюється при випарюванні киплячого розчину, називається вторинним. Тепло необхідне для підтримки процесу зазвичай підводять через стінку. Процес проводять під вакуумом, при підвищеному та атмосферному тиску. Вибір тиску значною мірою залежить від властивостей випарюючого і можливістю використання тепла вторинної пари.
1. Аналіз теоретичних основ випарювання
Випарюванням називають процес концентрування розчинів, що полягає в частковому видаленні розчинника шляхом його видалення при кипінні. Сутність випарювання полягає в переводі розчинника в пароподібний стан і відвід отриманої пари від сконцентрованого розчину, що залишився [1].
Процес випарювання проводять таким чином, щоб при заданій продуктивності отримати розчин необхідної концентрації, належної якості без втрат сухої речовини і при можливо меншій витраті палива. Особливістю процесу випарювання є те, що в парах киплячих розчинів нормально містяться тільки пари чистого розчинника, а розчинена речовина є нелетучою. Це положення, що лежить в основі теорії і методів розрахунку випарних апаратів, для більшості розчинів твердих речовин цілком виправдовується. Розчинник, що видаляється, в пароподібному стані найчастіше представляє собою водяний пар, що носить назву вторинної пари.
В якості теплоносія при випарюванні використовують насичений або злегка перегрітий водяний пар, який називається гріючим або первинним. Первинним служить або пар, що одержується з парогенератора, або відпрацьований пар, або пар проміжного відбору парових турбін. Тепло, необхідне для випарювання розчину, зазвичай підводиться через стінку, яка відокремлює теплоносій від розчину. У деяких виробництвах концентрування розчинів здійснюють при безпосередньому дотику випарюваного розчину з топковими газами або іншими газоподібними теплоносіями. Також може застосовуватися електричний обігрів.
Протікання теплоносіїв у гріючій камері відбувається під дією напору, що створюється ззовні. Швидкість течії теплоносіїв по трубках в більшості випадків визначається природною циркуляцією, що залежить від різниці питомих ваг закипаючого в гріючій камері розчину, пронизаного бульбашками пари, і розчину, що опускається по циркуляційної трубі.
2. Аналіз технологічного процесу як об’єкту управління з точки зору основних матеріальних потоків та їх інформаційних змінних
Дослідимо ТП на наявність матеріальних потоків. Мета управління випарною установкою полягає в отриманні розчину заданої концентрації.
Основною регульованою технічною величиною є концентрація випарюваного розчину на виході з другого випарного апарату. Концентрація випарюваного розчину залежить від витрати і концентрації початкового розчину, витрати гріючої пари, рівня розчину в випарних апаратах [2–4]. Отже, схема матеріальних потоків та інформаційних змінних буде виглядати наступним чином:
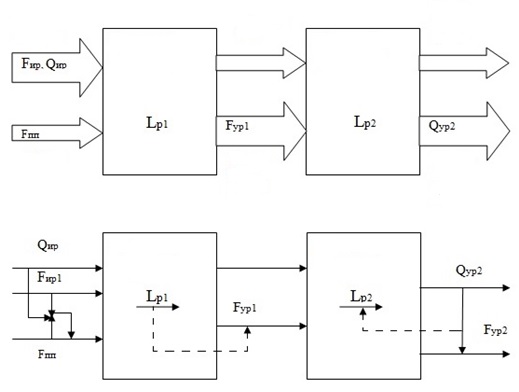
Рисунок 1 – Схема матеріальних потоків та інформаційних змінних процесу випарювання
На рис. 1 застосовані наступні позначення:
- витрата початкового розчину – Fир;
- концентрація початкового розчину – Qир;
- рівень у випарному апараті – Lp;
- концентрація випарюваного розчину – Qyр2;
- витрата первинного пара – Fпп;
- витрата упаренного розчину – Fур2.
До випарного апарату-1 подаються вихідний розчин з певною концентрацією і гріючий пар. Гріючий пар подають в установку в певному співвідношенні з витратою вихідного розчину і з його конценрацією. Далі відбувається часткове випарювання вихідного розчину. Частково випарений розчин відводять з установки за рівнем в першому апараті. Потім отриманий розчин і вторинний пар надходять у другій випарний апарат. Випарений розчин відводять з установки за рівнем в останньому апараті, регулятором, завдання якого змінює регулятор концентрації розчиненої речовини в випареному розчині.
3. Особливості процесу випарювання в схемі багатоконтурного регулювання
Мета управління випарною установкою полягає в отриманні розчину заданої концентрації, а також у підтримці матеріального і теплового балансів.
При великих коливаннях витрати вихідного розчину, а також при зміні в ньому концентрації розчиненої речовини, якісне регулювання процесу забезпечується застосуванням складних схем, наприклад, схеми багатоконтурного регулювання, яка представлена на рис. 2 [5–7].
Гріючий пар подають в установку в певному співвідношенні з витратою вихідного продукту. Це співвідношення коригують регулятором концентрації розчиненої речовини у вихідному розчині. Для стабілізації роботи другого випарного апарату частково випарений розчин, що направляється до нього, регулюється каскадною схемою регулювання витрати з корекцією за рівнем розчину у першому випарному апараті. Тиск у системі підтримується на заданому значенні за допомогою регулювання витрати пари розчинника з корекцією за тиском в останньому випарному апараті.
Тепловий баланс процесу випарювання при великих коливаннях витрати вихідного розчину, а також при зміні в ньому концентрації розчиненої речовини, забезпечують регулятором витрати на трубопроводі подачі граючої пари в кип'ятильник 2 першого корпусу установки.
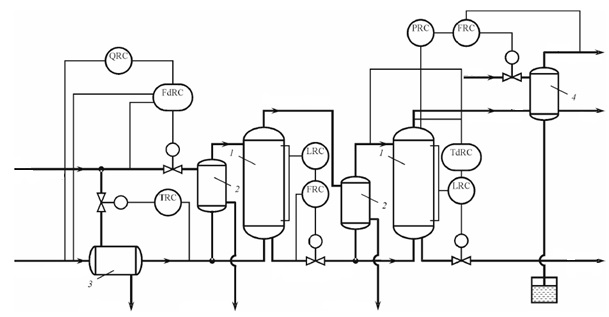
Рисунок 2 – Схема багатоконтурного регулювання двокорпусною випарною установкою
Нормальний тепловий режим роботи випарної установки можливий тільки при подачі вихідного розчину з постійною температурою ТК, близької до температури кипіння розчину. Для досягнення цього встановлюють регулятор температури вихідного розчину, вихідний сигнал якого впливає на клапан, що змінює подачу граючої пари в теплообмінник-підігрівач вихідного розчину 3.
Якщо весь вторинний пар з попереднього корпусу направляють в кип'ятильник 2 подальшого, то тиск (розрідження) стабілізують тільки в останньому корпусі, змінюючи за допомогою регулятора кількість парів розчинника, що відводяться з нього. Останнє зазвичай досягають шляхом зміни подачі охолоджуючої води в барометричний конденсатор 4.
Випарений розчин відводять з установки за рівнем в останньому апараті, регулятором, завдання якому змінює регулятор концентрації розчиненої речовини у випареному розчині.
Якщо витрата початкового розчину залежить від роботи попередніх технологічних установок, але коливання її незначні, то концентрацію випареного розчину можна регулювати зміною подачі гріючої пари на установку. При цьому за допомогою регуляторів рівня у випарних апаратах змінюють кількість відведеного з них розчину.
4. Математична модель процесу випарювання гідроксиду калію
Випарний апарат, будучи великогабаритним апаратом, як об'єкт регулювання, по каналу витрата гріючої пари – концентрація отриманого розчину
володіє значною інерційністю. Динаміку випарного апарату по основному керуючому каналу концентрація отриманого розчину – витрата гріючої пари
можна описати лінеаризованим диференціальним рівнянням ідеального перемішування за умови, що рівень рідини в апараті постійний, тобто виконується умова стабілізації матеріального балансу. Зміна концентрації гідроксиду калію на виході ΔQ з апарату об'ємом V при зміні концентрації ΔQ0 у вихідному розчині повинно усуватися зміною витрати пари ΔF2 [8–10].
Регулювання концентрації розчину гідроксиду калію здійснюється шляхом зміни витрати гріючої пари F2 через регулюючий клапан, який здійснює регулювання в межах 0...100%. На електропривід (виконавчий механізм) регулюючого клапана надходить сигнал завдання відкриття клапана у вигляді нормованого токового сигналу 4...20 мА. Максимальна швидкість переміщення штока складає 25 %/с.
За своїми динамічним властивостями виконавчий механізм являє собою аперіодичне ланку першого порядку з постійною часу 1 с. Трубопровід від клапана до входу випарного апарату моделюється інерційною ланкою першого порядку з коефіцієнтом передачі K = 3/100 і постійною часу T = 2 с. [11]. На вхід ланки повинен подаватися сигнал положення штока у відсотках ходу регулюючого органу (РО) (0...100% ходу РО).
Схема моделювання виконавчого механізму (ВМ) з регулюючим органом (РО) і трубопроводом до випарного апарату зображена на рис. 3.
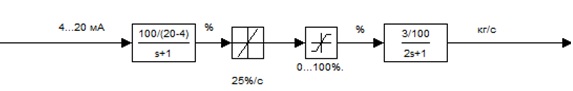
Рисунок 3 – Схема моделювання ВМ з РО, трубопроводом до випарного апарату
4.1. Схема моделювання САР співвідношення потоків вихідного розчину і гріючої пари
У відповідності до обраної ідеології управління комбінована САУ стабілізації концентрації розчину гідроксиду калію складається з двох контурів [12–15]. Внутрішній контур – це контур стабілізації співвідношення витрат вихідний розчин – гріюча пара
. Він регулює витрату гріючої пари F2 у певному співвідношенні з витратою вихідного розчину F1 (так званий регулятор співвідношення потоків). Зовнішній контур стабілізує концентрацію отриманого розчину KOH шляхом зміни витрати пари F2 і змінює завдання регулятору співвідношення в залежності від концентрації КОН на виході випарного апарату.
Побудуємо і проаналізуємо динаміку регулятора співвідношення потоків вихідного розчину і гріючої пари. Структурна схема САР співвідношення потоків буде побудована у відповідності з принципом по відхиленню.
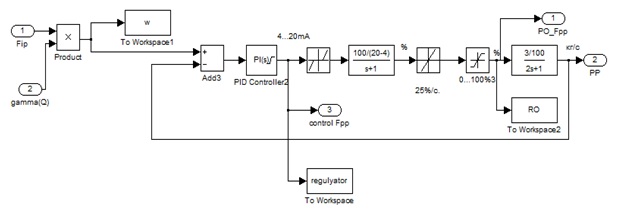
Рисунок 4 – Схема моделювання САР співвідношення потоків вихідного розчину і гріючої пари
Зі структури САР видно, що вихід регулятора співвідношення обмежений можливим діапазоном його вихідного сигналу 4...20 мА, а також є блок зони нечутливості в інтервалі -4....4 мА, що випливає з нижнього граничного значення діапазону вихідного сигналу контролера. Далі йде модель ВМ, РО та трубопроводу, розглянута вище.
Основне завдання синтезу САР полягає у виборі закону регулювання та визначенні настроювальних параметрів регулятора. З практики застосування регуляторів співвідношення потоків приймаємо ПІ-закон управління.
Значення параметрів настройки, досить близькі до оптимальних, можуть бути отримані в результаті дослідження динаміки замкнутої системи. В якості методу знаходження настроювальних параметрів регулятора виберемо метод автоматичної настройки блоку PID-control пакета моделювання Matlab, оскільки методи автоматичної оптимізації є потужним засобом сучасних промислових контролерів. Метод автоматичної настройки грунтується на трьох етапах: ідентифікації моделі об'єкта, визначенні параметрів регулятора і настройці параметрів.
Вибір вищезгаданого методу обумовлений тим, що параметри регулятора, що визначаються за існуючими і широко поширеними методиками Зіглера і Нікольса, а також CHR (Chien, Hrones і Reswick) потім настроюються вручну або автоматично у процесі аналізу динаміки САР.
При настройці регулятора основна увага приділяється відпрацюванню зміни сигналу уставки, оскільки контур регулювання витрати гріючої пари в співвідношенні з витратою вихідного розчину є внутрішнім контуром САР концентрації гідроксиду калію. Таким чином, з урахуванням обмежень на вихідний сигнал регулятора 4...20 мA і швидкість РО 25 %/c, параметри настройки ПІ-регулятора мають такі значення: Kp = 0, Ku = 0.67 що забезпечують швидкодію, рівну 16,6 с. На анімації під цифрою 1 наведено графік перехідної характеристики настройки регулятора співвідношення, а під цифрою 2 – графік витрати гріючої пари при зміні витрати вихідного розчину з 0,6 кг/с до 0,5 кг/с.
Перехідна характеристика витрати гріючої пари носить аперіодичний характер з перерегулюванням 8% і часом регулювання 473 с. Дані показники є задовільними для внутрішнього контуру.
На анімації під цифрою 3 і під цифрою 4 наведені графіки перехідних характеристик керуючого сигналу на виході ПІ-регулятора, а також ходу регулюючого органу.
З цих графіків випливає, що регулятор не виходить за межі зони обмеження 4...20 мА, необхідна витрата гріючої пари 2,4 кг/с забезпечується відкриттям клапана на 80%.
4.2. Схема моделювання САР концентрації розчину гідроксиду калію
Зовнішній контур стабілізує концентрацію отриманого розчину KOH шляхом зміни витрати пари F2 і коригує завдання регулятору співвідношення в залежності від концентрації КОН на виході випарного апарату [16–18].
За технологією вимоги до показників САР концентрації наступні:
- аперіодичний характер перехідного процесу з допустимим перерегулюванням 5...10%;
- час встановлення (регулювання) 20 хв;
- час відпрацювання зовнішнього збурення 8-10 хв.
Вихід концентрації розчину гідроксиду калію на уставку 40% вимагає налаштування зовнішнього регулятора по концентрації. Оскільки канал з управління «концентрація – витрата гріючої пари» володіє великою інерційністю [19, 20], а також виходячи з практики необхідно вибрати ПІД-закон управління.
Для розрахунку початкових значень параметрів регулятора концентрації був застосований метод CHR по відгуку на зовнішні обурення. Початкові розрахункові дані наступні: Kp = -0.026, Ku = -6e-4, Kd = -2.1. Однак при такому значенні диференціальної складової вихід регулятора виходить за межі обмежень його вихідного сигналу і тому дані початкові значення були оптимізовані за допомогою автоматичного методу підстроювання.
Результати моделювання були отримані за схемою моделювання САР. Підсистема САР співвідношення потоків реалізована на рис. 5
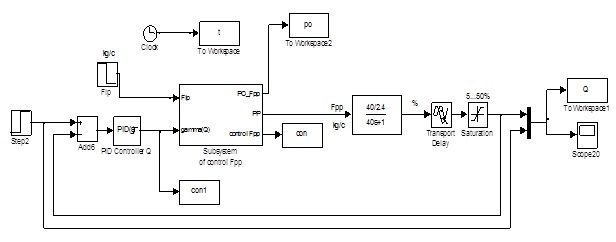
Рисунок 5 – Схема моделювання двохконтурної САР концентрації розчину гідроксиду калію
Результати автоматичної настройки забезпечили задані вимоги з якості перехідного процесу. Графік перехідної характеристики регулятора, графік перехідної характеристики концентрації КОН та графік перехідного процесу регулятора співвідношення при відпрацюванні уставки концентрації на 40% наведені у анімації під цифрами 5, 6 та 7 відповідно.
Аналіз перехідної характеристики по концентрації розчину гідроксиду калію на виході показує, що регулятор відпрацьовує зовнішнє обурення на систему за 9 хв, не виходячи за допустимий діапазон зміни по концентрації, що відповідає вимогам.
Перехідна характеристика по концентрації розчину носить аперіодичний характер з перерегулюванням 6% і часом регулювання 527 с.
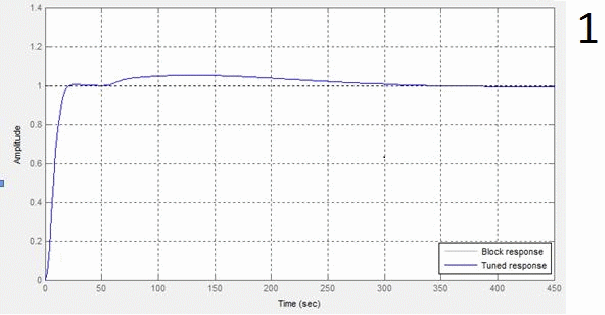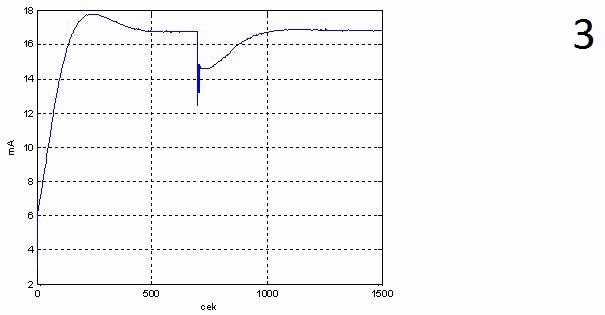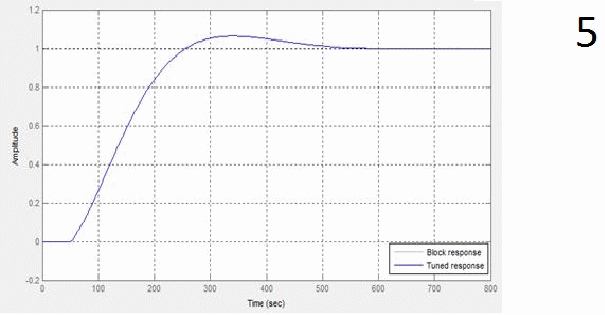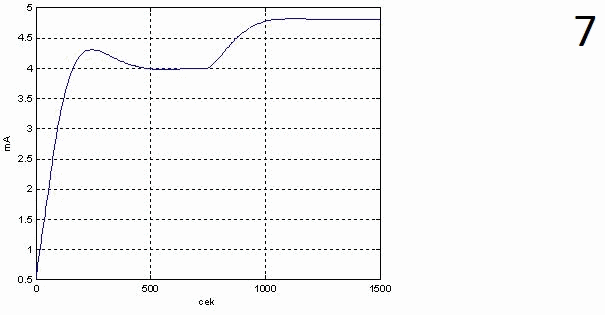
1 – вікно налаштування параметрів блоку PID-control,
2 – графік перехідного процесу витрати пари при зміні витрати вихідного розчину з 0,6 кг/с до 0,5 кг/с,
3 – графік перехідного процесу виходу регулятора при зміні витрати вихідного розчину з 0,6 кг/с до 0,5 кг/с,
4 – графік перехідного процесу ходу регулюючого органу при зміні витрати вихідного розчину з 0,6 кг/с до 0,5 кг/с,
5 – вікно налаштування параметрів блоку PID-control регулятора концентрації,
6 – графік перехідної характеристики концентрації КОН,
7 – графік перехідного процесу регулятора співвідношення при відпрацюванні уставки концентрації на 40%
Рисунок 6 – Отримані графіки перехідних процесів у результаті моделювання
(анімація: 7 кадрів, 5 циклів повторення, 106 кілобайт)
Висновки
- Розроблено математичну модель процесу випарювання гідроксиду калію на підставі лінеаризованого диференціального рівняння.
- Складена комплексна модель САР. Проведено синтез систем автоматичного регулювання процесів випарювання розчину гідроксиду калію. В якості законів регулювання по каналу управління
концентрація – витрата гріючої пари
обрано ПІД-закон, а по каналувитрата вихідного розчину – витрата гріючої пари
ПІ-закон. Параметри регуляторів були визначені за методом Chien, Hrones і Reswick і автоматично оптимізовані засобами блоку PID-control. Результати моделювання показують працездатність САР і можливість застосування розроблених систем, основними показниками якості яких виступають:
- відсутність статичної помилки;
- час регулювання – близько 20 хв;
- аперіодичний характер перехідних процесів з допустимим перерегулюванням;
- задовільний час відпрацювання збурень;
- компенсація збурень за рахунок обраного принципу управління по відхиленню.
При написанні даного реферату магістерська робота ще не завершена. Остаточне завершення: грудень 2015 року. Повний текст роботи та матеріали по темі можуть бути отримані у автора або його керівника після вказаної дати.
Перелік посилань
- Таубман Е. И. Расчёт и моделирование выпарных установок. – М.: Химия, 1970. – 215 с.
- Попов Н. П. Выпарные аппараты в производстве минеральных удобрений. – Калининград: КГТУ, 1974. – 538 с.
- Кафаров В. В., Макаров В. В. Гибкие автоматизированные системы в химической промышленности: Учебник для вузов. – М.: Химия, 1990. – 320 с.
- Дудников Е. Г. Автоматическое управление в химической промышленности. – М.: Химия, 1987. – 368 с.
- Шувалов В. В. Огаджанов Г. А., Голубятников В. А. Автоматизация производственных процессов в химической промышленности. – М.: Химия, 1991. – 480 с.
- Полоцкий Л. М., Лапшенков Г. И. Автоматизация химических производств. – М.: Химия, 1982. – 295 с.
- Исаев С. И., Кожинов И. А., Кофанов В. И., Леонтьев А. И. Теория процесса выпаривания: Учебник для технических университетов и вузов. / 2-е изд., испр. и доп. – М.: Изд-во МГТУ им. Н. Э. Баумана, 1997. – 683 с.
- Кафаров В. В., Глебов М. Б. Математическое моделирование основных процессов химических производств: Учебн. пособие для вузов. – М.: Высш. шк., 1991. – 400 с.
- Курко В. И. Методы исследования процесса выпаривания химических растворов. – М.: Химическая промышленность, 1977. – 191 с.
- Борисов Г. С., Брыков В. П., Дытнерский Ю. И. Основные процессы и аппараты химической технологии: Пособие по проектированию / Под ред. Дытнерского Ю. И., 2-е изд., перераб. и дополн. – М.: Химия, 1991. – 496 с.
- Дытнерский Ю. И. Процессы и аппараты химической технологии: Учебник для вузов. Изд. 2-е В 2-х кн.. Часть 2. Массообменные процессы и аппараты. – М.: Химия, 1995. – 368 с.: ил.
- Таубман Е. И. Выпаривание. – М., 1982.
- Иоффе И. Л. Проектирование процессов и аппаратов химической промышленности: Учебник для техникумов. – Л.: Химия, 1991. – 352 с.: ил.
- Гельперин Н. И. Основные процессы и аппараты химической технологии. – М.: Химия, 1981. – 812 с.:ил.
- Клюев А. С. Проектирование систем автоматизации технологических процессов: Справочное пособие. Изд. 2-е, перераб. и доп. – М.: Энергоатомиздат, 1990. – 464 с.: ил.
- Плановский А. Н., Николаев П. И. Процессы и аппараты химической и нефтехимической технологии:Учебник для вузов. Изд. 3-е, перераб. и доп. – М.: Химия, 1987. – 496 с.
- Плановский А. Н., Рамм В. М., Каган С. З. Процессы и аппараты химической технологии. Изд. 5-е. – М.: Химия, 1991. – 848 с.
- Гуров А. М., Починкин С. М. Автоматизация технологических процессов. – М.:Высшая школа, 1979. – 355 с.
- Колач Т. А., Радун Д. В. Выпарные станции. – М.: Машгиз, 1963. – 219 с.
- Гельперин Н. И., Пебалк В. Л., Костанян А. Е. Структура потоков и эффективность колонных аппаратов химической промышленности. – М.: Химия, 1977. – 262 с.
