|
Актуальність теми
Як поглиначі вологи з природного газу широке поширення одержали глsколі - етиленгліколь (ЕГ), диетиленгліколь (ДЕГ) і триетиленгліколь (ТЕГ). Усі гліколі мають приблизно однакову здатніст осушувати, і вибір осушувача визначається набіром його інших технологічних властивостей. Однією з таких важливих властивостей є тиск насиченої пари абсорбенту, оскільки воно визначає його втрати у виді пари з осушеним газом. На теперешній час для осушування газу частіше використовують диетиленгліколь, що є набагато менш летучою речовиною, чим етиленгліколь. Триетиленгліколь має ще більш низький тиск насиченої пари при температурах осушування газу і має гарні перспективи в технології осушування. У процесі осушування газу в абсорбент попадають краплі розсолу, які уносяться газм зі шпари. Солі, що утримуються в розсолі, (здебільшого хлорид натрію - близько 90 % від загальної маси солей), у процесі регенерації гликолей від вологи залишаються в них і поступово накопичуються.Насичений солями гліколь непридатний для використання в технологічному процесі осушування газу і його необхідно регенерувати, очищаючи від розчинених солей.При виведенні гліколей із процесу осушування, відбувається забруднення навколишнього середовища солями, які накопичились в гліколі, що попадають із природних газів. Тому розробка методу рекуперації дуже важлива для запобігання забруднення флори і фауни, і тим самим, здоров'я людини.А ще тому що застосування триетиленгліколя на сьогоднішній день стає більш актуальною, то розробка методу регенерації цього осушувача може принести не малу користь.

|
|
Мета й завдання
Ціль роботи - розробка способу рекуперації триетиленгліколя (ТЕГ) за допомогою ацетону.. Для рішення цього питання ставляться наступні задачі:
- аналіз стану питання і вивчення літературних джерел по способах осушування природних газів і механізм технології рекуперації осушувача газу різними способами;
- екологічна значимість розв'язуваної проблеми;
- проведення лабораторного експерименту. Обробка отриманих даних за допомогою пакета MS Excel;
- розробка технології знесолення триетиленгліколя на основі отриманих експериментальних даних.

|
|
Наукова новизна
Ціль роботи - розробка способу рекуперації триетиленгліколя (ТЕГ) за допомогою ацетону.До цього цим питанням мало хто займався. Саме тому воно представляє наукову новизну як для кафедри "Фізичної й органічної хімії", так і для наукового суспільства в цілому. Можливо розроблена нами схема очищування засолоненого ТЕГ від солей ацетоном зацікавить підприємства, що працюють у цій сфері.
|
|

|
|
Практична цінність
Планований практичний результат: розроблений метод очищення триетиленгліколя від солей ацетоном дає можливість майже повного очищення осушувача від солей завдяки високій знесолювальної здатності ацетону.

|
|
Огляд існуючих досліджень
При використанні на газових промислах ДЕГ, як поглинача вологи з газу й інгібітору гідратоутворення, у нього потрапляють солі, що містяться в краплинній волозі, [2]. При регенерації такого ДЕГ від вологи солі відкладаються на теплопередаючих поверхнях, порушуючи нормальну роботу установок. Втрати ДЕГ від засолонення обчислюються сотнями тонн на рік на одному промислі. Особливо інтенсивно процес засолонення ДЕГ протікає при експлуатації газових родовищ, що виснажуються.
Основними компонентами суміші солей, які присутні у ДЕГ є хлориди натрію і кальцію. Зміст хлориду натрію в краплинній волозі досягає 90 % від загального змісту солей [2], а у відкладеннях на жарових трубах випарника до 97 % [3]. Хлориду кальцію набагато менше - у краплинній волозі порядком 10 % [2], у відкладеннях - до 2 %[3]. Великі втрати від засолонення дорогого поглинача обумовлюють пошуки методів і способів усунення їх.
Пошуки рішення проблеми знесолення ДЕГ можуть проводитися в наступних напрямках:
1)виключення влучення краплинної вологи в поглинач;
2)очищування поглинача від розчинених солей.
Перший шлях припускає розробку більш зроблених уловлювачів краплинної вологи і є радикальним.
Другий шлях, тобто очищення ДЕГ від розчинених у ньому солей, може бути принципово здійснений наступними методами:
1)відгоном ДЕГ під вакуумом у вигляді азеотропної суміші;
2)осадженням солей деякими хімічними речовинами;
3)виділення солей шляхом зниження їхньої розчинності;
4)виділення солей з використанням іонообмінних смол і інших іонітів,
5)електролізом і электродіалізом.
Кожний з цих методів має визначені недоліки, що перешкоджують використання зазначених методів для промислового знесолення диетіленгликоля. Наприклад, перегонка ДЕГ повинна здійснюватися при досить глибокому розрядженні -тиск насиченої пари ДЕГ при температурі 437 К складає Па [5] Більш висока температура перегонки неприйнятна через небезпеку розкладання поглинача [6]. Речовин, що утворювали б з ДЕГ азеотропні суміші з низькою температурою кипіння дуже мало і вони малодосягнені [7]. Крім того, очищування ДЕГ шляхом перегонки зв'язані з великою витратою тепла.
Осадження солей хімічними реагентами є перспективним методом очищення, але його можна використовувати тільки для видалення хлориду кальцію
При цьому хлорид натрію, що виходить, залишається в ДЕГ і його сумарна концентрація зростає. Отриманий після осадження іонів кальцію ДЕГ необхідно очищувати від хлориду натрію.
Відомий спосіб очищення, заснований на випарюванні водяних розчинів ДЕГ, що містять солі [2]. При цьому автори вказують, що розчинність хлориду натрію падає зі збільшенням температури і зменшенням змісту води в ДЕГ. Таким чином, при розпарюванні засолоненних водяних розчинів ДЕГ у деяких випадках можна частково звільнитися від розчиненого хлориду натрію. По суті, такий процес протікає в установках регенерації при видаленні вологи з засолоненого ДЕГ. При цьому хлорид натрію випадає на теплопередаючих
поверхнях у вигляді щільного важковидаляємого осаду. Це може призвести до виведення з ладу установки, що осушує. Метод, в основі якого лежать процеси іонного обміну, починає широко використовуватися в промисловості для очищення ДЕГ від солей [3, 8]. Використання цього методу дає можливість глибокого очищувати ДЕГ від солей. Але є ряд недоліків:
- мала швидкість очищення;
- необхідність проведення окремо катіонного й аніонного обміну;
- необхідність регенерації іонітів (іонообмінних смол);
- швидкий вихід іонітів і смол з ладу при очищенні частково розложеного ДЕГ;
- громіздкість установок заважають широкому впровадженню цього методу в промисловість.
Електроліз і електродіаліз як методи очищення поглинача вологи від розчинених солей, мабуть, мало перспективні для використання в промисловості, коли потрібно видаляти солі з концентрованих розчинів.
Той факт, що в даний час немає ще добре розроблених методів видалення солей з ДЕГ, не дозволяє вважати задачу остаточно вирішеною. Необхідно шукати нові методи видалення солей з поглинача. Одним з таких перспективних методів є метод зворотнього висолювання. Розроблено спосіб видалення солей із засолоненого ДЕГ за допомогою бензолу [9]. Процес полягає в додаванні до засолоненого ДЕГ бензолу, нагріванні з перемішуванням отриманої системи до температури 433 К, фільтруванні суспензії хлориду натрію, що утворюється, і видаленні бензолу з регенерованого ДЕГ нагріванням.
Позитивні сторони методу:
1)велика швидкість знесолення і велика продуктивність установки при малих її габаритах;
2)бензол увесь час знаходиться в циклі. Єдиним відходом є твердий хлорид
натрію з домішкою інших солей;
3)сіль виділяється у всьому обсязі розчину і виходить сипучий кристалічний осад;
4)проведення глибокого очищення ДЕГ від солі здійснюється за один прийом (залишкова концентрація солі порядку декількох десятих часток відсотка) незалежно від величини початкової концентрації солі;
5)широке варіювання глибини очищення солі за рахунок зміни температури обробки і кількості бензолу, що додається;
6)можливо спільне дуже ефективне використання цього методу з методами
глибокого зневоднювання ДЕГ.
Але даний метод висалювання за допомогою бензолу має і ряд недоліків:
1)висока температура знесолення (близько 388 - 433 К) і зв'язаною з цим
необхідність проведення процесу під підвищеним тиском;
2)висока токсичність бензолу;
3)невисока ефективність знесолення при низьких температурах (порядку 298К);
4) погана розчинність бензолу в ДЕГ і його водяних розчинах при низьких температурах.
Подальший розвиток методу зворотнього висолювання складається в усуненні цих недоліків, що досягається використанням нетоксичних речовин, що дозволяють при більш низьких температурах і тисках домогтися глибокого знесолення ДЕГ. Встановлено, що гарними высолюючими властивостями володіють органічні рідини, які містять кисень, зокрема , кетони. Серед останніх найбільш кращим є ацетон, що виробляється в промисловості у величезних масштабах. Цей розчинник малотоксичен, летючий, змішується з ДЕГ у будь-яких співвідношеннях.
Видалення солей з диетиленгликоля, як було показано раніше, може бути ефективно здійснене за допомогою методу зворотнього висолювання за допомогою деяких речовин ( бензолу, ацетону,диоксана і інших. ), що добре розчиняються в ДЕГ, але не розчиняють неорганічні солі.
Нами була поставлена задача розробки аналогічного методу очищення ТЕГ з використанням ацетону. Для вирішання цієї задачі необхідна інформація про розчинність хлориду натрію (основного компонента сольової суміші) у двокомпонентних розчинниках ТЕГ - ацетон, ТЕГ - вода, ацетон - вода і трикомпонентний розчинник ТЕГ - ацетон - вода. Необхідність включення води до складу розчинників продиктована тим, що в процесі осушування природного газу вода разом із сіллю знаходиться в рідкій фазі. На першому етапі дослідження ми провели вивчення розчинності в системі хлорид натрію - ТЕГ - ацетон і розчинність хлориду натрію в сумішах ТЕГ - вода при 25 і 40°C.

|
|
Основні результати роботи
1. Підготовка реактивів і основна установка для вивчення розчинності хлориду натрію в ацетонгліколевых і водногліколевых розчинниках:
Підготовка реактивів, необхідних для проведення експерименту, проводилася в такий спосіб. ТЕГ кваліфікації "хч" переганявся при зниженому тиску при температурі 120 °C, і для експерименту відбиралася середня фракція. Показник переломлення очищеного ТЕГ при 20 °C склав 1,4555 (довідкове значення 1,4559). Ацетон кваліфікації "осч" переганявся при атмосферному тиску з добором середньої фракції. Щільність ацетону, що використовувався, 790,6 кг/ м3, показник переломлення при 20 °C - 1,3590, зміст води, визначений по методу Фишера, - 0,03%. Вода бралася у виді бідистиллята. Хлорид натрію кваліфікації "хч" використовувався без додаткового очищення, але попередньо прогрівався до 150 °C для осушування
Установка для вивчення розчинності містила в собі термостатуючу скляна склянку, заповнену водою. Вода інтенсивно перемішувалася пропелерною мішалкою. У склянку вставлявся осередок, що представляє собою ампулу ємністю близько 15 мл, зі звуженням у верхній частині, що щільно закривалося поліетиленовою пробкою. Попередньо в осередок містився кристалічний хлорид натрію, узятий у надлишку, і двухкомпонентный розчинник (ТЕГ - ацетон або ТЕГ - вода) відомого складу. Точні значення мас компонентів розчинника знаходилися шляхом зважування на аналітичних вагах. Вміст осередку перемішувалося за допомогою сталевого стрижня, що обертався при включенні магнітної мішалки.
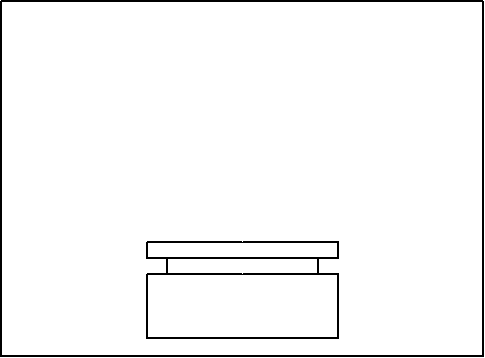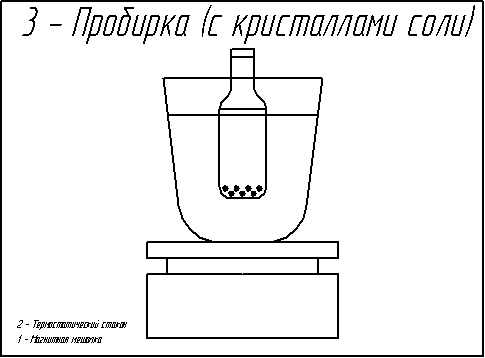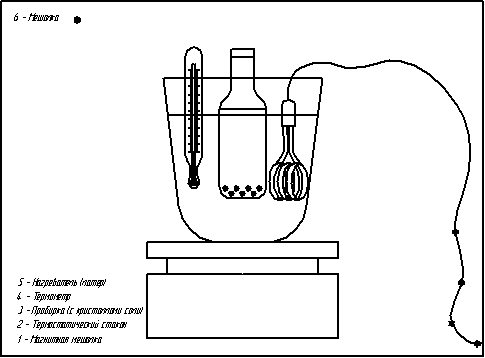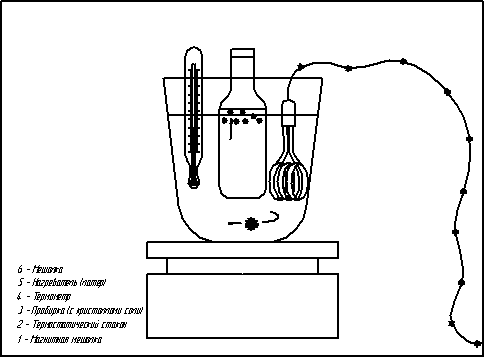
Рисунок 1– Схема установки для проведення експерименту
2. Порядок проведення дослідження:
Вивчення розчинності хлориду натрію в ацетонгліколевых і водногліколевых розчинах полягало в наступному. При постійній температурі проводили інтенсивне перемішування вмісту осередку до досягнення стану рівноваги. Як було встановлено, при температурі 25 °C рівновага встановлюється протягом 15 - 20 хв. Після цього при відключеній магнітній мішалці відбувалося осідання надлишку кристалів солі. За допомогою шприца відбиралася проба насиченого розчину для визначення концентрації хлориду натрію. Проба розчину переносилася в зважену на аналітичних вагах мірну колбу, що після цього знову зважувалася. Потім проба розбавлялася дистильованою водою до обсягу 100 мл. Для титрування бралася аліквотная частина в 20 - 50 мл у залежності від концентрації солі в розчині. Аналіз проводили за методом Мора 0,05 N розчином нітрату срібла з використанням хромата калію як індикатор. Як правило, титрування досліджуваного розчину проводилося двічі
3.Анализ отриманних даних:
Спочатку ми провели вивчення розчинності в системі хлорид натрію - ТЕГ - ацетон при температурі 25 °C.Дані по розчинності хлориду натрію в сумішах ТЕГ - ацетон при температурі 25 °C приведені в таблиці 1.
Таблица.1
| Вміст ТЕГ в розчиннику, % мас. |
100,0 |
81,7 |
60,4 |
38,8 |
23,4 |
0,0 |
| Вміст. ацетона в розчиннику, % мас. |
0,0 |
18,3 |
39,6 |
61,2 |
76,6 |
100,0 |
| Конц. хлорида натрія в нас. р-ні, % мас. |
4,92 |
2,83 |
1,37 |
0,49 |
0,14 |
<0.01 |
Як випливає з приводи експериментальних даних, додавання ацетону до розчинів хлориду натрію в триэтиленгликоле приводить до різкого зменшення розчинності солі і переходові її у тверду фазу, що свідчить про високий высаливающей здатності ацетону.
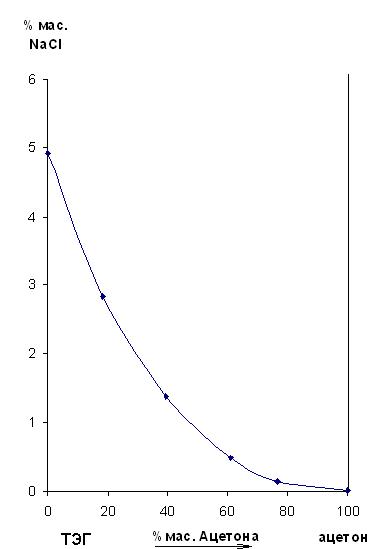
Рисунок 2– Розчинність NaCl у двухкомпонентном розчиннику ТЕГ - ацетон при 25°C
Крім того, була досліджена розчинність хлориду натрію в сумішах триэтиленгликоль - вода при температурах 25 °C і 40 °C. Розчинність хлориду натрію в сумішах триэтиленгликоль - вода різного складу при температурах 25 і 40 °C приведена в таблиці 2.
Таблица.2
| Вміст ТЕГ в розчиннику, % мас. |
100.0 |
78.4 |
60.7 |
44.9 |
0,0 |
| Вміст води в розчиннику, % мас. |
0.0 |
21.6 |
39.3 |
55.1 |
100,0 |
| Конц. хлорида натрія в нас. р-ні, % мас. |
при 25 °C |
4,92 |
7,24 |
11,0 |
14,5 |
26,5 |
| Конц. хлорида натрія в нас. р-ні, % мас. |
при 40 °C |
4,16 |
7,34 |
11,5 |
15,1 |
26,7 |
Характер розчинності хлориду натрію в сумішах триетиленгліколь - вода аналогічна характерові розчинності цієї солі в сумішах диетиленгліколь - вода. З ростом температури концентрація хлориду натрію у водногліколевом розчині з високим змістом води збільшується, а з високим змістом гліколя - падає, так само, як і в чистому гліколі. При цьому, як було встановлено нами, існує двухкомпонентный розчинник, що містить близько 80 % триетиленгліколя, розчинність хлориду натрію в якому не залежить від температури. У цьому розчиннику теплота розчинності хлориду натрію дорівнює нулю. Такий характер розчинності солі в двухкомпонентном розчиннику триетиленгліколь - вода може бути зв'язаний з утворенням іонних пар, частка яких росте при збільшенні змісту триетиленгліколя у розчиннику.
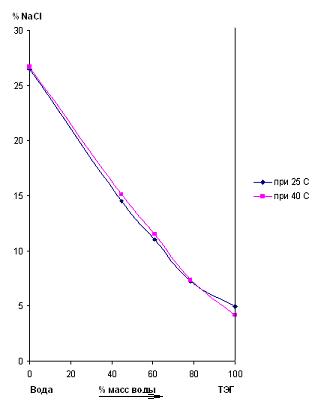
Рисунок 3– Розчинність NaCl у двухкомпонентному розчиннику ТЕГ - вода при 25 °C і 40 °C
На підставі отриманих даних розроблена схема очищення засолоненого ТЕГ від солей за допомогою ацетону з поверненням у цикл останнього і визначені основні технологічні параметри її роботи. Холодний засолоненный ТЕГ проходить теплообмінник 14, де нагрівається гарячим регенерованим ТЕГ до температури 313К и подається насосом 13 у реактор 1.Реактор постачений мішалкою, що приводиться в рух електродвигуном 2 і сорочкою, у яку подається пара. Після завантаження ТЕГ у реактор насосом 12 зі збірника 8 подається рідкий ацетон до потрібного співвідношення. При інтенсивному перемішуванні і нагріванні до температури 363 К и тиску 2,5 * 105 Па в системі відбувається виділення кристалів солі. Отримана суспензія під тиском парів ацетону при відкриванні вентиля 4 (засувки) надходить у фільтр 3 для відділення кристалів NaCl від рідкої фази. У фільтрі при падінні тиску відбувається частковий випар ацетону з розчину. Пари його через вентиль 5, попадають у конденсатор 7, де прохолоджуються і конденсуються за допомогою холодної води. Рідкий ацетон попадає в збірник 8. З цього збірника ацетон насосом 12 може знову подаватися в реактор 1 для видалення солі з ТЕГ. Рідкий знесолений ТЕГ надходить у куб 9, де він нагрівається глухою парою до температури 403 До для відгону ацетону, що залишається, пари якого перетворюються в рідину в конденсаторі 7. Гарячий знесолений ТЕГ насосом 14 подається в теплообмінник 15, де прохолоджується за рахунок передачі тепла холодному засолоненному ТЕГ, і подається потім на осушку природного газу. Для відшкодування втрат ацетону у виді пари і з уходящим регенерованим ТЕГ передбачена подача свіжого ацетону в збірник 8.
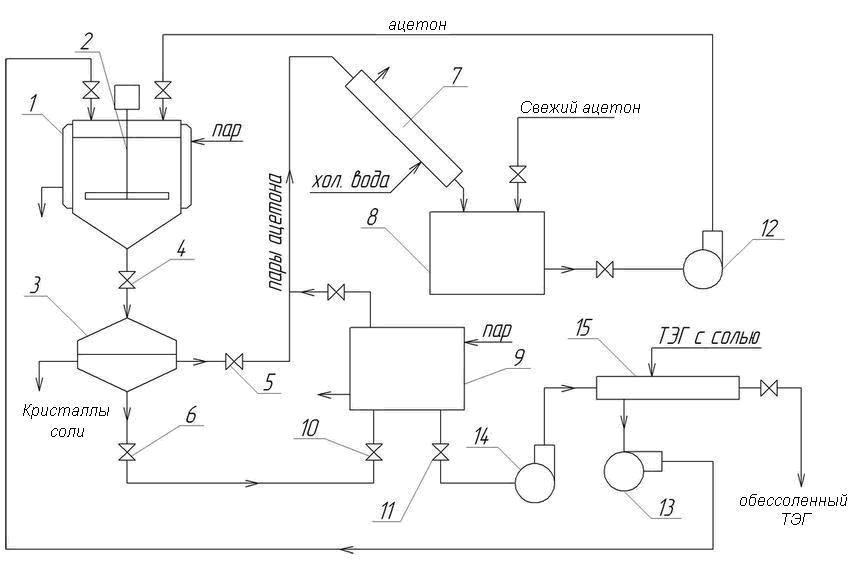
Рисунок 4– Технологічна схема знесолення триэтиленгликоля за допомогою ацетону
4.Плановані дослідження
Звичайно, наявність води в ТЕГ істотно знижує ефективність використання ацетону для видалення хлориду натрію з гліколя. Наскільки велике це зниження повинне показати вивчення розчинності хлориду натрію в трикомпонентному розчиннику ТЕГ - ацетон - вода. Підвищення температури збільшує глибину очищення ТЕГ від солей, тому необхідно також вивчити поводження досліджуваної системи при набагато більш високих температурах, що перевищують нормальну температуру кипіння ацетону. Крім того, такі дані будуть необхідні для розрахунку процесу видалення ацетону з регенерованого від солі ТЭГ.

Висновки
Рішення проблеми очищення поглинача вологи з газу, триетиленгліколя, від солей дуже важливо в екологічному значенні, оскільки при цьому запобігається забруднення навколишнього середовища. З метою розробки способу очищення триэтиленгликоля від солей за допомогою ацетону експериментальним шляхом вивчена розчинність NaCl у двухкомпонентных розчинниках: ТЕГ - ацетон, ТЕГ - вода, ацетон - вода, а також у трикомпонентному розчиннику ТЕГ -ацетон - вода при температурі 298 К. Вивчення розчинності в системі ТЕГ - ацетон - вода -NaCl показує, що хлорид натрію може бути вилучений із засолоненного ТЕГ за допомогою ацетону. При цьому ,як показує експеримент, очищення ТЕГ від солей найбільше ефективно протікає під час відсутності води при підвищеній температурі змішання засолоненного ТЕГ з ацетоном. Останнє доцільно, тому що при наступному відгоні ацетону з регенерованого ТЕГ розчин необхідно нагрівати.На підставі досліджень розроблена технологічна схема очищення ТЕГ від солей за допомогою ацетону. Оцінний розрахунок показує працездатність цієї технологічної схеми й економічну доцільність процесу регенерації ТЕГ від солей за допомогою ацетону. Метод зворотного висалювання хлориду натрію ацетоном може бути покладений в основу ефективного промислового методу знесолення поглинача вологи з природного газу -ТЭГ.

Література
1. Могильный В.И., Клименко А.П., Чалюк Г.И. Исследование растворимости хлористого натрия и кальция в диэтиленгликоле. // Химическая технология. - 1972. -
№ 1.-С. 42-61.
2. Бондарь А. Д., Грибкова В.И., Моисеева Н.Ф. Опыты по обессоливанию диэтиленгликоля. // Газовое дело. - 1970. - № 2. - С. 43 - 45.
3. Способ очистки диэтиленгликоля от солей, выносимых из скважин с пластовой водой на групповых пунктах низкотемпературной сепарации газа: Отчет НТО НТП Шебелинского газопромыслового упр. имени 50-летия Октября; Руководитель
Будынко В.Ф. - Пос. Червоный Донец, 1970. - 90 с: ил.
4. Жданов Н.В, Халиф АЛ. Осушка природных газов. - М.: Недра, 1975. - 160 с.
5. Справочник химика, т. 1. —Л,: Химия, 1964. - 1168 с.
6. Дымент О.Н., Казанский КС, Мирошников A.M. Гликоли и другие производные
окисей этилена и пропилена. - М.: Химия, 1976. - 376 с.
7. Равновесие между жидкостью и паром. Справочник / Под ред. В.Б.Когана. - Л.: Химия, 1971. -1123 с.
8 Соловьев СИ., Михельман А.И., Червоненко А Г. Очистка диэтиленгликоля от ионов натрия, калия и кальция при помощи катеонитов // Известия высших учебных заведений. Нефть и газ. - 1971. - № 10. - С. 57 - 59.
9. Матвиенко В.Г., Ярым-Агаев Н.Л. Очистка ДЭГ от растворенных солей бензолом. //
Газовая промышленность. - 1988. - № 1. - С 52 - 53.
10. Лабораторные исследования процесса осушки природного газа абсорбентами-смесями
диэтиленгликоля с у - бутиролактоном и N - метилпирролидоном, определение
способов их регенерации и способа обессоливания водных растворов
диэтиленгликоля: Отчет по теме Х-75-132; Руководитель Н.Л Ярым-Агаев.- №
ГР75042657; Инв. № Б 495 897. - Донецк, 1975. - 175 с: ил.
11. Коробчанский И.Е.Э Кузнецов М.Д. Расчеты аппаратуры для улавливания химических
продуктов коксования. - М.: Металлургия, 1972. - 296 с.
12. Захаров Л.Н. Техника безопасности в химических лабораториях. - Л.: Химия, 1991. -
336 с.
13. Макаров Г.В., Васин А.Я. Охрана труда в химической промышленности, - М.: Химия,
1989.-496 с.
14. СНиП 11-4 - 79. Естественное и искусственное освещение. Нормы проектирования. -
М.: Стройиздат, 1980. -48 с.

ДонНТУ> Портал магістрів ДонНТУ> Біографія
| Електронна бібліотека
| Посилання
|
Звіт з пошуку | Індивідуальне
завдання
| |
![]()
![]()





