Реферат по теме выпускной работы
Содержание
- Введение
- 1. Актуальность, цель и задачи исследования
- 2. Общая характеристика глин
- 3. Физико–химические основы процесса адсорбции
- 4. Экспериментальная часть
- Выводы
- Список источников
Введение
Среди большого числа факторов, формирующих здоровье человека, важную роль играют факторы окружающей среды. Промышленная деятельность человека привела к загрязнению водоемов вредными веществами: металлами в ионной форме, нефтепродуктами, токсическими синтетическими веществами и другими загрязнителями [1].
Из всех специальных методов очистки вод адсорбционные методы являются наиболее простыми, менее дорогостоящими, доступными и эффективными [2].
Адсорбционные процессы с использованием природных минеральных сорбентов всё больше находят применение в связи с возможностью их использования в процессах водоочистки вследствие их низкой стоимости и в то же время достаточной сорбционной емкостью. Обзор периодических изданий по сорбционным процессам на природных минералах показал, что данные процессы изучены слабо, и это направление требует более детального исследования. Кроме того, использование в течение длительного времени классических технологий водоочистки, привело к росту объемов еще больше загрязнений гидросферы, что требует новых стратегий и технологий в очистке сточных вод вод [3].
1. Актуальность, цель и задачи исследования
При очистке вод сорбционными методами как адсорбент используют активированный уголь. Целесообразно и рационально заменить его на природные сорбенты, которые с одной стороны являются недорогими и доступными материалами, а с другой – позволяют достичь достаточной степени очистки. Использование таких сорбентов обусловлено относительно высокой емкостью, избирательностью, катионообменными свойствами некоторых из них, сравнительно низкой стоимостью и доступностью. Актуальным является использование природных сорбентов — глин
Целью работы является исследование сорбционных свойств некоторых глин Донбасса. Для этого было выбрано шесть образцов глин различных месторождений: суглинок (месторождение Белая Балка), два образца глины, которые отличаются содержанием алюминия, с Часовьярського месторождения, глина Луганского месторождения и два образца глин с Константиновского месторождения, которые отличаются содержанием титана и железа.
Для достижения цели поставлены следующие задачи:
– изучить химический состав исследуемых глин;
– исследовать экспериментально сорбционную активность глин по стандартным методикам в отношении красителей и определение йодного числа;
– построить изотермы адсорбции;
–определить сорбционные свойства глин относительно различных загрязнителей.
2. Общая характеристика глин
Глинистые породы – наиболее распространенные неорганические сорбенты для очистки воды. Они имеют развитую структуру с микропорами, которые имеют различные размеры в зависимости от вида материала. Механизм сорбции загрязнений из воды на глинистых минералах достаточно сложен и включает вандерваальсовое взаимодействие углеводородных цепочек с развитой поверхностью микрокристаллов силикатов и кулоновское взаимодействие заряженных и поляризованных молекул сорбата с положительно заряженными участками поверхности сорбента, содержащими ионы Н + и Аl 3+
Выделяют следующие причины высокой поглощающей способности глинистых материалов:
– нарушение связей на краях алюмокремниевых групп, вызывающих увеличение числа нескомпенсованных зарядов, которые уравновешиваются адсорбированными катионами;
– замещение внутри структуры четырехвалентного кремния в тетраэдрических слоях алюминием и трехвалентного алюминия в октаэдрических слоях катионами низшей валентности, обычно магнием, что вызывает появление нескомпенсированных зарядов в структурной ячейки некоторых глинистых минералов;
– замещение водорода внешнего гидроксила на катионы [6].
Обменные свойства глинистых минералов не могут быть обусловлены только одной из рассмотренных причин, они являются следствием всех трех.
Добавление глинистых минералов–адсорбентов в процессе очистки сточных и загрязненных природных вод на стадии отстаивания не только позволит избавиться от опасных антропогенных загрязняющих примесей путем адсорбции без химических реактивов, но и улучшить структуру и минерализацию воды [7];
Преимуществами применения таких адсорбционных материалов являются следующие:
–природные сорбенты широко распространены в Украине [7];
– природные сорбенты доступны, являются недорогим материалом [7];
– не разрушается структура сорбента (по сравнению с полимерными, синтетическими сорбентами) при взаимодействии с нефтепродуктами;
– широкий спектр сорбируемых веществ (нефтепродукты, тяжелые металлы, пестициды, радионуклиды) [3];
– в отличие от синтетических, поролоновых, нетканых сорбентов, глины не горят [3];
– работоспособен в широком интервале температур от -20 до + 100 0С
–адсорбционные технологии по использованию природных дисперсных сорбентов обеспечивают достаточную степень очистки
– адсорбционные технологии по использованию природных дисперсных сорбентов обеспечивают достаточную степень очистки [7];
Таким образом, глины месторождений Донбасса целесообразно использовать как адсорбент для извлечения из природных и сточных вод различных загрязнителей.
3. Физико–химические основы процесса адсорбции
Адсорбционная очистки сточных вод широко используется на предприятиях различных отраслей промышленности. Это один из эффективных способов глубокой очистки природных и сточных вод от веществ органического происхождения, тяжелых металлов, нефтепродуктов.
Сорбция эффективна для обесцвечивания и устранения запахов и привкусов из природных вод. Абсорбцию можно применять для очистки сточных вод от фенолов, гербицидов, пестицидов, ароматических нитросоединений, поверхностно-активных веществ, красителей и других растворенных веществ, содержащихся в сточных водах.
Преимуществом метода является высокая эффективность, возможность очистки сточных вод, содержащих несколько загрязняющих веществ, а также рекуперация этих веществ. Эффективность сорбционной очистки составляет 80–95 % и зависит от химической природы сорбента, величины адсорбционной поверхности и ее доступности, от химической природы загрязнителя и его состояния в растворе [4].
Основные сведения о сорбционных свойствах материала и характер адсорбции на нем определенных веществ могут быть получены из изотерм адсорбции, характеризующие зависимость сорбционной способности от концентрации (или давления) компонента, сорбируемого, при постоянной температуре. Брунауэр, Эммет и Теллер [8] выделили пять основных типов изотерм адсорбции, так называемых изотерм по БЭТ (рисунок 3.1). Выпуклые участки изотерм I, II и IV типов указывают на наличие в сорбентах микропор, но, кроме того, сорбенты II и IV имеют еще и макропоры. Изотермы III и V типов встречаются реже и описывают сильное межмолекулярное взаимодействие в веществе сорбата. Крутизна изотермы I типа характеризует размер микропор сорбентов: а – ультрамикропористых, б – микропористых.

Рисунок 3.1—Типы изотерм адсорбции по БЭТ
Для аналитического описания изотермы мономолекулярной адсорбции используют уравнение Ленгмюра:
А = Апред · С / (1 + кС),
где А – удельная адсорбция, ммоль/г;
Апред – предельная адсорбция, ммоль/г;
С – равновесная концентрация адсорбата, ммоль/дм3;
к – адсорбционная константа.
Графическое выражение этого уравнения приведенo на рисунке 3.3. На изотерме можно выделить три характерных участка. Начальная линия имеет прямолинейный участок, указывающая на то, что при малых концентрациях величина удельной адсорбционной способности прямо пропорциональна этим концентрациям. Это, в значительной степени, отвечает еще свободной поверхности адсорбента.

Рисунок 3.3 — Изотерма адсорбции Ленгмюра
Почти горизонтальный участок, который отвечает большим концентрациям, соответствует поверхности адсорбента, полностью насыщенным адсорбтивом. Размер удельной адсорбционной способности в этом случае не зависит от равновесной концентрации адсорбтива в растворе, что свидетельствует об образовании на поверхности мономолекулярного слоя. Средний участок изотермы соответствует промежуточным степеням заполнения поверхности. Уравнение Ленгмюра описывает изотерму адсорбции во всех областях равновесных концентраций. При малых концентрациях формула упрощается приобретает вид:
А = Апред · кС,
В области промежуточных равновесных концентраций (на небольших участках изменения концентрации адсорбата) зависимость адсорбции от концентрации часто может быть описана уравнением Фрейндлиха, в основе которого лежит предположение, что изотерма адсорбции является параболой:
А = к · С1/n,
где к и 1/n - константы.
В логарифмическом виде уравнения Фрейндлиха представляется прямой (рисунок 3.4):

Рисунок 3.4 – Изотерма адсорбции Фрейндлиха
Таким образом, адсорбция является сложным гетерогенным процессом, эффективность которого зависит от многих факторов.
4. Экспериментальная часть
Для исследования были выбраны глины, химический состав которых приведен в таблице 4.1.
Таблица 4.1 — Химический состав глин
|
Месторождение |
|
|||||
|
Al2O3 |
Fe2O3 |
TiO2 |
CaO |
SiO2 |
ППП |
|
|
Суглинок (Белая Балка) |
18,0 |
2,5 |
1,5 |
0,4 |
65,0 |
7,3 |
|
Часов-Ярское, II сорт |
22,13 |
1,94 |
0,81 |
0,75 |
63,75 |
7,5 |
|
Луганское |
21,6 |
1,0 |
21,6 |
0,4 |
67,4 |
6,65 |
|
Часов-Ярское |
32,17 |
1,31 |
0,84 |
0,94 |
53,66 |
9,56 |
|
Костантиновское |
32,30 |
1,04 |
1,11 |
0,50 |
51,9 |
9,79 |
|
19,09 |
0,67 |
1,76 |
0,56 |
63,7 |
4,69 |
Для подтверждения возможности использования глин в качестве сорбента, были проведены их испытания по стандартным методикам [9-10].
Сорбционная активность может быть определена на основе йодного числа, определение которого основано на измерении начальной и остаточной концентрации йода в исходном растворе и после адсорбции титриметрическим методом.
Для этого навески глин фракцией 1 мм и массой 1,00 г помещали в конические колбы емкостью 250 см3, добавляли туда по 100 см3 0,1 Н раствора йода в йодиде калия. Затем отделяли глину от раствора и определяли начальную и остаточную концентрацию йода в исходном растворе и растворе после адсорбции титрометрическим методом. Обработку результатов проводили по формуле, %:

где V1 – объём раствора тиосульфата натрия (0,1 н), который пошёл на титрование 10 см3 раствора йода в йодистом калии, см3;
V2 – объём раствора тиосульфата натрия (0,1 н), который пошёл на титрование 10 см3 раствора йода в йодистом калии, после обработки его глиной, см3;
0,0127 – масса йода, которая соответствует 1 см3 раствора тиосульфата натрия, г;
100 – объём раствора йода в йодистом калии, который брали на осветление глиной, см3;
m – масса навески глины, 1,00 г.
Результаты расчета приведены в таблице 4.2.

Рисунок 3.5 — Определение адсорбционной активности по йодному числу
(анимация: 2 кадрa, 7 повторений, 154 килобайтa)
Таблица 4.2 — Результаты расчета
|
Название сорбента |
Йодное число, |
|
Суглинок (Белая Балка) |
12,7 |
|
Часов-Ярское месторождение, ІІ сорт |
38,1 |
|
Луганское месторождение |
31,8 |
|
Часов-Ярское месторождениее |
57,2 |
|
Костантиновское месторождение |
38,1 |
|
38,1 |
Важной характеристикой сорбентов является определение адсорбционной активности по красителям. Согласно [10] определяли адсорбционную активность относительно метиленового синего, метилового оранжевого и метилового красного.
Для этого навеску угля массой 0,30 г помещали в коническую колбу ёмкостью 100 см3, добавляли 25 см3 раствора красителя. После этого определяли оптическую плотность на фотоэлектроколориметре с синим светофильтром и длиной волны 400 нм в кюветах, с расстоянием между рабочими гранями 10 мм.
В качестве контрольного раствора использовали дистиллированную воду. По полученным оптическим плотностям на основании градуировочного графика определяли остаточную концентрацию красителя.
Адсорбционную активность рассчитывали по формуле:
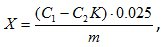
де С1 – концентрация исходного раствора красителя, мг/дм3;
С2 – концентрация раствора красителя после контакта с глиной, мг/дм3;
К – коэффициент разбавления;
m – масса навески глины, г;
0,025 – объём раствора красителя, участвующий в исследовании, дм3.
Результаты исследования адсорбционной ёмкости приведены в таблицах 4.3-4.5.
Таблица 4.3 — Экспериментальные данные определения концентрации метилового оранжевого в растворе
| Название сорбента | Исходная концентрация, Сисх, мг / дм3 | Навеска глины m, г | Остаточная концентрация, Сисх, мг / дм3 | Адсорбционная емкость Г, мг/г |
| Суглинок (Белая Балка) | 1500 | 0,30 | 2,1 | 108 |
| Часов-Ярское месторождение, II сорт | 1500 | 0,30 | 2,1 | 108 |
| Луганское месторождение | 1500 | 0,30 | 2,4 | 105 |
| Часов-Ярское месторождение | 1500 | 0,30 | 2 | 108 |
| Костантиновское месторождение | 1500 | 0,30 | 3,5 | 96 |
| Костантиновское месторождение | 1500 | 0,30 | 3,3 | 98 |
Таблица 4.4 — Экспериментальные данные определения концентрации метиленового голубого в растворе
| Название сорбента | Исходная концентрация, Сисх, мг / дм3 | Навеска глины m, г | Остаточная концентрация, Сисх, мг / дм3 | Адсорбционная емкость Г, мг/г |
| Суглинок (Белая Балка) | 1500 | 0,30 | 0,6 | 125 |
| Часов-Ярское месторождение, II сорт | 1500 | 0,30 | 0,8 | 124 |
| Луганское месторождение | 1500 | 0,30 | 2,4 | 123 |
| Часов-Ярское месторождение | 1500 | 1,2 | 2 | 114 |
| Костантиновское месторождение | 1500 | 0,30 | 1,5 | 124 |
| Костантиновское месторождение | 1500 | 0,30 | 1,7 | 124 |
Таблица 4.5 — Экспериментальные данные определения концентрации метилового красного в растворе
| Название сорбента | Исходная концентрация, Сисх, мг / дм3 | Навеска глины m, г | Остаточная концентрация, Сисх, мг / дм3 | Адсорбционная емкость Г, мг/г |
| Суглинок (Белая Балка) | 1500 | 0,30 | 3,8 | 93 |
| Часов-Ярское месторождение, II сорт | 1500 | 0,30 | 3,2 | 98 |
| Луганское месторождение | 1500 | 0,30 | 3,3 | 98 |
| Часов-Ярское месторождение | 1500 | 3,2 | 2 | 98 |
| Костантиновское месторождение | 1500 | 4,3 | 1,5 | 89 |
| Костантиновское месторождение | 1500 | 0,30 | 3,3 | 98 |
Выводы
При выполнении магистерской работы было сделано следующее:
1. Рассмотрено общую характеристику глин.
2.Рассмотрены физико-химические основы процесса адсорбции, приведены основные уравнения, оценены факторы, влияющие на процесс адсорбции.
3. Экспериментально определено йодное число глин. Йодное число отличается в значительных пределах, что обусловлено различным механизмом сорбции на глинах и углях.
4. Экспериментально изучены сорбционные свойства глин по отношению к красителям. Как свидетельствуют результаты исследований, все образцы глин проявляют сорбционные свойства. Величина сорбционной емкости глин составляет 50–60 % от аналогичной величины для активных углей.
В дальнейшем планируется оценить механизм абсорбции на глинах на основании изучения изотерм адсорбции для красителей, а также изучить адсорбционные свойства глин по отношению к загрязнителям различной природы (ионы тяжелых металлов, органические соединения и другие).
Перечень ссылок
- Везенцев, А.И. Адсорбционные свойства продуктов обогащения природных монтмориллонитсодержащих глин // А.И. Везенцев. – Белгород: Белгородский государственный национальный исследовательский университет, 2011. – С. 103-108
- Івченко, В.Д. Очищення стічних вод від іонів амонію та феруму глинистими мінералами Сумської області: Автореф. канд. техн. наук: 21.06.01 / Сумський національний аграрний університет – С., 2012. – 35 с.
- Ланець, Г. І. Дослідження адсорбційних властивостей глин родовищ Донбасу / О.А. Трошина, Г.І. Ланець // Матерiали XXIV Всеукраїнської наукової конференцiї аспірантів і студентів. – Т.1 – Донецьк: ДонНТУ, 2014. – С. 92 – 94
- Ланець, Г. І. Адсорбційні властивості глин родовищ Донбасу / О.А. Трошина, Г.І. Ланець // Матерiали ХХII Міжнародної науково-технічної конференцiї. – Харків: ХГТУСА, 2014. – С. 71
- Запольський, А.К. Водопостачання, водовідведення та якість води: Підручник / А. К. Запольський. – К.: Вища школа, 2005. – 671 с.
- Тарасевич, Ю.И., Овчаренко, Ф.Д. Адсорбция на глинистых минералах / Ю.И. Тарасевич, Ф.Д. Овчаренко. – К.: Наукова думка, 1975. – 340 с.
- Смирнов, А.Д. Сорбционная очистка воды / А.Д. Смирнов. – Л.: Химия, 1982. – 168 с.
- Фізико-хімічні основи технології очищення стічних вод / За редакцією А.К. Запольського. - Київ: Лібра, 2000. – 549 с.
- ГОСТ 6217 – 74. Уголь активный древесный дробленый. – М.: Государственный комитет стандартов, 1974. – 6 с.
- ГОСТ 4453 – 74. Уголь активный осветляющий древесный порошкообразный. Технические условия. М.: Государственный комитет стандартов, 1974. –11 с.








