Реферат за темою випускної роботи
Зміст
- Вступ
- 1. Актуальність, мета і завдання дослідження
- 2. Загальна характеристика глин
- 3. Фізіко-хімічні основи процесу адсорбції
- 4. Експериментальна частина
- Висновки
- Перелік посилань
Вступ
Серед великого числа факторів, що формують здоров'я людини, важливу роль відіграють фактори навколишнього середовища. Промислова діяльність людини призвела до забруднення водойм шкідливими речовинами: металами в іонної формі, нафтопродуктами, токсичними синтетичними речовинами та іншими забруднювачами [1].
З усіх спеціальних методів очищення вод адсорбційні методи є найбільш простими, недорогими, доступними та ефективними [2]. Адсорбційні процеси з використанням природних мінеральних сорбентів все більше знаходять застосування у зв'язку з можливістю їх використання в процесах водоочищення внаслідок їх низької вартості і в той же час достатньої сорбційної ємності. Огляд періодичних видань щодо сорбційних процесів на природних мінералах показав, що дані процеси мало вивчені, і цей напрямок потребує більш детального дослідження.
Так само, використання протягом тривалого часу класичних технологій водоочищення призвело до зростання обсягів ще більших забруднень гідросфери, що вимагає нових стратегій і технологій в очищенні стічних вод [3].
1. Актуальність, мета і завдання дослідження
При очищенні вод сорбційними методами як адсорбент використовують активоване вугілля. Доцільно і раціонально замінити його на природні сорбенти, які з одного боку, є недорогими і доступними матеріалами, а з іншого – дозволяють досягти достатнього ступеня очищення. Використання таких сорбентів обумовлено відносно високою ємністю, вибірковістю, катіонообмінними властивостями деяких з них, порівняно з низькою вартістю і доступністю. Актуальним є використання природних сорбентів — глин [1].
Метою роботи є дослідження сорбційних властивостей деяких глин Донбасу. Для цього було обрано шість зразків глин різних родовищ: суглинок (родовище Біла Балка), два зразки глини, які відрізняються вмістом алюмінію, з Часов’ярського родовища, глина Луганського родовища і два зразка глин з Костянтинівського родовища, які відрізняються вмістом титану і заліза.
Для досягнення мети поставлені такі завдання:
– вивчити хімічний склад досліджуваних глин;
– дослідити експериментально сорбційну активність глин за стандартними методиками щодо барвників та визначення йодного числа;
– побудувати ізотерми адсорбції;
– визначити сорбційні властивості глин щодо інших забруднювачей.
2. Загальна характеристика глин
Глинисті породи – найбільш поширені неорганічні сорбенти для очищення води. Вони мають розвинену структуру з мікропорами, які мають різні розміри залежно від виду матеріалу. Механізм сорбції забруднень з води на глинистих мінералах досить складний і включає вандерваальсову взаємодію вуглеводневих ланцюжків з розвиненою поверхнею мікрокристалів силікатів і кулонівську взаємодію заряджених і поляризованих молекул сорбата з позитивно зарядженими ділянками поверхні сорбенту, що містять іони Н + і Аl 3+ [4].
Виділяють такі причини високої поглинаючої здатності глинистих матеріалів:
– порушення зв'язків на краях алюмокремнієвих груп, що викликають збільшення числа незкомпенсованних зарядів, які врівноважуються адсорбованими катіонами;
– заміщення всередині структури чотирьохвалентного кремнію в тетраедричних шарах алюмінієм і тривалентного алюмінію в октаедричних шарах катіонами нижчої валентності, зазвичай магнієм, що викликає появу незкомпенсованих зарядів у структурному осередку деяких глинистих мінералів;
Обмінні властивості глинистих мінералів не можуть бути обумовлені тільки однією з розглянутих причин, вони є наслідком всіх трьох.Додавання глинистих мінералів-адсорбентів у процесі очищення стічних і забруднених природних вод на стадії відстоювання не тільки дозволить позбутися небезпечних антропогенних забруднюючих домішок шляхом адсорбції без хімічних реактивів, але і поліпшити структуру і мінералізацію води [6].
Перевагами застосування таких адсорбційних матеріалів є наступні:
– природні сорбенти широко поширені в Україні [7];
– природні сорбенти доступні, є недорогим матеріалом [7];
– не руйнується структура сорбенту (порівняно з полімерними, синтетичними сорбентами) при взаємодії з нафтопродуктами;
– широкий спектр сорбуючих речовин (нафтопродукти, важкі метали, пестициди, радіонукліди) [3];
– на відміну від синтетичних, поролонових, нетканих сорбентів, глини не горять[3];
– працездатний в широкому інтервалі температур від -20 до + 100 0С.
– адсорбційні технології з використання природних дисперсних сорбентів забезпечують достатню ступінь очищення[7];
Таким чином, глини родовищ Донбасу доцільно використовувати як адсорбент для вилучення з природних і стічних вод різних забруднювачів.
3.Фізико—хімічні основи процесу адсорбції
Адсорбційне очищення стічних вод широко використовується на підприємствах різних галузей промисловості. Це один з ефективних способів глибокого очищення природних і стічних вод від речовин органічного походження, важких металів, нафтопродуктів.
Сорбція ефективна для знебарвлення та усунення запахів і присмаків з природних вод. Адсорбцію можна застосовувати для очищення стічних вод від фенолів, гербіцидів, пестицидів, ароматичних нітросполук, поверхнево-активних речовин, барвників та інших розчинених речовин, що містяться в стічних водах.
Перевагою методу є висока ефективність, можливість очищення стічних вод, що містять кілька забруднюючих речовин, а також рекуперація цих речовин. Ефективність сорбційного очищення становить 80–95 % і залежить від хімічної природи сорбенту, величини адсорбційної поверхні і її доступності, від хімічної природи забруднювача і його стану в розчині [4].
Основні відомості про сорбційні властивості матеріалу і характер адсорбції на ньому певних речовин можуть бути отримані з ізотерм адсорбції, що характеризують залежність сорбційної здатності від концентрації (або тиску) компонента, який сорбується, при постійній температурі. Брунауер, Еммет і Теллер [8] виділили п'ять основних типів ізотерм адсорбції, так званих ізотерм по БЕТ (рисунок 3.1). Опуклі ділянки ізотерм I, II і IV типів вказують на наявність в сорбентах мікропор, але, крім того, сорбенти II і IV мають ще й макропори. Ізотерми III і V типів зустрічаються рідше і описують сильні міжмолекулярні взаємодії в речовині сорбата. Крутизна ізотерми I типу характеризує розмір мікропор сорбентів: а – ультрамікропорістих, б – мікропористих.

Рисунок 3.1 — Типи ізотерм адсорбції по БЕТ
Для аналітичного опису ізотерми мономолекулярної адсорбції використовують рівняння Ленгмюра:
А = Апред · С / (1 + кС),
де А – питома адсорбція, ммоль/г;
Апред – гранична адсорбція, ммоль/г;
С – рівноважна концентрація адсорбата, ммоль/дм3;
к – адсорбційна константа.
Графічне вираження цього рівняння приведенo на рисунку 3.3. На ізотермі можна виділити три характерних ділянки. Початкова лінія має прямолінійну ділянку, яка вказує на те, що при малих концентраціях величина питомої адсорбційної здатності прямо пропорційна цим концентраціям. Це, значною мірою, відповідає ще вільнії поверхні адсорбенту.

Рисунок 3.3 — Ізотерма адсорбції Ленгмюра
Майже горизонтальна ділянка, яка відповідає великим концентраціям, відповідає поверхні адсорбенту, повністю насиченим адсорбтивом. Розмір питомої адсорбційної здатності в цьому випадку не залежить від рівноважної концентрації адсорбтива в розчині, що свідчить про утворення на поверхні мономолекулярного шару. Середня ділянка ізотерми відповідає проміжним ступеням заповнення поверхні. Рівняння Ленгмюра описує ізотерму адсорбції у всіх областях рівноважних концентрацій. При малих концентраціях формула спрощується і набуває вигляду:
А = Апред · кС,
В області проміжних рівноважних концентрацій (на невеликих ділянках зміни концентрації адсорбата) залежність адсорбції від концентрації часто може бути описана рівнянням Фрейндліха, в основі якого лежить припущення, що ізотерма адсорбції є параболою:
А = к · С1/n,
де к и 1/n - константи.
У логарифмічному вигляді рівняння Фрейндліха має вигляд прямої (рисунок 3.4):

Рисунок 3.4 — Ізотерма адсорбції Фрейндліха
Таким чином, адсорбція є складним гетерогенним процесом, ефективність якого залежить від багатьох факторів.
4. Експериментальна частина
Для дослідження були обрані глини, хімічний склад яких наведено в таблиці 4.1.
Таблиця 4.1 — Хімічний склад глин
|
Родовище |
|
|||||
|
Al2O3 |
Fe2O3 |
TiO2 |
CaO |
SiO2 |
ВПП |
|
|
Суглинок (Біла Балка) |
18,0 |
2,5 |
1,5 |
0,4 |
65,0 |
7,3 |
|
Часов’ярське II сорт |
22,13 |
1,94 |
0,81 |
0,75 |
63,75 |
7,5 |
|
Луганське |
21,6 |
1,0 |
21,6 |
0,4 |
67,4 |
6,65 |
|
Часов’ярське |
32,17 |
1,31 |
0,84 |
0,94 |
53,66 |
9,56 |
|
Костянтинівське |
32,30 |
1,04 |
1,11 |
0,50 |
51,9 |
9,79 |
|
19,09 |
0,67 |
1,76 |
0,56 |
63,7 |
4,69 |
|
Для підтвердження можливості використання глин в якості сорбенту, були проведені їх випробування за стандартними методиками [9-10].
Сорбційна активність може бути оцінена на основі йодного числа, визначення якого засновано на визначенні початкової та залишкової концентрації йоду у вихідному розчині і після адсорбції титрометричним методом.
Для цього наважки глин фракцією 1 мм і масою 1,00 г поміщали в конічні колби ємністю 250 см3, додавали туди по 100 см3 0,1 Н розчину йоду в йодиді калію. Потім відокремлювали глину від розчину і визначали початкову та залишкову концентрацію йоду у вихідному розчині і розчині після адсорбції титрометричним методом. Обробку результатів проводили за формулою , %:

де V1 – об'єм розчину тіосульфату натрію (0,1 Н), який пішов на титрування 10 см3 розчину йоду в йодиді калію, см3;
V2 – об'єм розчину тіосульфату натрію (0,1 Н), який пішов на титрування 10 см3 розчину йоду в йодиді калію, після обробки його глиною, см3;
0,0127 – маса йоду, яка відповідає 1 см3 розчину тіосульфату натрію, г;
100 – об'єм розчину йоду в йодиді калію, який брали на прояснення глиною, см3;
m – маса наважки глини, 1,00 г.
Результати розрахунку наведені в таблиці 4.2.

Рисунок 3.5 — Визначення адсорбційної активності на основі йодного числа
(анімація: 2 кадрa, 7 повторень, 154 килобайтa)
Таблиця 4.2 — Результати розрахунку
|
Назва сорбенту |
Йодне число, % |
|
Суглинок (Біла Балка) |
12,7 |
|
Часов’рське родовище, II сорт |
38,1 |
|
Луганське родовище |
31,8 |
|
Часов’ярське родовище |
57,2 |
|
Костянтинівське родовище |
38,1 |
|
38,1 |
Важливою характеристикою сорбентів є визначення адсорбційної активності за барвниками. Згідно [10] визначали адсорбційну активність щодо метиленового синього, метилового оранжевого і метилового червоного.
Для цього наважки глин фракцією 1 мм і масою 0,30 г поміщали в конічну колбу ємністю 100 см3, додавали 25 см3 розчину барвника. Після цього визначали оптичну густину на фотоелектроколориметрі з синім світлофільтром і довжиною хвилі 400 нм в кюветах з відстанню між робочими гранями 10 мм.
В якості контрольного розчину використовували дистильовану воду. За отриманою оптичною густиною на підставі градуювального графіка визначали залишкову концентрацію барвника.
Адсорбційну активність розраховували за формулою:
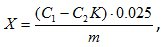
де С1 – концентрація вихідного розчину барвника, мг/дм3;
С2 – концентрація розчину барвника після контакту з глиною, мг/дм3;
К – коефіцієнт розбавлення;
m – маса наважки глин, г;
0,025 – об'єм розчину барвника, який бере участь у дослідженні, дм3.
Результати дослідження адсорбційної ємності наведені в таблицях 4.3-4.5
Таблиця 4.3 — Результати розрахунків адсорбційної ємності за метиловим оранжевим у розчині
| Назва сорбенту | Вхідна концентрація, Свх, мг / дм3 | Наважка глини m, г | Залишкова концентрація, Сзал, мг / дм3 | Адсорбційна ємність Г, мг/г |
| Суглинок (Біла Балка) | 1500 | 0,30 | 2,1 | 108 |
| Часов'ярське родовище, II сорт | 1500 | 0,30 | 2,1 | 108 |
| Луганське родовище | 1500 | 0,30 | 2,4 | 105 |
| Часов'ярське родовище | 1500 | 1,2 | 2 | 108 |
| Костантинівське родовище | 1500 | 4,3 | 3,5 | 96 |
| Костантинівське родовище | 1500 | 0,30 | 3,3 | 98 |
Таблиця 4.4 — Результати розрахунків адсорбційної ємності за метиленовим блакитним у розчині
| Назва сорбенту | Вхідна концентрація, Свх, мг / дм3 | Наважка глини m, г | Залишкова концентрація, Сзал, мг / дм3 | Адсорбційна ємність Г, мг/г |
| Суглинок (Біла Балка) | 1500 | 0,30 | 0,6 | 125 |
| Часов'ярське родовище, II сорт | 1500 | 0,30 | 0,8 | 124 |
| Луганське родовище | 1500 | 0,30 | 2,4 | 123 |
| Часов'ярське родовище | 1500 | 1,2 | 2 | 114 |
| Костантинівське родовище | 1500 | 4,3 | 1,5 | 124 |
| Костантинівське родовище | 1500 | 0,30 | 1,7 | 124 |
Таблиця 4.5 — Результати розрахунків адсорбційної ємності за метиловим червоним у розчині
| Назва сорбенту | Вхідна концентрація, Свх, мг / дм3 | Наважка глини m, г | Залишкова концентрація, Сзал, мг / дм3 | Адсорбційна ємність Г, мг/г |
| Суглинок (Біла Балка) | 1500 | 0,30 | 3,8 | 93 |
| Часов'ярське родовище, II сорт | 1500 | 0,30 | 3,2 | 98 |
| Луганське родовище | 1500 | 0,30 | 3,3 | 98 |
| Часов'ярське родовище | 1500 | 3,2 | 2 | 98 |
| Костантинівське родовище | 1500 | 4,3 | 1,5 | 89 |
| Костантинівське родовище | 1500 | 0,30 | 3,3 | 98 |
Висновки
При виконанні магістерської роботи було зроблено:
1. Розглянуто загальну характеристику глин.
2.Розглянуто фізико-хімічні основи процесу адсорбції, наведені основні рівняння, оцінені фактори, що впливають на процес адсорбції.
3. Експериментально визначено йодне число глин. Йодне число відрізняється в значних межах, що обумовлено різним механізмом сорбції на глинах.
4. Експериментально вивчені сорбційні властивості глин по відношенню до барвників. Як свідчать результати досліджень, всі зразки глин проявляють сорбційні властивості. Величина сорбційної ємності глин складає 50–60 % від аналогічної величини для активних вугілля.
Надалі планується оцінити механізм адсорбції на глинах на підставі вивчення ізотерм адсорбції для барвників, а також вивчити адсорбційні властивості глин по відношенню до забруднювачів різної природи (іони важких металів, органічні сполуки та інші).
Перелік посилань
- Везенцев, А.И. Адсорбционные свойства продуктов обогащения природных монтмориллонитсодержащих глин // А.И. Везенцев. – Белгород: Белгородский государственный национальный исследовательский университет, 2011. – С. 103-108
- Івченко, В.Д. Очищення стічних вод від іонів амонію та феруму глинистими мінералами Сумської області: Автореф. канд. техн. наук: 21.06.01 / Сумський національний аграрний університет – С., 2012. – 35 с.
- Ланець, Г. І. Дослідження адсорбційних властивостей глин родовищ Донбасу / О.А. Трошина, Г.І. Ланець // Матерiали XXIV Всеукраїнської наукової конференцiї аспірантів і студентів. – Т.1 – Донецьк: ДонНТУ, 2014. – С. 92 – 94
- Ланець, Г. І. Адсорбційні властивості глин родовищ Донбасу / О.А. Трошина, Г.І. Ланець // Матерiали ХХII Міжнародної науково-технічної конференцiї. – Харків: ХГТУСА, 2014. – С. 71
- Запольський, А.К. Водопостачання, водовідведення та якість води: Підручник / А. К. Запольський. – К.: Вища школа, 2005. – 671 с.
- Тарасевич, Ю.И., Овчаренко, Ф.Д. Адсорбция на глинистых минералах / Ю.И. Тарасевич, Ф.Д. Овчаренко . – К.: Наукова думка, 1975. – 340 с.
- Смирнов, А.Д. Сорбционная очистка воды / А.Д. Смирнов. – Л.: Химия, 1982. – 168 с.
- Фізико-хімічні основи технології очищення стічних вод / За редакцією А.К. Запольського. - Київ: Лібра, 2000. – 549 с.
- ГОСТ 6217 – 74. Уголь активный древесный дробленый. – М.: Государственный комитет стандартов, 1974. – 6 с.
- ГОСТ 4453 – 74. Уголь активный осветляющий древесный порошкообразный. Технические условия. М.: Государственный комитет стандартов, 1974. –11 с.




