|
Актуальность темы
В качестве поглотителей влаги из природного газа широкое распространение получили гликоли – этиленгликоль (ЭГ), диэтиленгликоль (ДЭГ) и триэтиленгликоль (ТЭГ). Все гликоли обладают примерно одинаковой осушающей способностью и выбор осушителя определяется набором его остальных технологических свойств. Одним из таких важных свойств является давление насыщенного пара абсорбента, поскольку оно определяет его потери в виде пара с осушенным газом. В настоящее время для осушки газа чаще используют диэтиленгликоль, который является гораздо менее летучим веществом, чем этиленгликоль. Триэтиленгликоль имеет еще более низкое давление насыщенного пара при температурах осушки газа и имеет хорошие перспективы в технологии осушки. В процессе осушки газа в абсорбент попадают капли рассола, уносимые газом из скважины. Соли, содержащиеся в рассоле, (большей частью хлорид натрия – около 90 % от общей массы солей), в процессе регенерации гликолей от влаги остаются в них и постепенно накапливаются.Насыщенный солями гликоль непригоден для использования в технологическом процессе осушки газа и его необходимо регенерировать, очищая от растворенных солей.При выведении гликолей из процесса осушки, происходит загрязнение окружающей среды накопившимися в гликолях солями, которые попадают из природных газов. Поэтому разработка метода рекуперации очень важна для предотвращения загрязнения флоры и фауны, и тем самым, здоровья человека.А так как применение триэтиленгликоля на сегодняшний день становится более актуальной, то разработка метода регенерации этого осушителя может принести не малую пользу.

|
|
Цель и задачи
Цель работы – разработка способа рекуперации триэтиленгликоля (ТЭГ) при помощи ацетона.. Для решения этого вопроса ставятся следующие задачи:
- анализ состояния вопроса и изучение литературных источников по способам осушки природных газов и механизм технологии рекуперации осушителя газа различными способами;
- экологическая значимость решаемой проблемы;
- проведение лабораторного эксперимента. Обработка полученных данных при помощи пакета MS Excel;
- разработка технологии обессоливания триэтиленгликоля на основе полученных экспериментальных данных.

|
|
Научная новизна
Цель работы – разработка способа рекуперации триэтиленгликоля (ТЭГ) при помощи ацетона.До этого этим вопросом мало кто занимался. Именно поэтому она представляет научную новизну как для кафедры «Физической и органической химии», так и для научного общества в целом. Возможно разработанная нами схема очиски засолоненного ТЭГ от солей ацетоном заинтересует предприятия, работающие в этой сфере.
|
|

|
|
Практическая ценность
Планируемый практический результат: разработанный метод очистки триэтиленгликоля от солей ацетоном дает возможность почти полной очистки осушителя от солей из - за высркрй высаливающей способности ацетона.

|
|
Обзор существующих исследований
При использовании на газовых промыслах ДЭГ в качестве поглотителя влаги из газа и ингибитора гидратообразования в него попадают содержащиеся в капельной влаге соли [2]. При регенерации такого ДЭГ от влаги соли откладываются на теплопередающих поверхностях, нарушая нормальную работу установок.
Основными компонентами смеси солей, присутствующих в ДЭГ являются хлориды натрия и кальция. Содержание хлорида натрия в капельной влаге достигает 90 % от общего содержания солей [2], а в отложениях на жаровых трубах испарителя до 97 % [3]. Хлорида кальция намного меньше - в капельной влаге порядка 10 % [2], в отложениях - до 2 %[3]. Большие потери от засолонения дорогостоящего поглотителя обуславливают поиски методов и способов устранения их.
Поиски решения проблемы обессоливания ДЭГ могут вестись в следующих направлениях:
1) исключение попадания капельной влаги в поглотитель;
2) очистка поглотителя от растворенных солей.
Первый путь предполагает разработку более совершенных улавливателей капельной влаги и является радикальным.
Второй путь, т.е. очистка ДЭГ от растворенных в нем солей, может быть принципиально осуществлен следующими методами:
1) отгонкой ДЭГ под вакуумом или в виде азеотропной смеси;
2) осаждением солей некоторыми химическими веществами;
3) выделение солей путем снижения их растворимости;
4) выделение солей с использованием ионообменных смол и других ионитов,
5) электролизом и электродиализом.
Каждый из этих методов имеет определенные недостатки, которые затрудняют использование указанных методов для промышленного обессоливания диэтиленгликоля. Например, перегонка ДЭГ должна осуществляться при достаточно глубоком разрежении -давление насыщенного пара ДЭГ при температуре 437 К составляет 5,3 Па [5] Более высокая температура перегонки неприемлема из-за опасности разложения поглотителя [6]. Веществ, которые образовывали бы с ДЭГ азеотропные смеси с низкой температурой кипения очень мало и они малодоступны [7]. Кроме того, очистка ДЭГ путем перегонки связана с большим расходом тепла.
Осаждение солей химическими реагентами является перспективным методом очистки, но его можно использовать только для удаления хлорида кальция.
При этом получающийся хлорид натрия остается в ДЭГ и его суммарная концентрация возрастает. Полученный после осаждения ионов кальция ДЭГ необходимо очищать от хлорида натрия.
Известен способ очистки, основанный на выпаривании водных растворов ДЭГ, содержащих соли [2]. При этом авторы указывают, что растворимость хлорида натрия падает с увеличением температуры и уменьшением содержания воды в ДЭГ. Таким образом, при упаривании засолоненных водных растворов ДЭГ в некоторых случаях можно частично освободиться от растворенного хлорида натрия. В сущности, такой процесс протекает в установках регенерации при удалении влаги из засолоненного ДЭГ. При этом хлорид натрия выпадает на теплопередающих поверхностях в виде плотного трудноудаляемого осадка. Это может привести к выведению из строя осушающие установки.
Метод, в основе которого лежат процессы ионного обмена, начинает широко использоваться в промышленности для очистки ДЭГ от солей [3, 8]. Использование этого метода дает возможность глубоко очищать ДЭГ от солей, но ряд недостатков: малая скорость очистки, необходимость проведения отдельно катионного и анионного обмена, необходимость регенерации ионитов (ионообменных смол), быстрый выход ионитов и смол из строя при очистке частично разложившегося ДЭГ, громоздкость установок мешают широкому внедрению этого метода в промышленность.
Электролиз и электродиализ как методы очистки поглотителя влаги от растворенных солей, очевидно, мало перспективны для использования в промышленности, когда нужно удалять соли из концентрированных растворов.
Тот факт, что в настоящее время нет еще хорошо разработанных методов удаления солей из ДЭГ, не позволяет считать задачу окончательно решенной. Необходимо искать новые методы удаления солей из поглотителя. Одним из таких перспективных методов является метод обратного высаливания. Разработан способ удаления солей из засолоненного ДЭГ с помощью бензола [9]. Процесс заключается в добавлении к засолоненному ДЭГ бензола, нагревании с перемешиванием полученной системы до температуры 433 К, фильтровании образующейся суспензии хлорида натрия и удалении бензола из регенерированного ДЭГ нагревом. Положительные стороны метода:
1) большая скорость обессоливания и большая производительность установки при малых
ее габаритах;
2) бензол все время находится в цикле. Единственным отходом является твердый хлорид
натрия с примесью других солей;
3) соль выделяется во всем объеме раствора и получается сыпучий кристаллический
осадок;
4) проведение глубокой очистки ДЭГ от соли осуществляется за один прием (остаточная
концентрация соли порядка нескольких десятых долей процента) независимо от
величины начальной концентрации соли;
5) широкое варьирование глубины очистки соли за счет изменения температуры
обработки и количества добавляемого бензола;
6) возможно совместное очень эффективное использование этого метода с методами
глубокого обезвоживания ДЭГ.
Но данный метод высаливания с помощью бензола имеет и ряд недостатков:
1) высокая температура обессоливания (около 388 - 433 К) и связанная с этим
необходимость проведения процесса под повышенным давлением;
2) высокая токсичность бензола;
3) невысокая эффективность обессоливания при низких температурах (порядка 298 К);
4) плохая растворимость бензола в ДЭГ и его водных растворах при низких температурах.
Дальнейшее развитие метода обратного высаливания состоит в устранении этих недостатков, что достигается использованием нетоксичных веществ, которые позволяют при более низких температурах и давлениях добиться глубокого обессоливания ДЭГ. Установлено, что хорошими высаливающими свойствами обладают органические кислородсодержащие жидкости, в частности, кетоны. Среди последних наиболее предпочтительным является ацетон, который производится в промышленности в огромных масштабах. Этот растворитель малотоксичен, летуч, смешивается с ДЭГ в любых соотношениях.
Мы экспериментальныи методом решили установить возможность использования метода обратного высаливания ТЭГ при добавлении ацетона. Широкое применение ТЭГ получил из-за его хорошей растворяющей способности, высокой температуры кипения, малой летучести и низкой токсичности и ,самое важное, повышенной гигроскопичности. Преимущества ТЭГ перед ДЭГ при осушке природных и нефтяных газов определяются более низким давлением паров над расвором и более высокой температурой начала разложеня. Меньшее давление паров ведет к снижению поерь абсорбена с газом: в равных условиях потери с 1000 м3 газа триэтиленгликоля составляют 5 г по сравнению с 20 г диэтиленгликоля.
С триэтиленгликолем осушку газа можно вести при более высокой температуре, чем с диэтиленгликолем ; удается повысить температуру регенерации абсорбента, уменьшить содержание в нем воды и тем самым дополнительно понизить точку росы осушаемого газа. Потери ТЭГ в производственных условиях (на испарение, механическй унос, утечки, растворение и т. п.) составляют 0.33 л или 0.4 кг на 100 тыс. м3 осушенного газа. При замене ДЭГ на ТЭГ себестоимость осушки природного газа снижается на 21%.

|
|
Основные результаты работы
1. Подготовка реактивов и основная установка для изучения растворимости хлорида натрия в ацетонгликолевых и водногликолевых растворителях:
Подготовка реактивов, необходимых для проведения эксперимента, проводилась следующим образом. ТЭГ квалификации «хч» перегонялся при пониженном давлении при температуре 120 °C, и для эксперимента отбиралась средняя фракция. Показатель преломления очищенного ТЭГ при 20 °Cсоставил 1,4555 (справочное значение 1,4559). Ацетон квалификации «осч» перегонялся при атмосферном давлении с отбором средней фракции. Плотность использовавшегося ацетона 790,6 кг/ м3, показатель преломления при 20°C — 1,3590, содержание воды, определенное по методу Фишера, — 0,03%. Вода бралась в виде бидистиллята. Хлорид натрия квалификации «хч» использовался без дополнительной очистки, но предварительно прогревался до 150 °C для осушки Установка для изучения растворимости включала в себя термостатирующий стеклянный стакан, заполненный водой. Вода интенсивно перемешивалась пропеллерной мешалкой. В стакан вставлялась ячейка, представляющая собой ампулу емкостью около 15 мл, с сужением в верхней части, которое плотно закрывалось полиэтиленовой пробкой. Предварительно в ячейку помещался кристаллический хлорид натрия, взятый в избытке, и двухкомпонентный растворитель (ТЭГ – ацетон или ТЭГ – вода) известного состава. Точные значения масс компонентов растворителя находились путем взвешивания на аналитических весах. Содержимое ячейки перемешивалось с помощью стального стержня, который вращался при включении магнитной мешалки.
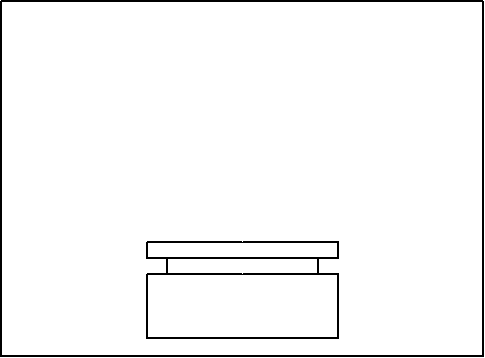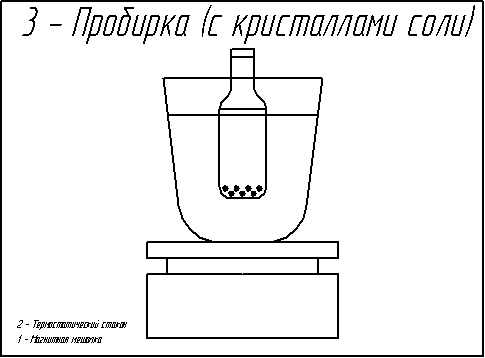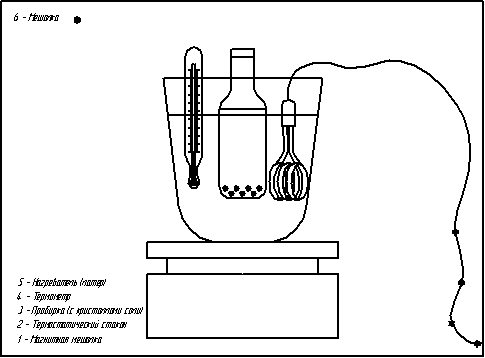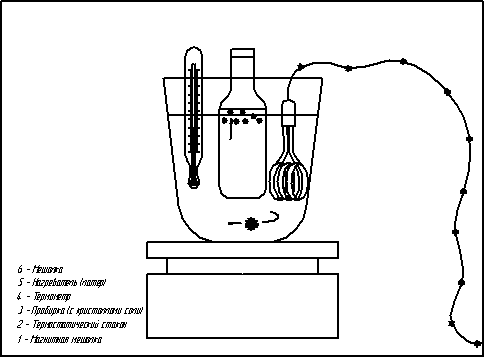
Рисунок 1– Схема установки для проведения эксперимента (38 слайдов с интервалом 0,2 сек., неограниченное количество повторений, )
2. Порядок проведения опыта:
Изучение растворимости хлорида натрия в ацетонгликолевых и водногликолевых растворах заключалось в следующем. При постоянной температуре проводили интенсивное перемешивание содержимого ячейки до достижения состояния равновесия. Как было установлено, при температуре 25 °C равновесие устанавливается в течение 15 – 20 мин. После этого при отключенной магнитной мешалке происходило оседание избытка кристаллов соли. С помощью шприца отбиралась проба насыщенного раствора для определения концентрации хлорида натрия. Проба раствора переносилась во взвешенную на аналитических весах мерную колбу, которая после этого снова взвешивалась. Затем проба разбавлялась дистиллированной водой до объема 100 мл. Для титрования бралась аликвотная часть в 20 – 50 мл в зависимости от концентрации соли в растворе. Анализ проводили по методу Мора 0,05 N раствором нитрата серебра с использованием хромата калия в качестве индикатора. Как правило, титрование исследуемого раствора проводилось дважды.
3.Анализ полученных данных:
Вначале мы провели изучение растворимости в системе хлорид натрия - ТЭГ – ацетон при температуре 25 °C.Данные по растворимости хлорида натрия в смесях ТЭГ – ацетон при температуре 25 °C приведены в таблице 1.
Таблица.1
| Сод. ТЭГ в растворителе, % мас. |
100,0 |
81,7 |
60,4 |
38,8 |
23,4 |
0,0 |
| Сод. ацетона в растворителе, % мас. |
0,0 |
18,3 |
39,6 |
61,2 |
76,6 |
100,0 |
| Конц. хлорида натрия в нас. р-ре, % мас. |
4,92 |
2,83 |
1,37 |
0,49 |
0,14 |
<0.01 |
Как следует из приводимых экспериментальных данных, добавление ацетона к растворам хлорида натрия в триэтиленгликоле приводит к резкому уменьшению растворимости соли и переходу ее в твердую фазу, что свидетельствует о высокой высаливающей способности ацетона.
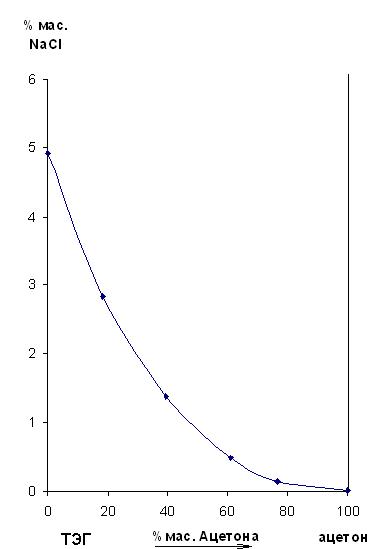
Рисунок 2– Растворимость NaCl в двухкомпонентном растворителе ТЭГ – ацетон при 25°C
Кроме того, была исследована растворимость хлорида натрия в смесях триэтиленгликоль – вода при температурах 25 °C и 40 °C.
Растворимость хлорида натрия в смесях триэтиленгликоль – вода различного состава при температурах 25 и 40 °C приведена в таблице 2.
Таблица.2
| Сод. ТЭГ в растворителе, % мас. |
100.0 |
78.4 |
60.7 |
44.9 |
0,0 |
| Сод. воды в растворителе, % мас. |
0.0 |
21.6 |
39.3 |
55.1 |
100,0 |
| Конц. хлорида натрия в нас. р-ре, % мас. |
при 25 °C |
4,92 |
7,24 |
11,0 |
14,5 |
26,5 |
| Конц. хлорида натрия в нас. р-ре, % мас. |
при 40 °C |
4,16 |
7,34 |
11,5 |
15,1 |
26,7 |
Характер растворимости хлорида натрия в смесях триэтиленгликоль – вода аналогичен характеру растворимости этой соли в смесях диэтиленгликоль – вода. С ростом температуры концентрация хлорида натрия в водногликолевом растворе с высоким содержанием воды увеличивается, а с высоким содержанием гликоля – падает, так же, как и в чистом гликоле. При этом, как было установлено нами, существует двухкомпонентный растворитель, содержащий около 80 % триэтиленгликоля, растворимость хлорида натрия в котором не зависит от температуры. В этом растворителе теплота рвстворения хлорида натрия равна нулю. Такой характер растворимости соли в двухкомпонентном растворителе триэтиленгликоль - вода может быть связан с образованием ионных пар, доля которых растет при увеличении содержания триэтиленгликоль в растворителе.
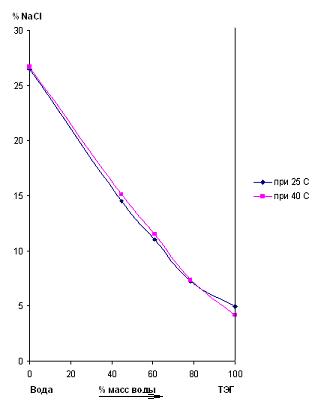
Рисунок 3– Растворимость NaCl в двухкомпонентном растворителе ТЭГ – вода при 25 °C и 40 °C
На основании полученных данных разработана схема очистки засолоненного ТЭГ от солей с помощью ацетона с возвращением в цикл последнего и определены основные технологические параметры ее работы.
Холодный засолоненный ТЭГ проходит теплообменник 14, где нагревается горячим регенерированным ТЭГ до температуры 313К и подается насосом 13 в реактор 1.Реактор снабжен мешалкой, приводимой в движение электродвигателем 2 и рубашкой, в которую подается пар. После загрузки ТЭГ в реактор насосом 12 из сборника 8 подается жидкий ацетон до нужного соотношения. При интенсивном перемешивании и нагреве до температуры 363 К и давлении 2,5 * 105 Па в системе происходит выделение кристаллов соли. Полученная суспензия под давлением паров ацетона при открывании вентиля 4 (задвижки) поступает в фильтр 3 для отделения кристаллов NaCl от жидкой фазы. В фильтре при падении давления происходит частичное испарение ацетона из раствора. Пары его через вентиль 5, попадают в конденсатор 7, где охлаждаются и конденсируются с помощью холодной воды. Жидкий ацетон попадает в сборник 8. Из этого сборника ацетон насосом 12 может вновь подаваться в реактор 1 для удаления соли из ТЭГ. Жидкий обессоленный ТЭГ поступает в куб 9, где он нагревается глухим паром до температуры 403 К для отгонки остающегося ацетона, пары которого превращаются в жидкость в конденсаторе 7. Горячий обессоленный ТЭГ насосом 14 подается в теплообменник 15, где охлаждается за счет передачи тепла холодному засолоненному ТЭГ, и подается затем на осушку природного газа. Для возмещения потерь ацетона в виде пара и с уходящим регенерированным ТЭГ предусмотрена подача свежего ацетона в сборник 8.
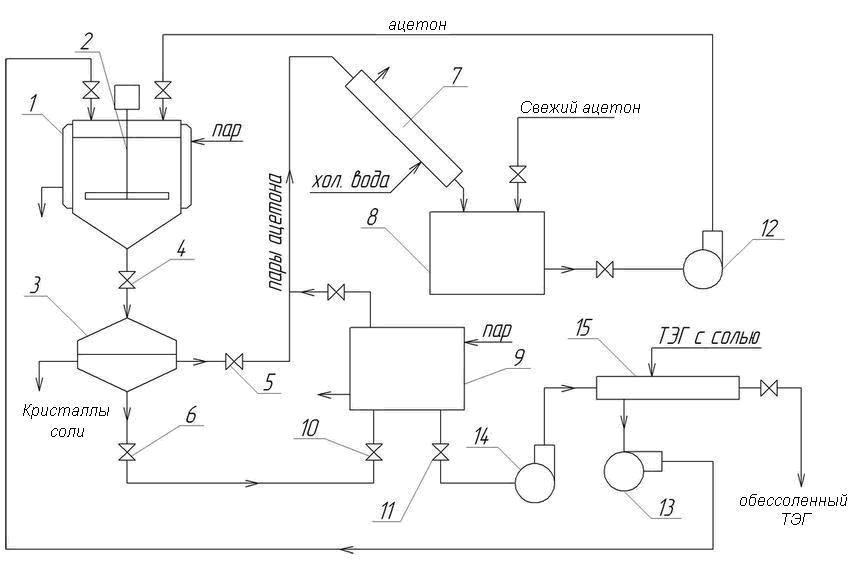
Рисунок 4– Технологическая схема обессоливания триэтиленгликоля с помощью ацетона
4.Планируемые исследования:
Конечно, наличие воды в ТЭГ существенно снижает эффективность использования ацетона для удаления хлорида натрия из гликоля. Насколько велико это снижение должно показать изучение растворимости хлорида натрия в трехкомпонентном растворителе ТЭГ – ацетон – вода. Повышение температуры увеличивает глубину очистки ТЭГ от солей, поэтому необходимо также изучить поведение исследуемой системы при гораздо более высоких температурах, превышающих нормальную температуру кипения ацетона. Кроме того, такие данные будут необходимы для расчета процесса удаления ацетона из регенерированного от соли ТЭГ.

Выводы
Решение проблемы очистки поглотителя влаги из газа, триэтиленгликоля, от солей очень важно в экологическом значении, поскольку при этом предотвращается загрязнение окружающей среды.
С целью разработки способа очистки триэтиленгликоля от солей с помощью ацетона экспериментальным путем изучена растворимость NaCl в двухкомпонентных растворителях: ТЭГ - ацетон, ТЭГ - вода, ацетон - вода, а также в трехкомпонентном растворителе ТЭГ -ацетон - вода при температуре 298 К. Изучение растворимости в системе ТЭГ - ацетон - вода -NaCl показывает, что хлорид натрия может быть удален из засолоненного ТЭГ с помощью ацетона. При этом ,как показывает эксперимент, очистка ТЭГ от солей наиболее эффективно протекает в отсутствие воды при повышенной температуре смешения засолоненного ТЭГ с ацетоном. Последнее целесообразно, так как при последующей отгонке ацетона из регенерированного ТЭГ раствор необходимо нагревать.На основании исследований разработана технологическая схема очистки ТЭГ от солей с помощью ацетона. Оценочный расчет показывает работоспособность этой технологической схемы и экономическую целесообразность процесса регенерации ТЭГ от солей с помощью ацетона.
Метод обратного высаливания хлорида натрия ацетоном может быть положен в основу эффективного промышленного метода обессоливания поглотителя влаги из природного газа -ТЭГ.
.

Литература
1. Могильный В.И., Клименко А.П., Чалюк Г.И. Исследование растворимости хлористого натрия и кальция в диэтиленгликоле. // Химическая технология. - 1972. -
№ 1.-С. 42-61.
2. Бондарь А. Д., Грибкова В.И., Моисеева Н.Ф. Опыты по обессоливанию диэтиленгликоля. // Газовое дело. - 1970. - № 2. - С. 43 - 45.
3. Способ очистки диэтиленгликоля от солей, выносимых из скважин с пластовой водой на групповых пунктах низкотемпературной сепарации газа: Отчет НТО НТП Шебелинского газопромыслового упр. имени 50-летия Октября; Руководитель
Будынко В.Ф. - Пос. Червоный Донец, 1970. - 90 с: ил.
4. Жданов Н.В, Халиф АЛ. Осушка природных газов. - М.: Недра, 1975. - 160 с.
5. Справочник химика, т. 1. —Л,: Химия, 1964. - 1168 с.
6. Дымент О.Н., Казанский КС, Мирошников A.M. Гликоли и другие производные
окисей этилена и пропилена. - М.: Химия, 1976. - 376 с.
7. Равновесие между жидкостью и паром. Справочник / Под ред. В.Б.Когана. - Л.: Химия, 1971. -1123 с.
8 Соловьев СИ., Михельман А.И., Червоненко А Г. Очистка диэтиленгликоля от ионов натрия, калия и кальция при помощи катеонитов // Известия высших учебных заведений. Нефть и газ. - 1971. - № 10. - С. 57 - 59.
9. Матвиенко В.Г., Ярым-Агаев Н.Л. Очистка ДЭГ от растворенных солей бензолом. //
Газовая промышленность. - 1988. - № 1. - С 52 - 53.
10. Лабораторные исследования процесса осушки природного газа абсорбентами-смесями
диэтиленгликоля с у - бутиролактоном и N - метилпирролидоном, определение
способов их регенерации и способа обессоливания водных растворов
диэтиленгликоля: Отчет по теме Х-75-132; Руководитель Н.Л Ярым-Агаев.- №
ГР75042657; Инв. № Б 495 897. - Донецк, 1975. - 175 с: ил.
11. Коробчанский И.Е.Э Кузнецов М.Д. Расчеты аппаратуры для улавливания химических
продуктов коксования. - М.: Металлургия, 1972. - 296 с.
12. Захаров Л.Н. Техника безопасности в химических лабораториях. - Л.: Химия, 1991. -
336 с.
13. Макаров Г.В., Васин А.Я. Охрана труда в химической промышленности, - М.: Химия,
1989.-496 с.
14. СНиП 11-4 - 79. Естественное и искусственное освещение. Нормы проектирования. -
М.: Стройиздат, 1980. -48 с.

ДонНТУ> Портал магистров ДонНТУ> Биография
| Електронная библиотека
| Ссылки
|
Отчет о
поиске | Индивидуальное
задание
| |
![]()
![]()





