Infectious Disease Transmission Models to Predict, Evaluate, and Improve Understanding of COVID-19 Trajectory and Interventions // Ann Am Thorac Soc Vol 17, No 10, pp 1204–1206, Oct 2020 [Ссылка]
Модели передачи инфекционных заболеваний для прогнозирования, оценки и улучшения понимания траектории и мер влияния на COVID-19
Andrea G. Buchwald, Jimi Adams, David M. Bortz, Elizabeth J. Carlton
Введение
Коронавирусная болезнь (COVID-19) быстро распространилась по миру с разрушительными последствиями. Возникают большие вопросы о том, как будет развиваться эта эпидемия и какие меры могут замедлить распространение. Перед лицом глобальной пандемии, вызванной новым инфекционным агентом, перед политиками стоит сложная задача – решить, как и когда принимать меры по борьбе с COVID-19 – меры, оказывающие серьезное экономическое и социальное воздействие [1]. Перед ними стоит чрезвычайно трудная задача найти баланс между приемлемым для общества бременем смерти с одной стороны и экономической активностью и возвращением к нормальной жизни с другой. Математические модели передачи инфекционных заболеваний играют ключевую роль в принятии ответных мер правительства; они обеспечивают основу для оценки потенциального воздействия различных мер политики – от ношения масок до ослабления социального дистанцирования – на течение эпидемии и на ожидаемое количество потерянных жизней, а также на то, могут ли и когда могут быть превышены возможности больниц. Мы работаем со штатом Колорадо, используя модели передачи, чтобы помочь директивным органам предсказать будущее развитие эпидемии и оценить потенциальное воздействие вмешательств, направленных на замедление распространения тяжело-острого респираторного синдрома коронавируса 2 (SARS-CoV-2). Учитывая решающую роль моделей инфекционных заболеваний в этой пандемии, важно понимать их сильные и слабые стороны, а также то, почему разные модели могут давать противоречивые результаты.
Моделирование эпидемий инфекционных заболеваний
Модели передачи заболеваний использовались для прогнозирования продолжительности и масштабов инфекционных вспышек, оценки потенциального воздействия вмешательств и оценки важных биологических и клинических параметров. Они особенно хорошо подходят для ранних стадий вспышки, так как экономно используют разреженные данные. В идеале используемая модель определяется интересующим вопросом и адаптирована к конкретным патогенам. Этот подход оказался необычайно мощным, поскольку он дает представление о движущих силах динамики заболевания, а также дает основу для изучения воздействия и эффективности многочисленных стратегий смягчения последствий.
Применение математического моделирования к инфекционным заболеваниям относится к 1600-м годам. Работа Кермака и МакКендрика в начале 20-го века привела к стандартному разделению популяции на уязвимые, инфекционные и иммунные (или выздоровевшие) категории, составляющие модель SIR [2]. В этой формулировке приоритет отдается потоку между категориями, особенно скорости передачи, то есть скорости перехода населения от восприимчивого к инфекционному. Модели SIR могут быть детерминированными или стохастическими, а сложность может быть увеличена, чтобы адаптировать модели к характеристикам конкретных патогенов с учетом различий в инкубационных периодах, тяжести симптомов и множественных путях передачи, как показано на модели Колорадо (рисунок 1). Модели SIR могут быть расширены в рамках метапопуляционной структуры [3], а с современными вычислительными возможностями агентные модели могут моделировать популяцию людей, а не отдельные части, со сложными демографическими и поведенческими профилями, взаимодействующими для распространения патогенов [4]. .
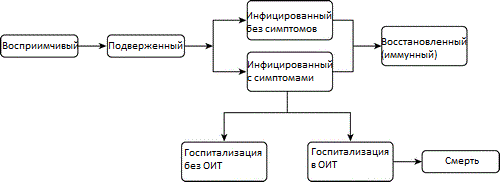
Рисунок 1 – Структура модели Восприимчивые Подверженные Инфицированный Восстановленный
(SEIR), используемой для моделирования вспышки SARS-CoV-2 в Колорадо. Инфицированные люди разделены на бессимптомные и симптоматические
группы. Предполагается, что бессимптомные люди менее заразны, но циркулируют в обществе, тогда как пациенты с симптомами считаются более заразными, но некоторая их часть самоизолируется после появления симптомов. ОИТ – отделение
интенсивной терапии.
При использовании любой модели оценки, прогнозы хороши настолько, насколько хороши их предположения, и сильно зависят от качества данных, которые могут быть ограничены в начале эпидемии. В период эпидемии Эболы 2014–2015 гг. большинство моделей переоценивали серьезность вспышки из-за недостатка данных и множества неизвестных [5]. Однако математические модели показали большую полезность при прогнозировании вспышек гриппа, особенно в контексте надежных источников данных [6]. Кроме того, хотя технология предлагает возможность создавать все более сложные модели, для каждого дополнительного элемента требуется дополнительный набор допущений [7]. Эти расширяющиеся предположения создают внутреннее противоречие между сложностью и экономностью, и усиливают потребность в прозрачности предположений модели и источников данных среди исследователей, чтобы можно было сравнивать и интерпретировать результаты различных моделей.
Моделирование передачи во время пандемии COVID-19
На ранней стадии пандемии модели передачи заболеваний использовались для оценки основных характеристик SARS-CoV-2, включая долю случаев, выявленных системами эпиднадзора, и различия в инфекционности между выявленными и невыявленными случаями [8]. Для этих целей исследователи разработали модели передачи и, сравнивая прогнозы моделей с наблюдаемыми данными, они делают выводы о неизвестных значениях параметров.
Модели передачи также используются для оценки воздействия вмешательств путем моделирования будущего хода пандемии при различных сценариях вмешательства. В марте разработчики моделей из Имперского колледжа опубликовали ряд прогнозов, оказавших широкое влияние на политику и общественное мнение. Используя агентную модель, включающую плотность населения с высоким разрешением и взаимодействие людей, они спрогнозировали ужасные уровни госпитализаций и смертей при всех сценариях вмешательства, кроме самых интенсивных, и пришли к выводу, что меры социального дистанцирования на уровне населения в сочетании со сдерживанием случаев заболевания, будет необходимо применять в течение нескольких месяцев, чтобы избежать переполнения больниц [9], а ослабление таких мер, вероятно, приведет к восстановлению кривых заболеваемости [10].
Такие модели передачи полезны для руководства национальной политикой, но течение эпидемии широко варьируется в зависимости от местности; поэтому модели должны быть адаптированы к местным условиям. В Колорадо наша группа разработала модель на основе SIR в сотрудничестве с государственными чиновниками для ретроспективной оценки воздействия мер политики на уровне штата и прогнозирования воздействия будущих мер на потребность в больницах[11]. Наша модель расширяет базовую структуру SIR, чтобы учесть инкубационный период вируса и бессимптомные инфекции, а также включить влияние возрастной структуры на прогрессирование заболевания (рисунок 1). Модель соответствует местным данным о COVID-19 и использует оценки загруженности больниц и отделений интенсивной терапии (ОИТ) на уровне штата, характерные для Колорадо. Мы ответили на прямые запросы правительства штата и разработали модель специально, чтобы ответить на основанные на политике вопросы о траектории вспышки и потребностях больниц и интенсивной терапии (рис. 2). Нас также попросили количественно оценить влияние политики на эпидемию вскоре после ее реализации. Для оценки потребностей в здравоохранении были разработаны другие модели, в первую очередь Модель воздействия эпидемий на больницы COVID-19. Модель CHIME позволяла генерировать оценки потребности в больницах на ранней стадии эпидемии, но она страдала от упрощеного подбора данных для конкретных местностей.
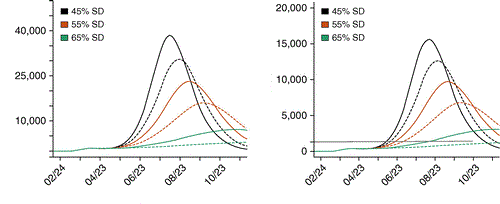
Рисунок 2 – Прогнозируемые госпитализации связанные с коронавирусными заболеваниями (слева) и потребности в отделениях интенсивной терапии (ОИТ) (справа) в Колорадо при различных сценариях вмешательства с использованием модели SEIR. Жирными линиями показаны планируемые стратегии поощрения социального дистанцирования (SD) с разной интенсивностью, а пунктирными линиями показаны комбинированные вмешательства, включающие как социальную дистанцию, так и ношение масок. Социальная дистанция моделируется как процентное снижение частоты контактов, где, например, 65% – это 65% сокращение тесного контакта между людьми. Серая горизонтальная линия указывает на вместимость отделения интенсивной терапии 1800 человек.
Одной из существенно отличающихся моделей общественного прогнозирования была модель, разработанная Институтом показателей и оценки здоровья [12]. Она не начиналась как механистическая модель передачи, которая явно моделирует распространение инфекции, а вместо этого использовала смертность в качестве индикаторной переменной, рассчитывая ожидаемую госпитализацию и использование интенсивной терапии с помощью методов аппроксимации кривой. Несмотря на недавние обновления, которые теперь добавляют последствия ослабления социального дистанцирования, оценочная траектория эпидемии Института показателей и оценки здоровья все еще расходится с другими моделями передачи, особенно из-за того, что не предсказывает вторую волну инфекций [13].
Модели и принятие решений
Команды моделирования должны быть прозрачными в предположениях своих моделей и обновлять эти предположения по мере развития понимания COVID-19, что, несомненно, приведет к изменениям в прогнозах со временем и опытом.
Как лица, принимающие решения, должны решить, какой модели верить и использовать при принятии решений? Как ученые, мы стремимся к согласованности [14]: в идеале, несколько моделей, выполненных разными командами, сходятся на схожих выводах, укрепляя нашу уверенность в этих выводах [15]. Когда прогнозы разных групп не совпадают, политики сталкиваются с трудной задачей – противоречивой информацией из этих моделей. В идеале политические и практические решения должны основываться на ряде моделей, использующих разные структуры и допущения, а не на едином подходе. На момент написания этой статьи в мае 2020 года существует практически единое мнение о том, что полное ослабление социального дистанцирования может привести к катастрофической второй волне инфекций.
Модели передачи инфекционных заболеваний, первоначально разработанные более века назад, будут и дальше играть важную роль в обеспечении ответных мер на COVID-19. Оптимальное использование таких моделей требует четкой информации об их исходных предположениях, постоянного уточнения, чтобы отразить текущее состояние науки, и выработки политики, основанной на выводах нескольких моделей.
Ссылки
- Correia S, Luck S, Verner E. Pandemics depress the economy, public health interventions do not: evidence from the 1918 flu. June 5, 2020 [accessed 2020 Jun 5]. Available from: http://dx.doi.org/10.2139/ssrn.3561560.
- Kermack WO, McKendrick AG. Contributions to the mathematical theory of epidemics. II.—The problem of endemicity. Proc R Soc A 1932;138:55–83. Available from: https://royalsocietypublishing.org/doi/ abs/10.1098/ rspa.1932.0171
- Grenfell B, Harwood J. (Meta)population dynamics of infectious diseases. Trends Ecol Evol 1997;12:395–399. Available from: https://pubmed.ncbi.nlm.nih.gov/21238122/
- Burke DS. Computational modeling and simulation of epidemic infectious diseases. In: Smolinski MS, Hamburg MA, Lederberg J, editors. Microbial threats to health: emergence, detection, and response. Washington, DC: National Academies Press; 2003. pp. 335–341.
- Chretien J-P, Riley S, George DB. Mathematical modeling of the West Africa Ebola epidemic. Elife 2015;4:e09186. Available from: https://pubmed.ncbi.nlm.nih.gov/26646185/
- Nsoesie EO, Brownstein JS, Ramakrishnan N, Marathe MV. A systematic review of studies on forecasting the dynamics of influenza outbreaks. Influenza Other Respir Viruses 2014;8:309–316. Available from: https://pubmed.ncbi.nlm.nih.gov/24373466/
- Jewell NP, Lewnard JA, Jewell BL. Predictive mathematical models of the COVID-19 pandemic: underlying principles and value of projections. JAMA [online ahead of print] 16 Apr 2020; DOI: 10.1001/jama.2020.6585. Available from: https://jamanetwork.com/journals/jama/article-abstract/2764824
- Li R, Pei S, Chen B, Song Y, Zhang T, Yang W, et al. Substantial undocumented infection facilitates the rapid dissemination of novel coronavirus (SARS-CoV-2). Science 2020;368:489–493. Available from: https://pubmed.ncbi.nlm.nih.gov/32179701/
- Ferguson NM, Laydon D, Nedjati-Gilani G, Imai N, Ainslie K, Baguelin M, et al. Impact of non-pharmaceutical interventions (NPIs) to reduce COVID-19 mortality and healthcare demand. London: Imperial College London; 16 March 2020 [accessed 2020 May 1]. Available from: https://www.imperial.ac.uk/media/imperial-college/medicine/sph/ide/gida-fellowships/Imperial-College-COVID19-NPI-modelling-16-03-2020.pdf
- Unwin HJT, Mishra S, Bradley VC, Gandy A, Mellan T, Coupland H, et al. State-level tracking of COVID-19 in the United States [preprint]. medRxiv; 2020 [accessed 2020 Jul 14]. Available from: https://www.medrxiv.org/ content/10.1101/ 2020.07.13.20152355v1
- Buchwald A, Carlton E, Ghosh D, et al. Findings on the COVID-19 epidemic in Colorado to date and projections for future scenarios of social distancing. 2020 [accessed 2020 Apr 20]. Available from: https://covid19.colorado.gov/ sites/covid19/files/ COVIDModelingReport-042020.pdf
- Murray C. Forecasting COVID-19 impact on hospital bed-days: ICU-days, ventilator days and deaths by US state in the next 4 months. MedRxiv [online ahead of print] 26 Mar 2020; DOI: 10.1101/2020.03.27.20043752.
- Jewell NP, Lewnard JA, Jewell BL. Caution warranted: using the Institute for Health Metrics and evaluation model for predicting the course of the COVID-19 pandemic. Ann Intern Med [online ahead of print] 14 Apr 2020; DOI: 10.7326/M20-1565. Available from: https://www.acpjournals.org/doi/full/10.7326/M20-1565
- Hill AB. The environment and disease: association or causation? Thousand Oaks, CA: Sage Publications; 1965. Available from: https://journals.sagepub.com /doi/pdf/ 10.1177/ 003591576505800503
- Excellence U-AIFCo. COVID-19 forecast hub. 2020 [accessed 2020 May 1]. Available from: https://github.com/reichlab/covid19-forecast-hub