Реферат по теме выпускной работы
Содержание
- 1. Цель, задачи и объект исследований
- 2. Влияние диоксида серы на человека, растительный и животный мир
- 3. Обзор сухих и мокрых методов очистки отходящих газов содержащих диоксид серы
- 3.1 Методы на основе суспензий природных сорбентов
- 3.2 Методы на основе применения растворов солей натрия и аммония
- 3.3 Поглощение диоксида серы твердыми поглотителями
- 3.4 Сухие методы сероочистки
- 4. Методика эксперемента
- Выводы
- Список источников
1. Цель, задачи и объект исследований
Цель и задачи исследований активации оксида и карбоната кальция является:
- Определение температуры сплава активатора и карбоната кальция, активатора и оксида кальция;
- Температуры начала взаимодействия с диоксидом серы систем МеNO3 – CaCO3, МеNO3 – CaO;
- Определение эффективности поглощения диоксида серы оксидом и карбонатом кальция с использованием различных активаторов.
Объектом исследования: взаимодействие систем МеNO3 – CaCO3 и МеNO3 – CaO с SO2.
2. Влияние диоксида серы на человека, растительный и животный мир
Диоксид серы является одним из наиболее крупных и трудно поддающихся очистке загрязнителей атмосферного воздуха. Он неблагоприятно влияет на здоровье человека: вызывает раздражение слизистой оболочки глаз, дыхательных путей, спазм бронхов и увеличение сопротивления дыхательных путей.
Помимо влияния на здоровье человека, диоксид серы оказывает неблагоприятное воздействие на окружающую среду, в частности, на растительность, на здания и сооружения.
Неоднократно учеными было изучено влияние выбросов теплоэлектростанций на здоровье людей, проживающих в районах с различной интенсивностью загрязнения атмосферного воздуха, в результате чего было установлено наличие неблагоприятного влияния выбросов на санитарно-бытовые условия и здоровье населения в зоне задымления при максимальной концентрации S02 в атмосфере 3,3-4,0 и пыли 2,5-4,6 мг/м3. Общее число жалоб и частота заболеваний верхних дыхательных путей по некоторым формам в этой зоне оказалась в два раза выше, чем в относительно чистом районе. В основной группе школьников (зона задымления) у большинства детей отмечено пониженное содержание гемоглобина, выявлено наличие SO2 в крови (от следов до 0,02 мг), высокая заболеваемость конъюнктивитами (13,3% по сравнению с 3,8% в контрольном районе).
Результаты исследования воздействия S02 на организм человека приведены в табл.1.
| Концентрация S02 в воздухе, мг/м3 | Концентрация пыли в воздухе, мг/м3 | Продолжительность воздействия, ч | Результаты воздействия |
| 2600 | - | - | Мгновенно приводит к смерти |
| 1400–1600 | - | 0.5–1 | Приводит к смерти |
| 400–500 | - | 0.5–1 | Вызывает опасное для жизни заболевание |
| 40–60 | - | 0.5–1 | Вызывает раздражение слизистых оболочек, чихание, кашель |
| 20 | - | - | Порог раздражающего действия |
| 8–10 | - | - | Вызывает обонятельные ощущения |
| 2–3 | - | - | Концентрация неощутима по запаху |
| 0.72 | 0.75 | 24 | Частичный смертельный исход |
| 0.5 | Незначительная | 24 | Повышенная смертность среди лиц определенной категории |
| 0.1–0.27 | 0.185 (дым) | Годовая | Возрастание заболеваний верхних дыхательных путей и бронхит |
| 0.115 | 0.16 (дым) | - | Повышенная смертность лиц с бронхиальной астмой и бронхитом |
Средняя концентрация SO2 в воздухе изменяется в зависимости от количества сжигаемого топлива и содержания в нем серы. Обычно в атмосферном воздухе диоксид серы не содержится в большой концентрации. Содержание SO2 в атмосфере закономерно повышается в несколько раз с наступлением отопительного сезона, а также период неблагоприятных метеорологических условий.
При наличии отдельных случаев превышения ПДК в целом атмосферный воздух не характеризуется экстремальными уровнями загрязнения диоксидом серы по отношению к человеку, в тоже время эти уровни являются опасными для растительности, поскольку ПДК леса в 3 раза ниже ПДК для воздуха населенных мест. При этом многие ингредиенты, в том числе SO2, при совместном нахождении могут создавать эффекты суммации или потенцирования, в связи с чем экологическая обстановка может быть опасной. Поэтому необходимо вести регулярный контроль за содержанием диоксида серы в атмосфере и разрабатывать способы очистки [1].
Существует множество методов для обезвреживания газовых выбросов от SO2, но все их принято делить на «сухие» и «мокрые».
Каждый из них может быть подразделен на три группы:
- Первая обеспечивает только санитарную очистку газа;
- Вторая группа предполагает циклические процессы с получением товарного SO2 или соединений серы;
- Третья группа включает процессы, в результате которых поглотитель не возвращается в процесс, а используется для получения новых химических веществ. Ниже по подробнее рассмотрим некоторые из них [2].
3. Обзор сухих и мокрых методов очистки отходящих газов содержащих диоксид серы
3.1 Методы на основе суспензий природных сорбентов
Известняковый (известковый) метод
Метод очистки основан на нейтрализации сернистой кислоты, получающейся в результате растворения двуокиси серы, содержащейся в дымовых газах, щелочными реагентами: гидратом окиси кальция (известью) или карбонатом кальция (известняком). При этом протекают следующие реакции:
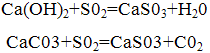
В результате этих реакций получается сульфит кальция, частично окисляющийся в сульфат. В большинстве случаев продукты нейтрализации не используются и направляются в отвал.
Преимуществами известнякового (известкового) метода являются простота технологической схемы, доступность в дешевизне сорбента, относительно малые капитальные затраты, возможность очистки газа без предварительного охлаждения и обеспыливания.
К недостаткам метода относятся низкий коэффициент использования известняка, зависящий от типа применяемого минерала и достигающий, как правило, 40-50%, получение в качестве продукта утилизации неиспользуемого шлама, относительно низкая эффективность очистки, подверженность забиванию кристаллическими отложениями абсорбционной аппаратуры и жидкостных коммуникаций.
Магнезитовый метод
Связывание двуокиси серы происходит при взаимодействии ее с магнезитом по реакции:
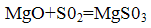
Образовавшийся сульфит магния снова взаимодействует с двуокисью серы и водой, образуя бисульфит магния:
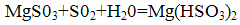
Образовавшийся бисульфит нейтрализуется добавлением магнезита:
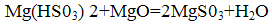
Образовавшийся сульфит магния в процессе обжига при температуре 800-900°С подвергается термическому разложению с образованием исходных продуктов по реакции:
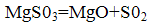
Окись магния возвращается в процесс, а концентрированный S02 может быть переработан в серную кислоту или элементарную серу.
Газ очищается от окислов серы до концентрации 0,03% в скруббере (рис. 1), а образовавшийся раствор бисульфита магния с концентрацией 50-70 г/л поступает в циркуляционный сборник, откуда часть раствора подается в напорный бак и возвращается на орошение скруббера, а другая часть в нейтрализатор для выделения сульфита магния. Раствор из нейтрализатора выводится в гидроциклоиы, затем пульпа направляется на ленточный вакуум-фильтр и затем в обжиговую печь, где образуются двуокись серы и магнезит, повторно используемый в цикле.
Маточный раствор и промывочная вода после фильтр-пресса поступает в сборник осветленного раствора, куда добавляется магнезит из обжиговой печи. Раствор из сборника подается в напорный бак, где смешивается с кислым раствором из циркуляционного сборника и направляется на орошение скруббера. Степень очистки газов от SO2 составляет 90-92%.
Достоинством магнезитового способа является возможность достижения высокой степени очистки газов без предварительного их охлаждения. Обжиг сульфита магния может производиться на химическом предприятии за пределами ТЭС, так как высушенные и обезвоженные кристаллы могут достаточно удобно транспортироваться.
Основным недостатком магнезитового способа является наличие многочисленных операций с твердыми веществами (кристаллами сульфита, окиси магния, золы), что связано с абразивным износом аппаратуры и пилением. Для сушки кристаллов и удаления гидратной влаги требуется значительное количество тепла.
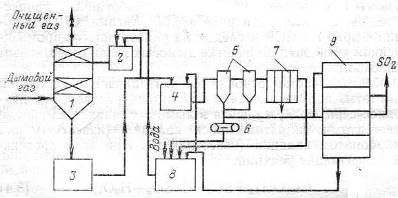
Рисунок 1 – Схема очистки дымовых газов от SO2 магнезитовым методом: 1 – скруббер; 2 – напорный бак; 3 – циркуляционный сборник; 4 – нейтрализатор; 5 – гидроциклоны; 6 – ленточный вакуум-фильтр; 7 – фильтр-пресс; 8 – сборник осветленного раствора; 9 – обжиговая печь [3].
3.2 Методы на основе применения растворов солей натрия и аммония
Аммиачные методы
Аммиачно-циклический способ очистки газа позволяет получить сжиженный 100%-иый сернистый ангидрид и сульфат аммония – продукты, которые могут найти широкое применение в народном хозяйстве. Количество отходов при этом способе очистки невелико.
К числу недостатков способа следует отнести необходимость предварительного глубокого охлаждения дымовых газов перед абсорбцией серы. Глубокое охлаждение достигается водой, которая вступает в непосредственный контакт с газами и нагревается при этом до 40–50°С. Такая вода не может быть сброшена в водоемы общего пользования, а ее рециркуляция в системе охлаждения требует нейтрализации кислоты известью и охлаждения в градирне. При нейтрализации образуются соли кальция, которые могут кристаллизоваться в системе охлаждения. Очищенные охлажденные газы требуют значительного количества теплоты для их подогрева перед выбросом в атмосферу.
Выбросы воздуха из градирен, охлаждающих жидкость, вытекающую из скрубберов, содержат некоторое количество аммиака, которое может загрязнять атмосферу. Дополнительный расход топлива, связанный с потреблением пара на регенерацию раствора, выпарку и сушку сульфата аммония, расход электроэнергии на установку и топлива на подогрев очищенных газон составляют около 10% топлива, расходуемого на ТЭС. Аппаратура сероулавливающей установки довольно громоздка и имеет высокую стоимость.
Методы с применением растворов соды
Сущность этого метода заключается в промывке отходящих газов водными растворами кальцинированной соды. При этом протекают реакции:
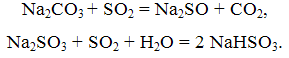
Процесс поглощения SO2 содовым раствором осуществляется в аппаратах насадочного или барботажного типов. Газ проходит последовательно две башни, первая из которых орошается раствором NaHSO3, вторая – раствором Na2SO3. Содовый способ обеспечивает хорошую очистку отходящих газов от SO2 с одновременным получением товарной соли NaHSO3 и Na2SO3.
Преимуществами методов, основанных на применении водных растворов солей натрия, являются высокая эффективность очистки, отсутствие в абсорбенте твердых составляющих, получение в качестве продуктов утилизации ценных для народного хозяйства веществ.
К недостаткам указанных методов относятся повышенная окисляемость солей в цикле сорбции и регенерации, что приводит к дополнительным расходам сорбента; относительная дефицитность сорбента; сложность технологической схемы; повышенные расходы пара на регенерацию в циклических процессах; повышенная коррозионная активность абсорбента.
Кислотно-каталитические методы
Кислотно-каталитический метод основан на получении в зоне абсорбции слабой серной кислоты (10–15 вес.%), находящей ограниченное применение.
К недостаткам метода, послужившим препятствием для его широкого распространения в промышленности, относится низкая скорость окисления SO2 в растворах серной кислоты, несмотря на применение различных катализаторов, а также резкое снижение активности катализаторов под действием ингибирующих органических примесей, например, присутствующих в газах ТЭС [5].
3.3 Поглощение диоксида серы твердыми поглотителями
Недостатки мокрых методов очистки выбросных газов от SO2 (снижение температуры и увлажнение выбрасываемого газового потока, коррозия аппаратуры, громоздкость и высокая стоимость установки) вызвали необходимость разработки процессов, основанных на поглощении SO2 из газовых потоков адсорбентами и химически активными поглотителями при температуре, превышающей точку росы газа. Такие работы в последнее время широко проводятся во всех промышленно развитых странах. Многие исследователи считают сухие процессы весьма перспективными для очистки выбросных газов, особенно в энергетической промышленности и цветной металлургии.
Капитальные затраты на сооружение установок для очистки газов сухими методами, как правило, ниже, а эксплуатационные расходы зачастую бывают значительными. С условиями регенерации сорбентов и очистки выбрасываемых газов от пыли поглотительного материала связано появление смешанных процессов, где наряду с сухими применяются мокрые циклы.
3.4 Сухие методы сероочистки
Из сухих методов сероочистки рассмотрены только процессы, использующие природные реагенты. Существуют и другие сухие способы, например, процессы, разработанные фирмой «Бергбау-Форшунг», «УОП-Шелл» и некоторые др. Однако эти технологии сложны и малоперспективны в условиях электростанций [6].
Сухой аддитивный метод
Метод заключается в том, что тонкоразмолотый известняк вводится в топку котла. При этом известняк обжигается (кальцинируется) с образованием окиси кальция и углекислоты
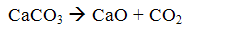
При температуре дымовых газов 500...900 ОС окись кальция взаимодействует с сернистым ангидридом с образованием сульфита кальция
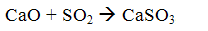
затем, за счет кислорода, содержащегося в дымовых газах, часть сульфита кальция доокисляется в сульфат
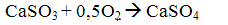
После котла смесь сульфита и сульфата кальция вместе с золой и непрореагировавшей известью улавливается в золоуловителях.
Этот метод опробован во многих странах в различных модификациях, как на стендовых, так и промышленных установках. Ввод аддитива в топку осуществлялся по различным схемам:
- путем добавки к топливу;
- вдуванием в надфакельное пространство;
- через горелки в периферийную область факела.
Сухой аддитивный метод технологически наиболее простой из всех известных на сегодня методов обессеривания дымовых газов. По сравнению с другими методами он требует наименьших капитальных и эксплуатационных затрат, легко реализуется в условиях действующей электростанции. Фактором, сдерживающим применение метода, является его низкая эффективность, составляющая в среднем 30...40%. Кроме того, возможности применения метода ограничиваются условиями безшлаковочной работы экранов топки и высокотемпературных поверхностей нагрева.
Из-за того, что конечный продукт содержит химически активный сульфит возникает проблема складирования отходов.
В то же время на основе этого метода разработана технология «SONOX» (Канада) в энергосистеме «ONTARIO HYDRO», для одновременного снижения выбросов окислов серы а азота. В ней, при использовании в качестве реагента известняка КПД сероочистки составляет 70%, а азотоочистки 90%. При добавлении в суспензию известняка 5-ти процентной присадки доломитого камня КПД сероочистнки удалось повысить до 80% [7].
Метод «Лифак»
Процесс «Лифак», разработанный финской фирмой «Тампелла» по существу является совмещением сухого аддитивного и полусухого методов сероулавливания.
Принципиальная технологическая схема установки «Лифак» показана на рис.2.
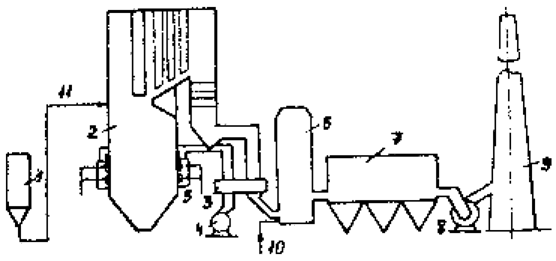
Рисунок 2 – Схема установки «Лифак»: 1 – бункер известняка; 2 – котел; 3 – регенеративный воздухоподогреватель; 4 – дутьевой вентилятор; 5 – горелочные устройства; 6 – активационный реактор; 7 – электрофильтр; 8 – дымосос; 9 – труба; 10 – подвод воды; 11 – ввод известняка в топку
Известняк а виде мелкодисперсной пыли, 80% фракций которой имеют размер не более 32 мкм, вводится с помощью пневматических сопл в поток дымовых газов с температурой 950...1100 °С. В этом интервале происходят кальцинирование известняка по реакции (1). Дальше по тракту котла происходит связывание части диоксида серы по реакциям (2) и (3). Степень улавливания диоксида в этой фазе процесса составляет 30...35%. На этом этапе и не ставится задача достижения максимальной степени связывания SО2. Не менее важно обеспечить оптимальный процесс кальцинирования – максимально возможный переход известняка в окись кальция. С изменением нагрузки зона оптимальных для кальцинирования газовых температур перемещается. Поэтому узлы ввода известняка целесообразно выполнять по крайней мере в двух сечениях газового тракта.
После котла дымовые газы, содержащие смесь твердых веществ в виде золы, сульфита и сульфата кальция и непрореагировавшей извести поступает в активационный реактор, в который впрыскивается вода. Распыливание воды до оптимального размера капель обеспечивается при помощи системы сопл, разработанной фирмой Тампелла.
В реакторе негашеная известь СаО в результате контакта с водой переходит в активную гашеную, которая соединяется с SО2 с образованием сульфита кальция:
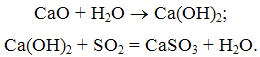
По мере движения газового потока в реакторе капли жидкости испаряются, температура газов понижается. На выходе из реактора остается сухая смесь золы, сульфита и сульфата кальция, которая затем улавливается в электрофильтре или в рукавном фильтре.
Общая степень очистки достигает величины при молярном соотношении Са/S равном 2 (рис.3). Эффективность очистки тем выше, чем ближе температура потока к температуре точки росы.
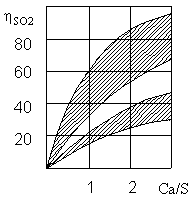
Рисунок 3 – Зависимость степени очистки ηSО2 дымовых газов от сернистого ангидрида от соотношения Са/S [7]
Температура дымовых газов в реакторе поддерживается на 10...15°С выше Температуры точки росы, что обеспечивает получение продуктов реакции в сухом виде.
- летучая зола – 50...70;
- сульфат кальция – 10...15;
- сульфит кальция – 10...15;
Остаток аддитива (СаО, СаСО3, Са(ОН)2) – 10...20.
Основные объекты автоматизации процесса следующие:
- ввод известняка регулируется в зависимости от количества подаваемого топлива. Ввиду того, что качество поступающего топлива (серосодержание, влажность, зольность и др.) меняется, количество подаваемого известняка автоматически корректируется по концентрации SО2 в дымовых газах после котла;
- количество вводимой в реактор воды регулируется в зависимости от конечной температуры газов в реакторе, превышающей на 10...15°С температуру точки росы.
Высокая степень автоматизации установки, дистанционное управление оборудованием со щита управления упрощает ее обслуживание, осуществляемое, как правило, только обходчиками.
Дополнительно требующиеся площади оказываются минимальными, так как реактор размещается в несколько модифицированном газоходе котла, что особенно важно в случае оснащения сероулавливающими установками действующих ТЭС. Капитальные и эксплуатационные затраты на установку «Лифак» значительно ниже затрат на сероочистные установки по любому другому методу [7].
4. Методика эксперемента
Но все представленные методы не совершенны, в связи с этим возникает необходимость в создании универсального поглотителя, который смог бы работать в широком диапазоне температур и концентраций, а также не требовал дальнейшей переработки или утилизации.
В качестве такого поглотителя может выступать оксид и карбонат кальция, реакция процесса:
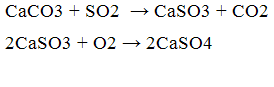
Также использование в качестве поглотителя карбоната и оксида кальция представляется рациональным по следующим причинам:
- предположительно высокая реакционная способность по отношению к оксиду серы (IV);
- отсутствие необходимости в дополнительной обработке;
- выделение тепла, которое в перспективе можно использовать.
Еще одним немаловажным достоинством таких поглотителей является его низкая стоимость, широкое распространение в природе, а также возможность перерабатывать отходы производств по получению соды. Что в свою очередь, решает сразу несколько проблем, утилизация отходов, получение сырья, поглотителя, без извлечения природных ресурсов. В связи с этим, данная работа является очень актуальной и востребованной по ряду вышеизложенных причин.
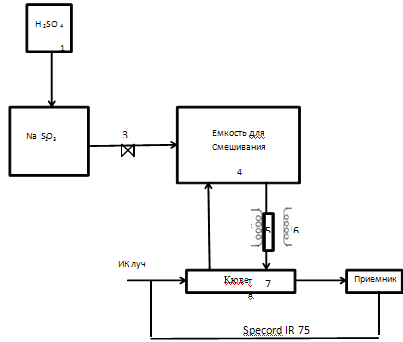
Рисунок 4 – Принципиальная лабораторная схема установки поглощения диоксида серы оксидом и карбонатом кальция.
В колбу 2, которая является реакционной емкостью для получения сернистого газа засыпается навеска Na2SO3. Полученный SO2 через осушитель, в роли которого выступает силикогель, подается насосом 3 в емкость смешения, которая представляет собой 20 л. баллон 4, необходимый для достижения равномерно малых концентраций SO2 порядка 6 г/л. Далее усреднившийся газ проходит через поглотительную трубку 5, помещенную в трубчатую печь 6, температура которой варьируется а широких интервалах. Далее газ проходит через кювету 7 при этом на приборе (Specord IR 75) фиксируется содержание SO2 в виде пиков на спектрограмме.
Далее полученные данные анализируются и опыт повторяется.
Первоначально полученные данные проведены ниже.
Для наглядности приводится таблица температур взаимодействия соединений кальция и активатора.
Таблица 2 – Температура сплавления активаторов и соединений кальция
| Соединение кальция | Активатор | Температура взаимодействия активатора и соединения кальция, оC |
| СаСО3 | Активатор 1 | 215 |
| Активатор 2 | 272 | |
| СаО | Активатор 1 | 210 |
| Активатор 2 | 260 |

Рисунок 5 – ИК спектры поглощения SO2 с добавлением активатора 1 – CaCO3 в зависимости от температуры
(анимация: 9 кадров, 5 циклов повторения, 16,3 килобайт)
Из представленных данных, видно что на первом и втором участке наблюдаются максимальные концентрации SO2 = 6 г/л. Это говорит, о том, что от комнатной температуры до +194 оС никаких изменений не наблюдается, а в интервале температур от + 194 оС до +210оС идет интенсивное поглощение диоксида серы, о чем свидетельствует уменьшение пиков SO2, а уже на последнем участке ми можем наблюдать полное исчезновение пиков SO2. О полноте поглощения свидетельствует так же тот факт, что чувствительность ИК спектроскопии на SO2 составляет 0,09 мг/л.
Выводы:
Предварительные выводы по предложеной теме еще конечно очень рано делать, т.к. эксперемент будет длится до осени, как минимум. Но в связи с тем, что данный поглотитель проверялся на высокотемпературных и высококонцентрированых выбросах, мы надеимся на успех и при наших условиях!!!
Список источников
- Ганз С.Н., Кузнецов И.Е. Очистка промышленных газов.– Киев, 1967
- Алиев Г.М.-А. Техника пылеулавливания и очистки промышленных газов. Справочник М.: Металлургия, 1986. – 544 с.
- Э.М. Соколов, В.М. Панарин, А.А. Зуйкова, Н.А. Криничная. Абсорбционно-каталитический способ очистки дымовых газов от диоксида серы [Электронный ресурс]. – Режим доступа: http://www.eco-oos.ru/biblio/konferencii/ekologiya-obrazovanie-i-zdorovyi-obraz-jizni/07/
- А.В. Гладкий «Абсорбционные методы очистки газов от двуокиси серы» / М. ЦИНТИХИМНЕФТЕМАШ, 1978.
- Абсорбционно-каталитический способ очистки дымовых газов от диоксида серы [Электронный ресурс]. – Режим доступа: http://works.tarefer.ru/94/100077/index.html
- Носков А.С., Пай З.П. Технологические методы защиты атмосферы от вредных выбросов на предприятиях энергетики. Аналит. обзор СО РАН, ГПНТБ, Институт катализа, Новосибирск, 1996. Вып.40.
- Кочетков А.Ю., Коваленко Н.А., Кочеткова Р.П. и др. Катализаторы жидкофазного каталитического окисления сернистых соелинений в сточных водах//Катализ в промышленности, 2003. № 4.
- В.И. Смола, Н.В. Кельцев «Защита атмосферы от двуокиси серы» / М. «Металлургия», 1976.
ВАЖНОЕ ПРИМЕЧАНИЕ. При написании данного реферата магистерская работа еще не завершена. Окончательное завершение: декабрь 2013 г. Полный текст работы и материалы по теме могут быть получены у автора или его руководителя после указанной даты.
