Реферат по теме выпускной работы
Содержание
- Введение
- 1. Актуальность темы
- 2. Цель и задачи исследования, планируемые результаты
- 3. Обзор исследований и разработок
- 3.1 Обзор международных источников
- 3.2 Обзор национальных источников
- 3.3 Обзор локальных источников
- 4. Калориметрия
- Выводы
- Список источников
Введение
В настоящее время природный газ широко используется в качестве сырья и топлива для различных отраслей промышленности. Природный газ является лучшим видом топлива, уступая лишь нефти. Это преимущество связано с высокой теплотой сгорания, легко регулируемой подачей газа в печь, отсутствием золы.
Газ – самый экологически чистый вид топлива, вследствие чего его используют в качестве источника энергии гораздо чаще, чем другие виды топлива. Но его количество в связи с ростом промышленности резко уменьшается, вследствие чего возникает проблема о рациональном использовании газа, его качества. Известно, что чем больше удельная теплота сгорания топлива, тем меньше удельный расход топлива при таком же показателе коэффициента полезного действия. Удельная теплота сгорания измеряется в джоулях на килограмм или калориях на килограмм. Для экспериментального измерения этой величины используются методы калориметрии.
Калориметрия – это наука, которая занимается определением изменения количества энергии путем измерения теплового обмена с окружающей средой. Приборы, используемые для таких измерений, называются калориметрами. Стандартными инструментами для измерения калорийности твердых и жидких сгораемых материалов являются кислородные бомбовые колориметры.
1. Актуальность темы
В связи с современным развитием прикладных областей науки и техники, становятся актуальными работы, касающиеся измерительной техники. Важнейшее место в измерительной технике занимает калориметрия. С помощью калориметров определяют теплоемкость, теплопроводность, теплотворную способность, количество теплоты, выделяющиеся при изменении состояния, энтальпию, энтропию.
Калориметры применяются в металлургии, радиоэлектронике, медицине, радиационной дозиметрии, физике, физической химии, газификации. В последние годы разработан ряд эталонных и образцовых установок для калориметрии. Но, не смотря на это, до сих пор остаются нерешенными некоторые проблемы, связанные с созданием технических калориметров, которые удовлетворяли бы требованием массовых технических измерений для различных прикладных калориметрических задач по чувствительности, температуре, пороговой чувствительности, быстродействию, метрологическим характеристикам.
Все перечисленные параметры калориметров зависят от их теплофизических характеристик (характера теплообмена с окружающей средой), конструктивных особенностей калориметров, типов датчиков температур, способа проведения калориметрического опыта. Следовательно, необходимо уточнение классификации калориметров, их характеристик, изучения существующих моделей, их сравнение и последующая разработка калориметра с улученными характеристиками. Поэтому работа, направленная на решение этих задач, является актуальной и имеющей большое народнохозяйственное и промышленное значение.
2. Цель и задачи исследования, планируемые результаты
Целью данной работы является разработка прибора, определяющего теплотворную способность газа на современной элементной базе.
Основные задачи исследования:
- Анализ существующих калориметров, исследование их характеристик, сравнительный анализ приборов.
- Исследование и поиск решения различных производственных и лабораторних измерений в калориметрии.
- Оценка способов увеличения быстродействия, спектра температуры, чувствительности, пороговой чувствительности, радиационной прозрачности.
- Проведение метрологического исследования и аттестации.
- Введение разработки в исcледовательскую и производственную практику.
Объект исследования: процесс измерения теплотворной способности природного газа в контрольных точках газопровода Россия – Украина.
Предмет исследования: прибор для определения теплотворной способности газа.
3. Обзор исследований и разработок
Так как колориметры являются важной частью в промышленности и газификации, то проблемы их минимизации, улучшения технических и экономических характеристик и реализации было широко исследовано как европейскими, американскими, японскими учеными, так и отечественными специалистами.
3.1 Обзор международных источников
Изучение калориметрии берет свои корни еще в 18 веке. В 1780 г. французские ученые Антуан Лавуазье (1743 – 1794) и Пьер Симон Лаплас (1749 – 1827) предложили прибор для измерения удельных теплоемкостей, названный ими калориметром. Основу калориметра составляет теплоизолированный сосуд и калориметрическое тело, в котором поглощается или выделяется тепло. Прибор состоит из углеродной мишени, в которой происходит генерация вторичных частиц – нейтральных ионов, которые, распадаясь, формируют поток фотонов.
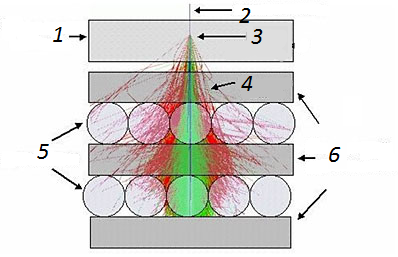
Рисунок 1 – Калориметр 18 века
1– углеродная мишень, 2– первичная частица, 3– место взаимодействия, 4– вторичные частицы,
5– детекторы, 6– свинцовый поглотитель.
Они регистрируются слоями детекторов, расположенных между поглотителями и свинца под мишенью. Измеряя количество вторичных частиц, можно определить энергию первичной. Чем больше слоёв детекторов, тем точнее измеряемая энергия. В 1750 г. петербургский физик Георг Рихман (1711 – 1753), работавший в содружестве с М. В. Ломоносовым, установил на опыте, что если смешать равные количества воды, имеющие различную температуру, то температура смеси будет равна среднему арифметическому температур частей. Эти опыты были повторены в 1772 г. Иоганном Вильке в Германии. Вильке ввел единицу измерения количества теплоты – калорию как количество теплоты, необходимой для изменения температуры единицы массы воды на один градус. Она сохранилась до наших дней [14].
Одновременно развиваются статистические представления. Больцман находит точную связь между средней энергией теплового движения частиц и температурой, вводя новую мировую константу, названную его именем.
Современные калориметры работают в диапазоне температур от 0,1 до 3500 К и позволяют измерять количество теплоты с точностью до 10–20%. Устройство калориметров весьма разнообразно и определяется характером и продолжительностью изучаемого процесса, областью температур, при которых производятся измерения, количеством измеряемой теплоты и требуемой точностью.
В начале 20 века была издана первая монография по калориметрии, написанная Вайтом [11] в 1928 году.
В 1946 Свитославским С.И. [12] было впервые введено такое понятие, как микрокалориметрия, где была изложена история развития теплофизических величин, которые играют важную роль в современной промыщленности, приведено описание, метрологические характеристики, принципы дейстия эталонов единиц этих величин.
В области калориметрии произошел прогресс, что привело к значительным достижениям в экспериментальной калориметрии. В 1989 году Хеммингер выпускает книгу, где четко изложено принципы калориметричеких методов, классификация калориметров и обработки результатов калориметрических измерений, приведено множество математических моделей, позволяющих проводить сравнительную характеристикуразличных калориметрических методик [1].
В 1963 году Кальве и Прат в своем издании описали изобретение нового типа калориметра – теплопроводящего. Несмотря на внешние изолирующие оболочки, он не адиабатичен, так как теплота, выделяющаяся в нем, выводится из калориметрической камеры по мере ее выделения и рассеивается в большом металлическом блоке. В калориметре Тиана–Кальве хоть температура калориметрической системы изменяется незначительно, прибор нельзя назвать изотермическим, так как в нем обнаруживаются небольшие изменения температуры, которые неизбежны и служат основой измерений [2].
Стандартные состояния для калориметрической бомбы в середине 20 века впервые описал Эдвард Вашбурн. В его работах подробно описаны исследования термодинамических условий, существующих в калориметрической бомбе [3]. Экспериментальной термодинамикой и адиабатическими калориметрами занималась команда ученых, в составе которой были Веструм Е.Ф., Фурукава Г.Т., Маккаллог Д.П. [6].
В 1990 году Бернштейном В.А и Егоровым В.М. был разработан метод, сочетающий качества традиционной калориметрии и динамического анализа тепловых процессов, имеющий название дифференциальная сканирующая калориметрия. Этот метод позволяет определять как термодинамические параметры веществ (теплоемкость, температуру, энтальпию и энтропию фазовых переходов, энергетические измерения разной природы), так и кинетические характеристики процессов в условиях линейно программируемого измерения температуры [9].
3.2 Обзор национальных источников
Отечественные ученые впервые плотно занялись калориметрическими исследованиями в начале 20 века. В 1914 году Попов М.М. под руководством Свентославского В.А. в журнале русского физико–химического общества выпустил свою первую научную работу «О калориметрической бомбе и теплоте горения бензойной кислоты». Большое внимание Попов уделял совершенствованию методики калориметрических измерений. Ему принадлежит идея и первая в мире конструкция калориметра с движущейся бомбой, разработанная в 1933 году, что впоследствии стало применяться во всех термохимических лабораториях. Также Поповым М.М. вместе с учениками были разработаны и построены калориметры для измерения теплоемкости при высоких (до 1200 К) и низких (от 60 до 300 К) температурах, калориметры для определения теплоты растворения солей и теплоемкостей их водных растворов [4].
В конце 20 века в калориметрии начали открываться новые отрасли. Так, в 1981 году Анатычук Л.И. и Лусте О.Я. установили, что микрокалориметрические эксперименты позволяют устанавливать порядок реакций, константы равновесия, выявлять нефиксируемые иными методами особенности уменьшения концентрации реагентов во времени [8].
Впоследствии появились методики, способствующие найти оптимальный путь по экспериментальному определению требуемой калориметрической величины, который был бы наименее трудоёмким и обеспечивал бы достаточную точность результатов, используя при этом уже хорошо апробированные и детально разработанные аппаратуру и способы измерений. Это было предложено Кирьяновым К.В. в «Калориметрических методах исследования» [5].
Различные конструкции теплообменных аппаратов были описаны Вяхиревым Р.А. в Российской газовой энциклопедии [10].
Вопросы, касающиеся исследования образцовых мер количества теплоты в калориметрии сжигания и методов и средства калориметрии теплофизических измерений, были рассмотрены Александровым Ю.И. и Осиповым Т.Р. [7].
В Национальной академии наук Украины Степкиным А.А. было написано множество работ, посвященных калориметрическим исследованиям. В своей диссертационной работе он провел сравнительный анализ и разработку дифференциальных и мостовых калориметров с термоэлектрическими и резистивными элементами [13].
3.3 Обзор локальных источников
В Донецком национальном техническом университете темой, касающейся калориметрических исследований, изучали следующие студенты: Борисенков А. Д. Пьянков М. В., Прохорова Е.В., Трач Д.С., Пивоваров Д.А., Киливник О.С.,
4. Калориметрия
Основной задачей при использовании природного газа является его рациональное потребление, то есть снижение удельного расхода посредством внедрения экономических технологических процессов, при которых наиболее полно реализуются положительные свойства газа.
Применение газового топлива позволяет избежать потерь теплоты, определяемых механическим и химическим недожогом. Уменьшение потерь теплоты с уходящими продуктами горения достигается сжиганием газа при малых коэффициентах расхода воздуха.
При работе агрегатов на газовом топливе возможно также ступенчатое использование продуктов горения. Для того, чтобы использование газа было наиболее рациональным, необходимо определять его теплотворную способность. Именно для этого существуют колориметры.
Калориметр представляет собой устройство настольного типа. Принцип действия калориметра заключается в измерении изменения температуры калориметрической системы с заранее известным энергетическим эквивалентом при сжигании строго определенного количества исследуемого топлива.
Удельная теплота сгорания топлива определяется по формуле:
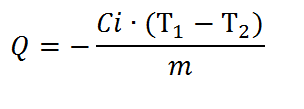
где С i – энергетический эквивалент калориметра, Т1 – теоретическое значение, Т2– экспериментальное значение, m – масса образца топлива.
В калориметре В–08 М изменение температуры производится с помощью метастатического термометра и оптического устройства.
Калорийность (теплоту сгорания) образца можно определить в широком смысле как количество тепла, освобожденного еденицей массы образца при сгорании в кислородной среде в замкнутом постоянном объеме. При этой реакции образец и кислород вначале имеют одинаковую температуру, и продукты сгорания охлаждаются на несколько градусов от начальной температуры. Водяной пар, образующийся при сгорании, конденсируется в жидком состоянии. Более точное определение должно бы указывать температуру, при которой реакция начинается и заканчивается.
Однако изменение теплоты сгорания при возможных вариациях начальной температуры являются такими незначительными, что подобная детализация не требуется. К тому же, температуры начала и окончания не совпадают, различаясь по величине повышения температуры в калориметре – но влияние этой разницы настолько мало, что им пренебрегают. Следовательно, термин калорийность (или теплота сгорания) при измерении в бомбовом калориметре означает количество тепла освобожденного при сгорании всего углерода и водорода в кислороде и образованием двуокиси углерода и воды, включая тепло, освобожденное при окислении других элементов (таких как сера), которые могут присутствовать в образце.
Теплота сгорания, определенная в кислородном бомбовом калориметре измеряется в процессе замещения, при котором теплота, полученная от образца сравнивается с теплотой, полученной от сгорания подобного количества бензольной кислоты или другого стандартизованного материала с известной калорийностью. Эти измерения получаются путем представленного образца в кислородной среде под давлением в металлических сосудах высокого давления, так называемых «бомбах». Энергия полученная при этом сгорании поглощается в калориметре. При этом фиксируется происходящее изменение температур в поглощающей среде. Затем теплота сгорания образца рассчитывается путем умножения величины повышения температуры в калориметре на ранее определенный энергетический эквивалент или теплоемкость, определенную при предыдущих испытаниях со стандартизованным материалом. При этом следует вводить поправки, чтобы подвести эти величины к любой передаче теплоты, происходящей в калориметре, а также учесть любые побочные реакции, являющиеся уникальными в процессе сгорания в бомбе.
Любой бомбовый калориметр должен состоять из четырех основных частей:
1. Бомба или сосуд, в котором производится сжигание заряда.
2. Короб или контейнер, для погружения бомбы в измеренное количество воды, вместе с датчиком температуры и механизмом управления.
3. Изолирующая оболочка для защиты короба от неустановившейся тепловой нагрузки во время процесса сгорания.
4. Термометр или другой датчик для измерения изменений температуры в контейнере.
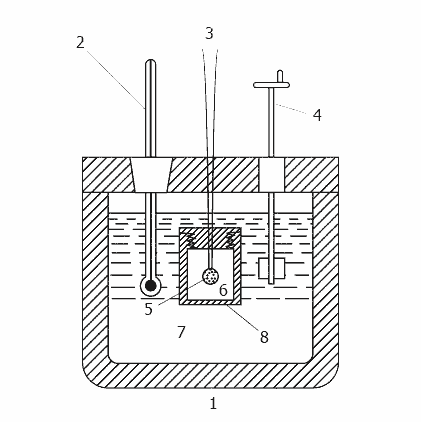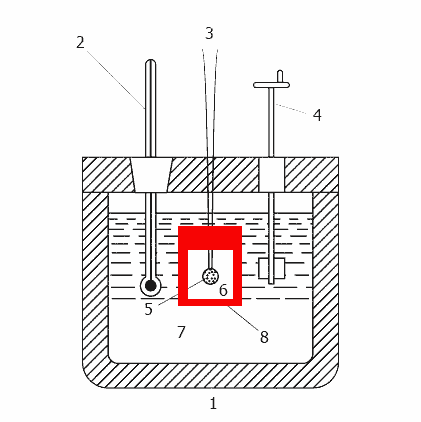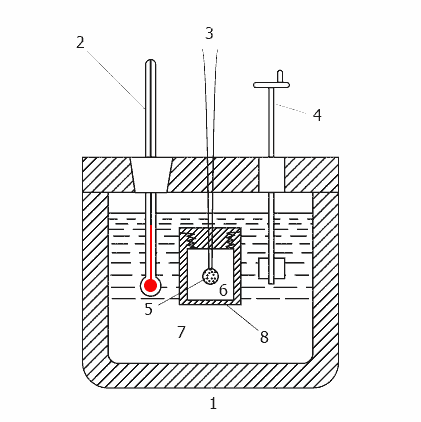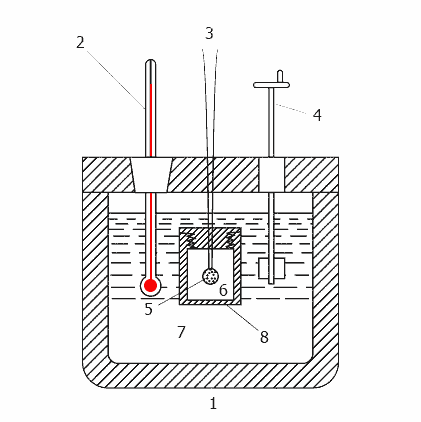
Рисунок 2 – Принцип действия калориметра
(анимация: 11 кадров, 13 циклов повторения, 20 килобайт)
1–теплоизолированный корпус, 2– термометр, 3– провода для поджига, 4– мешалка, 5– образец, 6– кислород, 7– вода,
8– бомба
Бомба представляет из себя прочный металлический сосуд с толстыми стенками, который можно открывать для помещения образца, для извлечения продуктов сгорания и для очистки. Должны быть предусмотрены трубки для заполнения бомбы кислородом под давлением и для выпуска оставшихся газов после завершения испытания. Кроме этого, бомба укомплектовывается электродами для подачи тока зажигания на провод запала. Поскольку во время зажигания внутреннее давление может доходить до 1500 фунтов на квадратный дюйм, большинство кислородных бомб рассчитаны на давление не менее 3000 фунтов на квадратный дюйм.
Выводы
В кислородных бомбовых калориметрах используется несколько систем оболочек. Простейшие из них являются нерегулируемыми или оболочками с простой изоляцией. При использовании этого типа оболочки предполагается, что температура оболочки, остается постоянной во время всего испытания без применения специальной системы регулировки температуры. Учитывая простоту, калориметры с простой изоляцией рекомендуются в качестве недорогих приборов для пользователей, которые только время от времени проводят калориметрические испытания или для тех пользователей, чья рабочая загрузка не оправдывает затрат на покупку моделей с регулировкой температуры. Калориметры с простой оболочкой не требуют постоянного подключения. Его можно настроить и подготовить к работе за несколько минут, если калориметр не используется, то его можно легко разобрать и положить на хранение.
Список источников
- Хеммингер В., Хене Г. Калориметрия. Теория и практика. М.: Химия. 1989. 176 с.
- Кальве Э., Прат А. Микрокалориметрия. М.: Изд–во ин. лит. 1963. 477 с.
- Washburn E.W. Standard states for bomb calorimetry. J. Res. Nat. Bur. Standards. 10. 1933. P. 525
- Попов М.М. Термохимия и калориметрия. 2–е изд. М.: 1954.
- Кирьянов К.В. Калориметрические методы исследования. Нижний Новгород, 2007, 76 с.
- Westrum E.F., Furukawa G.T., McCullough J.P. Adiabatic Low–temperature Calorimetry.Experimental Thermodynamics. V. I. Ed. McCullough J.P., Scott D.W. L.: Butterworths, 1968.
- Александров Ю.И., Осипова Т.Р., Юшкевич В.Ф. Исследование образцовых мер количества теплоты в калориметрии сжигания. Методы и средства калориметрии теплофизических измерений. Л., 1984. 250 с.
- Анатычук Л.И., Лусте О.Я. Микрокалориметрия. Львов: Вища школа. Изд–во при Львов. гос. ун–те. 1981. 160 с.
- Бернштейн В.А., Егоров В.М. Дифференциальная сканирующая калориметрия в физикохимии полимеров. Л.: Химия, 1990. 256 с.
- Вяхирев Р.А. Российская газовая энциклопедия, М: 2004, 527 с.
- Вайт П.А. Современная калориметрия, Л:1928, 340 с.
- Свитославский С.И. Микрокалориметрия, М:1946, 280 с.
- Сравнительный анализ и разработка дифференциальных, мостовых калориметров с термоэлектрическими и резистивными элементами [Электронный ресурс]. – Режим доступа: http://tekhnosfera.com/view/62460/a?#?page=20.
- История калориметрии . [Электронный ресурс]. – Режим доступа: http://www.kipstory.ru/pribori/color/.
